|
|
(21), (22) Заявка: 2005105143/13, 24.02.2005
(24) Дата начала отсчета срока действия патента:
24.02.2005
(46) Опубликовано: 27.09.2006
(56) Список документов, цитированных в отчете о
поиске:
RU 2157829 C1, 20.10.2000. RU 2181757 C2, 27.04.2002. ЭМАНУЭЛЬ Н.N., ЛЯСКОВСКАЯ Ю.Н. Торможение процессов окисления жиров. – М.: Пищепромиздат, 1961, с.236-282.
Адрес для переписки:
625000, г.Тюмень, ул. Володарского, 38, ТюмГНГУ, патентно-информационный отдел
|
(72) Автор(ы):
Перевозкина Маргарита Геннадьевна (RU),
Сторожок Надежда Михайловна (RU),
Никифоров Григорий Алексеевич (RU)
(73) Патентообладатель(и):
Государственное образовательное учреждение высшего профессионального образования “Тюменский государственный нефтегазовый университет” (RU)
|
(54) СОСТАВ ДЛЯ СТАБИЛИЗАЦИИ ЛИПИДОВ
(57) Реферат:
Изобретение относится к масложировой промышленности. Состав для стабилизации липидов включает фенольный антиоксидант. При этом в качестве фенольного антиоксиданта используют индивидуальный N,N,N-триметиламиноэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил) пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил) пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид, в концентрациях от 0,10 до 5,00 мМ. Фенольный антиоксидант добавляют в количестве 0,01-0,68% от массы липидов. Изобретение позволяет повысить ингибирующий эффект при наименьших концентрациях антиоксиданта. 3 табл. ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид, в концентрациях от 0,10 до 5,00 мМ. Фенольный антиоксидант добавляют в количестве 0,01-0,68% от массы липидов. Изобретение позволяет повысить ингибирующий эффект при наименьших концентрациях антиоксиданта. 3 табл.
Изобретение относится к области пищевой технологии, а именно к способам защиты липидов, масел, жиров от окисления и окислительной деструкции, и может быть использовано в пищевой, косметической и химико-фармацевтической промышленности для получения стабильных липидсодержащих пищевых добавок (нутрицевтиков), лечебно-косметических средств и лекарственных препаратов.
Известен состав для стабилизации липидов, включающий природный фенольный антиоксидант ( -токоферол или -токоферол или  -токоферол ацетат) и L-карнитин, действующий как синергист по отношению к ингибитору окисления, при следующих соотношениях компонентов: -токоферол ацетат) и L-карнитин, действующий как синергист по отношению к ингибитору окисления, при следующих соотношениях компонентов:  -токоферол или -токоферол или  -токоферол ацетат 75,0-94,5%; L-карнитин 5,5-25,0%, добавляемых в концентрации 0,28-0,50% от массы липидов /патент 2157829 RU, МПК С 11 В 5/00, опубликованный 20. 10. 2000 г./. -токоферол ацетат 75,0-94,5%; L-карнитин 5,5-25,0%, добавляемых в концентрации 0,28-0,50% от массы липидов /патент 2157829 RU, МПК С 11 В 5/00, опубликованный 20. 10. 2000 г./.
 -Токоферол(6-гидрокси-2,5,7,8-тетраметил-2-фитил хроман) является наиболее изученным природным антиоксидантом. Свойства -Токоферол(6-гидрокси-2,5,7,8-тетраметил-2-фитил хроман) является наиболее изученным природным антиоксидантом. Свойства  -токоферола как антиоксиданта проявляются в целом ряде сложных эффектов на всех уровнях организации от мембранных образований до организма в целом. /Ленинжер А. Основы биохимии. – М.: – Мир. – 1985. – T.1. – 385 с./. -токоферола как антиоксиданта проявляются в целом ряде сложных эффектов на всех уровнях организации от мембранных образований до организма в целом. /Ленинжер А. Основы биохимии. – М.: – Мир. – 1985. – T.1. – 385 с./.
С целью расширения ассортимента нетоксичных биологически активный антиоксидантов в Институте биохимической физики (ИБХФ) им. Н.М.Эмануэля РАН на основе фенозана (метилокса) ( -3,5-дитрет.бутил-4-гидроксифенилпропионовой кислоты) синтезированы стерически затрудненные фенолы: N,N,N-триметиламиноэтиловый эфир -3,5-дитрет.бутил-4-гидроксифенилпропионовой кислоты) синтезированы стерически затрудненные фенолы: N,N,N-триметиламиноэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид и N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид и N,N-диметил-N-гексадецил-аминоэтиловый эфир   ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида и N,N-диметил-N-гексадецил-аминоэтилового эфира ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида и N,N-диметил-N-гексадецил-аминоэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида была определена острая токсичность при однократном введении препарата белым беспородным мышам по Прозоровскому. Для N,N,N-триметиламиноэтилового эфира ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида была определена острая токсичность при однократном введении препарата белым беспородным мышам по Прозоровскому. Для N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида ЛД50 составляет 41 мг/кг, при пероральном введении – 221 мг/кг, для N,N-диметил-N-гексадецил-аминоэтилового эфира ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида ЛД50 составляет 41 мг/кг, при пероральном введении – 221 мг/кг, для N,N-диметил-N-гексадецил-аминоэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида ЛД50 составляет 65 мг/кг (внутрибрюшинно). ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида ЛД50 составляет 65 мг/кг (внутрибрюшинно).
Предложенные производные фенозана, в отличие от  -Токоферола, обладают бифункциональными свойствами – антиокислительным действием и наличием в молекуле положительно заряженного атома азота, позволяющего удерживать ее на поверхности клеточных мембран с фиксацией на определенном месте за счет липовильного фрагмента (поплавковый эффект). Подобная структура обеспечивает адресную посылку антиоксидантов и создает возможность использования их для подавления патологических процессов в клетке организма, при которых нарушаются проницаемость клеточных мембран и интенсифицируются процессы перекисного окисления липидов. -Токоферола, обладают бифункциональными свойствами – антиокислительным действием и наличием в молекуле положительно заряженного атома азота, позволяющего удерживать ее на поверхности клеточных мембран с фиксацией на определенном месте за счет липовильного фрагмента (поплавковый эффект). Подобная структура обеспечивает адресную посылку антиоксидантов и создает возможность использования их для подавления патологических процессов в клетке организма, при которых нарушаются проницаемость клеточных мембран и интенсифицируются процессы перекисного окисления липидов.
На основе такого подхода новые производные фенозана могут применяться для лечения заболеваний, вызываемых вирусом иммунодефицита, цитомегаловирусом, а также при воспалительных заболеваниях, вызванных грамположительными бактериями (стафилококки, менингококки) и др.
N,N,N-триметиламиноэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид проявляют активность в реакции с пероксидными радикалами и обладают дополнительно способностью непосредственно взаимодействовать с гидропероксидами, разрушая их без образования свободных радикалов, что не наблюдается в присутствии ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид проявляют активность в реакции с пероксидными радикалами и обладают дополнительно способностью непосредственно взаимодействовать с гидропероксидами, разрушая их без образования свободных радикалов, что не наблюдается в присутствии  -токоферола. Разрушение гидропероксидов под влиянием изучаемых соединений, в свою очередь, является причиной выигрыша в периодах индукции и ведет к обеспечению высокой эффективности изучаемых соединений по сравнению с прототипом. -токоферола. Разрушение гидропероксидов под влиянием изучаемых соединений, в свою очередь, является причиной выигрыша в периодах индукции и ведет к обеспечению высокой эффективности изучаемых соединений по сравнению с прототипом.
Для изучаемых синтетических антиоксидантов имеет место положительная корреляционная связь между концентрацией и величиной ингибирующего эффекта, что не наблюдается для  -токоферола, указанная зависимость имеет экстремальный характер и при высоких концентрациях антиоксидантное действие -токоферола, указанная зависимость имеет экстремальный характер и при высоких концентрациях антиоксидантное действие  -токоферола сменяется на проантиоксидантное. -токоферола сменяется на проантиоксидантное.
Задачей предлагаемого изобретения является экономия использования дорогостоящих соединений, достижение ингибирующего эффекта меньшим количеством антиоксиданта.
Техническим результатом изобретения является упрощение состава и повышение его ингибирующего эффекта при наименьших концентрациях антиоксидантов.
Указанный технический результат достигается тем, что в состав для стабилизации липидов, включающий фенольный антиоксидант, в качестве которого использован индивидуальный N,N,N-триметиламиноэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид, в следующих концентрациях, ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид, в следующих концентрациях,
| N,N,N-триметиламиноэтиловый эфир |
|
 ‘-(3,5-дитрет.бутил-4-гидрокси-фенил) ‘-(3,5-дитрет.бутил-4-гидрокси-фенил) |
|
| пропановой кислоты иодид |
от 0,10 до 5,00 мМ, |
или
| N,N-диметил-N-гексадецил-аминоэтиловый эфир |
|
 ‘-(3,5-дитрет.бутил-4-гидрокси-фенил) ‘-(3,5-дитрет.бутил-4-гидрокси-фенил) |
|
| пропановой кислоты)бромид |
от 0,10 до 5,00 мМ, |
добавляемых в количестве 0,01-0,68% от массы липидов.
Предлагаемые соединения обладают сравнимой антиоксидантной активностью, имеют близкое химическое строение и могут быть взаимозаменяемыми.
– изучалась кинетика поглощения кислорода при инициированном окислении липидных субстратов различного происхождения в присутствии предлагаемого состава и прототипа;
– тестировалась кинетика накопления первичных продуктов окисления – гидропероксидов методом иодометрического титрования (ПЧ) при аутоокислении липидов в при повышенных температурах (60±0,2°С)
Изучение кинетики поглощения кислорода проводилось манометрическим методом в установках типа Варбурга при инициированном окислении липидов в присутствии инициатора азобисизобутиронитрила (АИБН) в концентрации 3 мМ при температуре 60±0,5°С. Контролем служили образцы липидов без добавок антиоксидантов.
Эффективность индивидуальных компонентов и их комбинаций исследовалась в широком диапазоне концентраций:
| N,N,N-триметиламиноэтиловый эфир |
|
 ‘-(3,5-дитрет.бутил-4-гидрокси-фенил) ‘-(3,5-дитрет.бутил-4-гидрокси-фенил) |
|
| пропановой кислоты иодид |
от 0,10 до 5,00 мМ |
или
| N,N-диметил-N-гексадецил-аминоэтиловый эфир |
|
 ‘-(3,5-дитрет.бутил-4-гидрокси-фенил) ‘-(3,5-дитрет.бутил-4-гидрокси-фенил) |
|
| пропановой кислоты)бромид |
от 0,10 до 5,00 мМ |
что составляло для указанных выше компонентов (0,01-0,68%) от массы липидов.
В присутствии определенной добавки индивидуальных ингибиторов окисления  -токоферола, N,N,N-триметиламиноэтилового эфира -токоферола, N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтилового эфира ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, а также прототипа записывалась кинетика окисления с использованием вышеописанных методов. На основании полученных данных строились кинетические кривые поглощения кислорода (мм3 O2) либо накопления пероксидов (г I2/100 г липида). ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, а также прототипа записывалась кинетика окисления с использованием вышеописанных методов. На основании полученных данных строились кинетические кривые поглощения кислорода (мм3 O2) либо накопления пероксидов (г I2/100 г липида).
Из кинетических кривых определялись периоды индукции ( ), за которые принимали: ), за которые принимали:
– время (в мин), за которое процесс инициированного окисления липидов достигал максимальной скорости ( инд). инд).
– время (в часах) накопления пероксидов, количественно соответствующих значению ПЧ 0,1% I2.
Ингибирующее действие индивидуальных компонентов и их смесей оценивали по абсолютному значению разницы между периодами индукции окисления субстратов с индивидуальным антиоксидантом ( АО), смесью стабилизирующих добавок ( АО), смесью стабилизирующих добавок ( инг.) и без них ( инг.) и без них ( о) по формуле о) по формуле
 = =  = = инг– инг– AO, AO,
либо выражали ее в относительных единицах   / / АО, в %. АО, в %.
Критерием антиоксидантного действия служили начальная (Wo2 нач×10-7, М×c-1) и максимальная (Wo2 max×10-7, М×c-1) скорость процесса окисления в присутствии и в отсутствии антиоксиданта. Эффективность стабилизации окисления определяли также по величине Wo2 max (МО)/Wo2 max (МО+AO), количественно характеризующем степень уменьшения скорости поглощения кислорода в присутствии метилолеата (МО) и метилолеата с добавками индивидуальных антиоксидантов (АО).
Было установлено, что зависимость изменения периодов индукции для индивидуального  -токоферола носит экстремальный характер. Диапазон эффективных концентраций расположен в области (0,25-8,0) мМ, что соответствует (0,03-1,08) % от массы липидов, максимум указанной зависимости определялся при концентрации 2,5 мМ (0,34% от массы липидов). Зависимости изменения величины периодов индукции от концентрации N,N,N-триметиламиноэтилового эфира -токоферола носит экстремальный характер. Диапазон эффективных концентраций расположен в области (0,25-8,0) мМ, что соответствует (0,03-1,08) % от массы липидов, максимум указанной зависимости определялся при концентрации 2,5 мМ (0,34% от массы липидов). Зависимости изменения величины периодов индукции от концентрации N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида в системе окисления носили линейный характер, указанные соединения превосходили по своему ингибирующему действию смесь ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида в системе окисления носили линейный характер, указанные соединения превосходили по своему ингибирующему действию смесь  -токоферола с L-карнитином. -токоферола с L-карнитином.
Сущность изобретения иллюстрируется следующими примерами:
ПРИМЕР 1
Берут 10 г (точная навеска) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0078 г N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, что составляет соответственно 0,08% от массы липидов. ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, что составляет соответственно 0,08% от массы липидов.
ПРИМЕР 2
Берут 10 г (точная навеска) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата. Добавляют 0,0049 г N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, что составляет соответственно 0,05% от массы липидов. ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, что составляет соответственно 0,05% от массы липидов.
ПРИМЕР 3
Берут 10 г (точная навеска) рыбных липидов, например липидов сиговых рыб. Добавляют 0,0108 г N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, что составляет 0,11% от массы липидов. ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, что составляет 0,11% от массы липидов.
ПРИМЕР 4
Берут 10 г (точная навеска) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0027 г N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, что составляет соответственно 0,03% от массы липидов. ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, что составляет соответственно 0,03% от массы липидов.
ПРИМЕР 5
Берут 10 г (точная навеска) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0338 г N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, что составляет соответственно 0,34% от массы липидов. ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, что составляет соответственно 0,34% от массы липидов.
ПРИМЕР 6
Берут 10 г (точная навеска) эфиров ненасыщенных высших жирных кислот, например метилолеата или метиллинолеата, и добавляют 0,0676 г N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, что составляет соответственно 0,68% от массы липидов. ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, что составляет соответственно 0,68% от массы липидов.
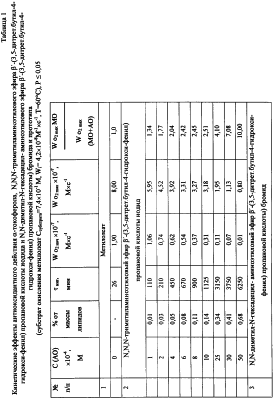
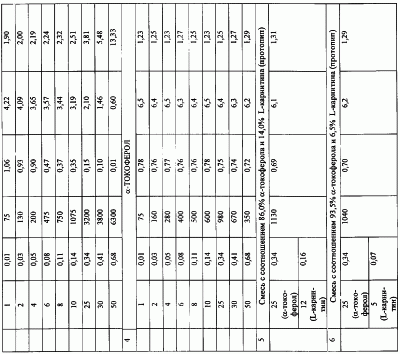
Эффективность ингибирующего действия указанных выше соединений оценивали на основании данных кинетики поглощения кислорода, получаемых с использованием манометрического метода, подробно изложенного в описании изобретения. Полученные результаты приведены в табл.1. Из данных табл.1 видно, что все рекомендуемые концентрации ингибиторов окисления превосходят по величине эффективности прототип. Наибольшую эффективность по сравнению с прототипом проявляет N,N,N-триметиламиноэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид, в концентрации 5 мМ, что составляет 0,68% от массы липидов. Так, при окислении метилолеата в присутствии N,N,N-триметиламиноэтилового эфира ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид, в концентрации 5 мМ, что составляет 0,68% от массы липидов. Так, при окислении метилолеата в присутствии N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтилового эфира ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, максимально достигаемый ингибирующий эффект составляет 6250 и 6300 мин соответственно, тогда как смесь ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида, максимально достигаемый ингибирующий эффект составляет 6250 и 6300 мин соответственно, тогда как смесь  -токоферола с L-карнитином (включающая 86,0% -токоферола с L-карнитином (включающая 86,0%  -токоферола и 14,0% L-карнитина) обеспечивает максимальный индукционный период в 1130 мин, при этом эффективность предлагаемой смеси выше эффективности прототипа на 453-458% -токоферола и 14,0% L-карнитина) обеспечивает максимальный индукционный период в 1130 мин, при этом эффективность предлагаемой смеси выше эффективности прототипа на 453-458%
Высокоэффективной является концентрация, приведенная в примере 5, соизмеримая с концентрацией  -токоферола в прототипе. При ингибировании окисления с добавками 2,5 мМ N,N,N-триметиламиноэтилового эфира -токоферола в прототипе. При ингибировании окисления с добавками 2,5 мМ N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтилового эфира ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида рыбных липидов индукционные периоды составили 1200 и 1250 мин соответственно. Следовательно, эффективной для метилолеата, а также рыбных липидов оказалась концентрация антиоксидантов 2,5 мМ, что составляет 0,34% от массы липидов ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида рыбных липидов индукционные периоды составили 1200 и 1250 мин соответственно. Следовательно, эффективной для метилолеата, а также рыбных липидов оказалась концентрация антиоксидантов 2,5 мМ, что составляет 0,34% от массы липидов
Эффективность указанной выше концентрации в идентичных условиях окисления была сопоставлена с периодами индукции опыт  -контроля (неингибированных липидов) и антиоксидантным действием прототипа (табл.1, 2). -контроля (неингибированных липидов) и антиоксидантным действием прототипа (табл.1, 2).
Было установлено, что эффективность использования новых антиоксидантов в разных субстратах составляет от (175-185)% по сравнению со смесью  -токоферола с L-карнитином (прототип) (табл.1). -токоферола с L-карнитином (прототип) (табл.1).
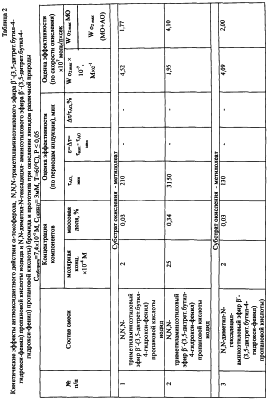
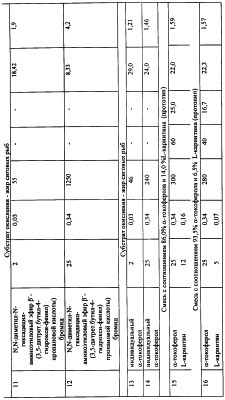
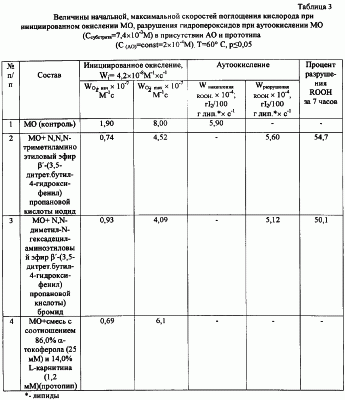
При изучении кинетики накопления гидропероксидов было показано, что периоды индукции в опытах с концентрацией N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтилового эфира ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтилового эфира  ‘-(3,5-дитретбутил-4-гидрокси-фенил)пропановой кислоты)бромида 0,2 мМ, добавляемой в количестве 0,03% от массы липидов, процент разрушения гидропероксидов составляет 54,7% и 50,1% соответственно, что не наблюдается в присутствии прототипа (табл.3). ‘-(3,5-дитретбутил-4-гидрокси-фенил)пропановой кислоты)бромида 0,2 мМ, добавляемой в количестве 0,03% от массы липидов, процент разрушения гидропероксидов составляет 54,7% и 50,1% соответственно, что не наблюдается в присутствии прототипа (табл.3).
Из сравнения ингибирующего действия исследуемых концентраций видно, что абсолютная величина периодов индукции наиболее эффективной концентрации N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтилового эфира ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтилового эфира 
Причинно-следственная связь между существенными признаками изобретения и достижением технического результата следующая. Эффекты ингибирования N,N,N-триметиламиноэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтилового эфира ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодида или N,N-диметил-N-гексадецил-аминоэтилового эфира  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида могут быть объяснены, исходя из представлений о механизме антиоксидантного действия используемых соединений. Установлено, что антиоксиданты воздействуют на сложный многостадийный процесс окисления по различным механизмам. ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромида могут быть объяснены, исходя из представлений о механизме антиоксидантного действия используемых соединений. Установлено, что антиоксиданты воздействуют на сложный многостадийный процесс окисления по различным механизмам.
Так, в соответствии с литературными данными  -токоферол проявляет чрезвычайно высокую активность в реакции с пероксидными радикалами (RO2 -токоферол проявляет чрезвычайно высокую активность в реакции с пероксидными радикалами (RO2  ), ведущими окисление. Константа скорости реакции токоферола с RO2 ), ведущими окисление. Константа скорости реакции токоферола с RO2  (реакции 7 согласно классической схемы) составляет 3,60×106 M-1×c-1, что превышает значение К7 (реакции 7 согласно классической схемы) составляет 3,60×106 M-1×c-1, что превышает значение К7
Таким образом, N,N,N-триметиламиноэтиловый эфир  ‘-(3.5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3.5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид проявляют активность в реакции с пероксидными радикалами с константой скорости реакции К7=0,59×104 M-1×c-1 и К7=0,94×104 M-1×c-1, соответственно, снижают скорость процесса окисления липидов в 5-10 раз, а также дополнительно снижают уровень гидропероксидов на 50-55% (табл.3). Разрушение гидропероксидов под влиянием изучаемых соединений, в свою очередь, является причиной выигрыша в периодах индукции и обеспечению высокой эффективности. ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид проявляют активность в реакции с пероксидными радикалами с константой скорости реакции К7=0,59×104 M-1×c-1 и К7=0,94×104 M-1×c-1, соответственно, снижают скорость процесса окисления липидов в 5-10 раз, а также дополнительно снижают уровень гидропероксидов на 50-55% (табл.3). Разрушение гидропероксидов под влиянием изучаемых соединений, в свою очередь, является причиной выигрыша в периодах индукции и обеспечению высокой эффективности.
Предлагаемый состав, включающий N,N,N-триметиламиноэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид значительно достигает эффекта ингибирования по сравнению с прототипом. Сочетание в одной композиции антиоксиданта, действующего на разные элементарные реакции сложного окислительного процесса, позволяет увеличить ингибирующую способность антиоксиданта и эффективно тормозить окисление полиненасыщенных субстратов. ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид значительно достигает эффекта ингибирования по сравнению с прототипом. Сочетание в одной композиции антиоксиданта, действующего на разные элементарные реакции сложного окислительного процесса, позволяет увеличить ингибирующую способность антиоксиданта и эффективно тормозить окисление полиненасыщенных субстратов.

Формула изобретения
Состав для стабилизации липидов, включающий фенольный антиоксидант, отличающийся тем, что в качестве фенольного антиоксиданта использован индивидуальный N,N,N-триметиламиноэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид, в концентрациях: ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой кислоты)бромид, в концентрациях:
| N,N,N-триметиламиноэтиловый |
|
эфир  ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой ‘-(3,5-дитрет.бутил-4-гидрокси-фенил)пропановой |
|
| кислоты иодид |
от 0,10 до 5,00 мМ |
| или |
|
| N,N-диметил-N-гексадецил-аминоэтиловый эфир |
|
 ‘-(3,5-дитрет.бутил-4-гидрокси-фенил) ‘-(3,5-дитрет.бутил-4-гидрокси-фенил) |
|
| пропановой кислоты)бромид |
от 0,10 до 5,00 мМ |
добавляемых в количестве 0,01-0,68% от массы липидов.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 25.02.2008
Извещение опубликовано: 10.12.2009 БИ: 34/2009
|
|

 ‘-(3,5-дитрет.бутил-4-гидрокси-фенил) пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир
‘-(3,5-дитрет.бутил-4-гидрокси-фенил) пропановой кислоты иодид или N,N-диметил-N-гексадецил-аминоэтиловый эфир  -токоферол или
-токоферол или  ), за которые принимали:
), за которые принимали: =
=
 ), ведущими окисление. Константа скорости реакции токоферола с RO2
), ведущими окисление. Константа скорости реакции токоферола с RO2 




