|
|
(21), (22) Заявка: 2005119813/04, 27.06.2005
(24) Дата начала отсчета срока действия патента:
27.06.2005
(46) Опубликовано: 20.08.2006
(56) Список документов, цитированных в отчете о
поиске:
РЕЗНИК Б.Е., ЦЫГАНОК Л.П. Известия Вузов. Химия и химическая технология. 1965, №3, с.412-416. RU 2161304 C1, 27.12.2000. RU 2126963 C1, 27.02.1999. RU 2201592 C2, 27.03.2003. SU 369472 A1, 12.04.1973. SU 336530 A1, 27.07.1972. SU 171655 A1, 23.06.1965. SU 260952 C1, 06.05.1970.
Адрес для переписки:
350040, г.Краснодар, ул. Ставропольская, 149, Кубанский государственный университет, отдел интеллектуальной собственности
|
(72) Автор(ы):
Темердашев Зауаль Ахлоович (RU),
Починок Татьяна Борисовна (RU),
Сынкова Татьяна Викторовна (RU)
(73) Патентообладатель(и):
Государственное образовательное учреждение высшего профессионального образования Кубанский государственный университет (КубГУ) (RU)
|
(54) СПОСОБ ОПРЕДЕЛЕНИЯ МЕДИ (II)
(57) Реферат:
Изобретение относится к аналитической химии, а именно к тест-методам анализа. Медь (II) определяют путем добавления к анализируемому раствору серной кислоты до рН 1-1.3 и 2.0-4.0 мл 2% раствора тиомочевины (ТМ). Объем исследуемого раствора доводят дистиллированной водой до 10 мл. Опускают тест-полосу, заранее пропитанную 2% раствором фосфорно-молибденовой кислоты (ФМК) и высушенную, и перемешивают. Определяют секундомером время изменения цвета тест-полосы до голубого. Достигается ускорение, упрощение и удешевление анализа. 6 табл., 2 ил.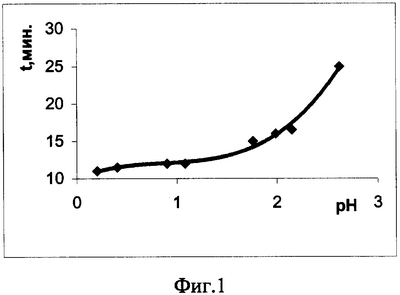
Изобретение относится к аналитической химии, а именно к тест-методам анализа.
Известен атомно-абсорбционный метод определения меди в растворах, контактирующих с силикатным эмалевым покрытием посуды [ГОСТ 24295-80. Посуда хозяйственная стальная эмалированная. Методы анализа вытяжек]. Метод основан на измерении поглощения излучения свободными атомами меди, образующимися при распылении анализируемых растворов в пламени воздух-ацетилен. Недостатками данного метода является необходимость использования сложного оборудования и привлечения для анализа высококвалифицированного персонала, высокая стоимость анализа.
Недостатком прототипа является его трудоемкость, длительность, необходимость инструментального определения оптической плотности, узкий интервал определяемых концентраций (1·10-5-1·10-6 М).
Технической задачей заявляемого изобретения является разработка тест-метода определения меди, позволяющего упростить анализ и снизить его стоимость и трудоемкость, а также расширить интервал определяемых концентраций.
Для решения технической задачи предлагается к 1.0 мл анализируемого раствора добавлять серную кислоту до рН 1-1.3, 2.0-4.0 мл 2% раствора тиомочевины (ТМ). При необходимости объем исследуемого раствора доводят дистиллированной водой до 10 мл. Опускают тест-полосу, заранее пропитанную 2% раствором фосфорно-молибденовой кислоты (ФМК) и высушенную, и перемешивают аналит. Определяют секундомером время изменения цвета тест-полосы до голубого. Аналогичным образом измеряют время реакции для стандартных растворов меди. Концентрацию меди (II) в растворе (Сх) находят методом ограничивающих растворов (двух стандартов) или методом градуировочного графика, используя линейность зависимости времени появления голубой окраски от величины рСCu (т.е. -IgCCu). Например, в методе ограничивающих растворов рассчитывают величину рСх по формуле 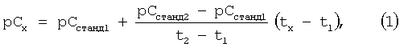
где рСх=-рСх для исследуемого раствора, рСстанд1=-lgCстанд1 для раствора с концентрацией, меньшей, чем Сх; рСстанд2=-lgCстанд2 для раствора с концентрацией, большей, чем Сх; t1, t2, tx – время реакции соответственно для растворов с концентрацией Сстанд1, Сстанд2 и Сх.
На фиг.1 изображен график зависимости времени реакции от рН; на фиг.2 – градуировочный график.
Для подбора оптимальных условий тест-определения меди готовили тест-полосы путем пропитки фильтровальной бумаги растворами ФМК 1,5%, 2,0% и 2,5%, после чего высушивали досуха. В анализируемом растворе варьировали содержание ТМ (таблица 1). Тест-полосы опускали в раствор с известной концентрацией меди и засекали время, за которое цвет тест-полосы изменится до голубого.
Таблица 1
Состав рабочих растворов и результаты опытов |
| № опыта |
 (ФМК), % (ФМК), % |
Состав рабочих растворов, мл |
Время изменения цвета, мин |
| CuCl2, 0.01 М |
H2SO4, 3 М |
ТМ, 2% |
H2O |
| 1 |
2,5 |
0,5 |
2,0 |
2,0 |
5,5 |
6,5 |
| 2 |
0,5 |
2,0 |
2,5 |
5,0 |
6,0 |
| 3 |
0,5 |
2,0 |
3,5 |
4,0 |
5,0 |
| 4 |
0,5 |
2,0 |
4,0 |
3,5 |
4,0 |
| 5 |
2,0 |
0,5 |
2,0 |
2,0 |
5,5 |
7,0 |
| 6 |
0,5 |
2,0 |
2,5 |
5,0 |
6,5 |
| 7 |
0,5 |
2,0 |
3,5 |
4,0 |
5,5 |
| 8 |
0,5 |
2,0 |
4,0 |
3,5 |
4,5 |
| 9 |
1,0 |
0,5 |
2,0 |
2,0 |
5,5 |
8,5 |
| 10 |
0,5 |
2,0 |
2,5 |
5,0 |
7,5 |
| 11 |
0,5 |
2,0 |
3,5 |
4,0 |
6,0 |
| 12 |
0,5 |
2,0 |
4,0 |
3,5 |
5,5 |
Оптимальными были выбраны 5-8 варианты, так как в этом случае наблюдается большее разрешение изменения цвета тест-полосы. При концентрации ФМК больше 2% раствор окрашивается в желтый цвет, а при концентрации меньше 2% время анализа увеличивается, что нежелательно для тест-определения.
В качестве оптимального был выбран общий объем системы с анализируемым раствором 10 мл, что обусловлено удобством работы с твердым носителем и невысоким расходом реактивов.
Диапазон оптимальных значений рН определяли, измеряя время изменения цвета тест-полосы в растворах с разным значением рН и постоянной концентрацией всех остальных компонентов. Готовили растворы, состав которых приведен в таблице 2. Кислотность растворов варьировали, добавляя разное количество серной кислоты и измеряя значение рН на иономере «Эксперт-001» с комбинированным стеклянным электродом.
Таблица 2
Определение оптимального диапазона рН |
| № |
Состав раствора, мл |
рН |
Время изменения цвета, мин |
| 10-4 CuCl2, |
ТМ 2% |
H2SO4, 3 М |
H2SO4, 0.3 М |
H2SO4, 0.03 М |
Н2O |
| 1 |
1.0 |
3.5 |
3.5 |
– |
– |
2.0 |
0.20 |
11.0 |
| 2 |
1.0 |
3.5 |
2.0 |
– |
– |
3.5 |
0.40 |
11.5 |
| 3 |
1.0 |
3.5 |
– |
5.5 |
– |
– |
0.90 |
12.0 |
| 4 |
1.0 |
3.5 |
– |
3.5 |
– |
2.0 |
1.08 |
12.0 |
| 5 |
1.0 |
3.5 |
– |
– |
5.0 |
0.5 |
1.76 |
15.0 |
| 6 |
1.0 |
3.5 |
– |
– |
3.0 |
2.5 |
1.99 |
16.0 |
| 7 |
1.0 |
3.5 |
– |
0.25 |
– |
5.25 |
2.15 |
16.5 |
| 8 |
1.0 |
3.5 |
– |
– |
0.5 |
5.0 |
2.62 |
>25 |
В соответствии с полученными данными построили график зависимости времени изменения цвета тест-полосы до голубого от рН среды, из которого видно, что в кислых растворах с рН до 1,3 кислотность раствора практически не влияет на время реакции (фиг.1).
Полученные данные о влиянии рН раствора на тест-определение использовались при установлении диапазона определяемых концентраций. Для этого готовили рабочие растворы в соответствии с таблицей 3. В пробирки с приготовленными растворами опускали тест-полосы, пропитанные 2% раствором ФМК, и засекали время, за которое цвет тест-полосы изменится до голубого. Полученные результаты представлены в таблице 3.
Таблица 3
Зависимость времени изменения цвета тест-полосы от концентрации меди в растворе |
| Состав раствора, мл |
Cобщ, CuCl2 |
Время, мин |
| CuCl2 1·10-2 M |
CuCl2 1·10-3 M |
CuCl2 1·10-4 M |
CuCl2 1·10-5 M |
H2SO4 3 М |
ТМ 2% |
Н2O |
| 1.0 |
– |
– |
– |
2.0 |
3.5 |
3.5 |
1·10-3 |
1.25 |
| 5.0 |
– |
– |
– |
2.0 |
3.5 |
4.0 |
5·10-4 |
2.50 |
| – |
0.7 |
– |
– |
2.0 |
3.5 |
3.8 |
7·10-5 |
4.33 |
| – |
0.3 |
– |
– |
2.0 |
3.5 |
4.2 |
3·10-5 |
5.00 |
| – |
– |
0.7 |
– |
2.0 |
3.5 |
3.8 |
7·10-6 |
5.50 |
| – |
– |
0.3 |
– |
2.0 |
3.5 |
4.2 |
3·10-6 |
6.67 |
| – |
– |
– |
0.7 |
2.0 |
3.5 |
3.8 |
7·10-7 |
7.15 |
| – |
– |
– |
0.2 |
2.0 |
3.5 |
4.3 |
2·10-7 |
7.80 |
| – |
– |
– |
– |
2.0 |
3.5 |
4.5 |
Хол. |
7.80 |
По полученным данным был построен градуировочный график (фиг.2). Из графика видно, что между временем тест-определения и величиной рС существует линейная зависимость. Диапазон линейности составил 1·10-3-1·10-7 М. При концентрации меди, меньшей 5·10-7 М, полученные значения времени сравнимы с фоновыми. При концентрациях меди, больших 1·10-3 M, время тест-определения меньше 30 с, что слишком мало для точного его измерения, кроме того, наблюдается окрашивание раствора в голубой цвет, что также мешает точному определению момента окончания реакции.
Для изучения мешающего влияния посторонних ионов на время тест-определения были выбраны вещества, которые, во-первых, могут взаимодействовать либо с ФМК, либо с тиомочевиной, во-вторых, содержат ионы, схожие по свойствам с медью, и, следовательно, могут обладать каталитическим действием на данную реакцию и, в-третьих, вещества, обладающие заметной окислительно-восстановительной активностью.
Путем последовательного разбавления готовили 10-1, 10-2, 10-3, 10-4 М растворы веществ, мешающее влияние которых будет изучаться. Готовили системы, содержащие медь и мешающий ион в соотношениях 1:1, 1:10, 1:100, 1:1000. Для этого в пробирку последовательно вносили 1 мл 10-4 М раствора CuCl2, 2 мл 3 М H2SO4, 3.5 мл 2% тиомочевины, 2,5 мл дистиллированной воды и добавляли 1 мл раствора постороннего иона концентрацией 10-1, 10-2, 10-3, 10-4 М соответственно. В раствор опускали тест-полосу и измеряли время изменения ее цвета до голубого. Полученные данные сравнивали с холостым опытом (см. табл.4).
Таблица 4
Зависимость времени изменения цвета тест-полосы от концентрации посторонних ионов |
| Посторонний ион |
Время реакции, мин |
| 10-5 M Cu |
1:1 |
1:10 |
1:100 |
1:1000 |
| Na+ |
8.5±0.7 |
8.0±0.7 |
8.0±0.7 |
8.5±0.7 |
8.5±0.7 |
| К+ |
8.5±0.7 |
8.5±0.7 |
9.0±0.8 |
8.0±0.7 |
8.5±0.7 |
| Са2+ |
8.5±0.7 |
9.0±0.8 |
8.0±0.7 |
8.5±0.7 |
8.5±0.7 |
| Ni2+ |
7.5±06 |
7.0±0.6 |
7.0±0.6 |
8.0±0.7 |
8.0±0.7 |
| Mg2+ |
7.5±0.6 |
7.5±0.6 |
8.0±0.7 |
8.5±0.7 |
8.5±0.7 |
| Zn2+ |
9.0±0.8 |
9.0±0.8 |
9.5±0.8 |
9.5±0.8 |
9.0±0.8 |
| Al3+ |
8.0±0.7 |
7.5±0.6 |
8.0±0.7 |
8.5±0.7 |
8.5±0.7 |
| Cl– |
8.5±0.7 |
8.0±0.7 |
8.0±0.7 |
8.5±0.7 |
8.5±0.7 |
| Br– |
8.5±0.7 |
8.5±0.7 |
8.5±0.7 |
9.0±0.7 |
9.0±0.8 |
| СН3СОО– |
8.5±0.7 |
8.0±0.7 |
8.0±0.7 |
8.0±0.7 |
8.5±0.7 |
| Мо |
9.0±0.8 |
8.5±0.7 |
8.5±0.7 |
8.0±0.7 |
7.5±0.6 |
| Cd2+ |
9.0±0.8 |
8.5±0.7 |
9.0±0.8 |
9.5±0.8 |
11.0±0.9 |
| Со2+ |
7.5±0.6 |
7.5±0.6 |
8.5±0.7 |
8.5±0.7 |
9.0±0.8 |
| РО3- 4 |
8.0±0.7 |
7.5±0.6 |
8.0±0.7 |
8.5±0.7 |
10.0±0.8 |
| Cr2O7 2- |
8.0±0.7 |
8.0±0.7 |
8.5±0.7 |
9.0±0.8 |
Цвет тест-полосы не определяется |
| Mn2+ |
8.0±0.7 |
7.5±0.6 |
8.5±0.7 |
9.5±0.8 |
9.5±0.8 |
| Pb2+ |
8.5±0.7 |
8.5±0.7 |
9.5±0.8 |
Цвет тест-полосы не определяется |
Цвет тест-полосы не определяется |
| Sr2+ |
8.5±0.7 |
9.0±0.8 |
9.5±0.8 |
10.0±0.8 |
11.0±0.9 |
| I– |
8.5±0.7 |
9.5±0.3 |
12.5±0.9 |
13.0±0.9 |
13.5±0.9 |
| Fe3+ |
6.5±0.6 |
8.5±0.7 |
11.5±0.9 |
14.0±0.9 |
>20.0 |
| Sn2+ |
8.5±0.7 |
6.5±0.6 |
5.0±0.6 |
<1 |
<1 |
| Sn4+ |
8.5±0.7 |
<3.0 |
<1 |
<1 |
<1 |
Было установлено, что Na, К, Са, Ni, Mg, Zn, Al, Cl, Br, ацетат-ионы тест-определению не мешают. Фосфат- и дихромат-ионы, а также Cd, Co и Мо (VI) мешают тест-определению при 1000-кратном избытке. При 100-кратном избытке Mn, Pb, Sr и 10-кратном избытке ионов I– скорость каталитической реакции уменьшается. Fe(III), Sn(II), Sn(IV) мешают определению меди уже при соотношении концентраций 1:1.
Правильность предложенной тест-методики проверяли на модельных растворах с использованием способа «введено-найдено» и реальных объектах. В модельные растворы с заранее известной концентрацией меди вносили тест-полосы и измеряли время изменения цвета тест-полосы до голубого. Концентрацию меди рассчитывали по методу ограничивающих растворов в соответствии с формулой (1) (табл.5).
Таблица 5
Результаты определения меди в модельных растворах (n=3, Р=0.95) |
| Объект анализа |
pCu (введено) |
pCu (найдено) |
| Модельные растворы |
4,0 |
4,3+0,4 |
| 5,0 |
5,3+0,4 |
| 5,3 |
5,8+0,5 |
Как видно из таблицы, отклонение между результатами составляет порядка 10%.
В качестве реальных объектов использовали фарфоровую, стеклянную и стальную посуду, контактирующую с пищевыми продуктами. В состав покрытий при использовании голубых глазурей могут входить соединения меди, концентрации которых нормируются. Результаты тест-определения сравнивали с данными метода ААС (см. табл.5 и табл.6).
Таблица 6
Результаты определения меди в реальных объектах (n=3, Р=0.95) |
| Объект анализа |
pCu (тест-определение) |
pCu (ААС) |
| Синее стекло |
5,8+0,6 |
6,0 |
| Зеленое стекло |
5,7+0,7 |
6,2 |
| Фарфор |
5,3+0,6 |
5,0 |
Отклонение между результатами составляет порядка 10-15%. Согласно литературным данным [ГН 2.3.3.972-00. Предельно допустимые количества химических веществ, выделяющихся из материалов, контактирующих с пищевыми продуктами] ПДК меди в растворах, контактирующих с указанной посудой, составляет 1 мг/л. Эта концентрация на порядок выше предела обнаружения по предлагаемой тест-методике. Это позволяет считать возможным полуколичественное тест-определение меди в подобных объектах с использованием заявляемой методики.
По сравнению с прототипом предлагаемый способ определения меди (II) уменьшает время анализа, снижает трудоемкость и стоимость анализа на различных объектах, расширяет интервал определяемых концентраций. Получаемый технический результат обеспечивают отличительные признаки заявляемого способа, т.е. предлагаемый способ обладает изобретательским уровнем, новизной и промышленной применимостью.
Формула изобретения
Способ определения меди (II), основанный на реакции между фосфорно-молибденовой кислотой (ФМК) и тиомочевиной, катализируемой медью (II), отличающийся тем, что реакцию проводят на твердом носителе, в качестве которого используют тест-полосу, приготовленную путем пропитки фильтровальной бумаги 2%-ным раствором ФМК, с последующим ее погружением в систему, содержащую анализируемый раствор, доведенный до рН 1-1,3, и 2-4 мл 2% тиомочевины, и по зависимости содержания меди от времени изменения цвета тест-полосы до голубого рассчитывают концентрацию меди.
РИСУНКИ
|
|