|
|
(21), (22) Заявка: 2005117588/15, 07.06.2005
(24) Дата начала отсчета срока действия патента:
07.06.2005
(46) Опубликовано: 10.08.2006
(56) Список документов, цитированных в отчете о
поиске:
Промышленные хлорорганические продукты. Под. ред. Ошина Л.А. – М.: Химия, 1978, с.190. ФРАНКЕ З. Химия отравляющих веществ. – М.: Химия, 1973, т.1. с.114-117. JP 63319205 A, 27.12.1988. US 5672747 A, 30.09.1997. СА 1159839 А, 03.01.1984.
Адрес для переписки:
429950, Чувашская Республика, г. Новочебоксарск, ул. Советская, 38, кв.89, А.Н.Савельеву
|
(72) Автор(ы):
Савельев Алексей Николаевич (RU),
Савельев Николай Иванович (RU),
Агафонов Борис Александрович (RU)
(73) Патентообладатель(и):
Савельев Алексей Николаевич (RU)
|
(54) СПОСОБ ПОЛУЧЕНИЯ ФОСГЕНА ИЗ ПЕРХЛОРЭТИЛЕНА
(57) Реферат:
Изобретение относится к химической промышленности и может использоваться в малотоннажных производствах высокомолекулярных материалов, биологически активных веществ, красителей, растворителей. На первой стадии парогазовую смесь из перхлорэтилена и кислорода, взятых в мольном соотношении 1:1,00-1,15, при температуре 500-1500°С подвергают окислительному пиролизу. На второй стадии из полученной газовой смеси, содержащей окись углерода и хлор, получают фосген. Результат изобретения: получение фосгена из перхлорэтилена и кислорода с высоким выходом. 1 ил., 1 табл.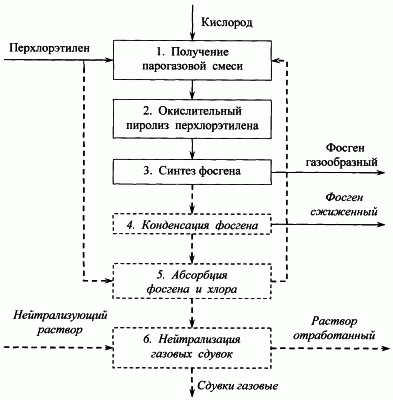
Изобретение относится к химической промышленности и может использоваться в малотоннажных производствах высокомолекулярных материалов, биологически активных веществ, красителей, растворителей.
В промышленности фосген получают из окиси углерода и хлора на активном угле при температуре 125-150°С [Франке З. Химия отравляющих веществ. М.: Химия, 1973, т.1. – С.114-117] по реакции:

Необходимую окись углерода выделяют из продуктов неполного окисления природного газа и других видов углеродсодержащего сырья, а хлор получают электролизом водного раствора хлористого натрия.
С целью совершенствования данного способа предложено:
– использовать катализатор с очень низким содержанием активного металла [заявка RU №98117445, МПК7 С 01 В 31/28, опубл. 07.20.2000];
– наносить на активированный уголь карбид кремния [патент RU №2178387, МПК7 С 01 В 31/28, опубл. 01.20.2002];
– проводить синтез при температуре 30-80°С [заявка RU №20011113719, МПК7 С 01 В 31/28, опубл. 06.20.2003].
Выделение из смеси газов неполного окисления углеродсодержащего сырья чистой окиси углерода представляет сложный технологический процесс, в связи с чем применение данного способа экономически обосновано только на установках большой мощности.
Возможно получение фосгена из четыреххлористого углерода [Промышленные хлорорганические продукты./ Под ред. Л.А.Ошина. – М.: Химия, 1978. – С.39-40] по реакциям, которые катализируются кислотами Льюиса:

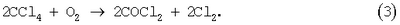
Данные реакции для промышленного производства фосгена не используются из-за низкого выхода по хлору.
Известны способы получения фосгена из четыреххлористого углерода и двуокиси углерода при температуре 350-550°С по реакции:

В качестве катализатора предложено использовать AlCl3, FeCl3 [патент RU №2042618, МПК6 С 01 В 31/28, опубл. 08.27.1995] или никель, сплавы никеля с хромом и их хлориды [патент RU №2042619, МПК6 С 01 В 31/28, опубл. 08.27.1995]. Фосген из реакционных газов выделяют методом абсорбции четыреххлористым углеродом и последующей десорбции.
Основным недостатком способов, основанных на обратимой реакции (4), является низкая степень конверсии четыреххлористого углерода, а также разложение фосгена на окись углерода и хлор по обратимой реакции (1) из-за высокой температуры.
Известен двухстадийный способ получения фосгена из метилового эфира муравьиной кислоты [Чичибабин А.Е. Основные начала органической химии. – М.: Химия, Госхимиздат, 1963. – С.834-835] по реакциям:
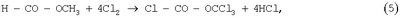

Известны способ и устройство для получения фосгена из дифосгена и/или трифосгена [заявка RU №2000109586/12, опубл. 07.10.2003].
В промышленности указанные способы не применяется из-за недостаточной селективности реакции (5).
Наиболее близким к предлагаемому изобретению является способ получения фосгена из перхлорэтилена [Промышленные хлорорганические продукты./ Под ред. Л.А.Ошина. – М.: Химия, 1978. – С.190] по параллельно протекающим реакциям:

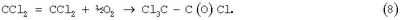
Недостатком данного способа является низкий выход фосгена.
Задачей изобретения является получение фосгена из перхлорэтилена и кислорода с высоким выходом.
Поставленная задача решается тем, что на первой стадии парогазовую смесь перхлорэтилена и кислорода, взятых в мольном соотношении 1:1,00-1,15, при температуре 500-1500°С подвергают окислительному пиролизу, а затем на второй стадии из полученной газовой смеси, содержащей окись углерода и хлор, известными способами получают фосген.
В качестве исходного сырья, содержащего перхлорэтилен, может использоваться смесь хлоруглеродов C1-С6, полученная из отходов производства хлорметанов, винилхлорида, хлорбензола и других хлоруглеводородов.
В качестве источника кислорода можно использовать осушенный воздух, обогащенный кислородом.
Заданное мольное соотношение кислород: перхлорэтилен  можно получать путем барботирования кислорода или кислородсодержащего газа через перхлорэтилен, нагретый до температуры, рассчитанной по уравнению можно получать путем барботирования кислорода или кислородсодержащего газа через перхлорэтилен, нагретый до температуры, рассчитанной по уравнению
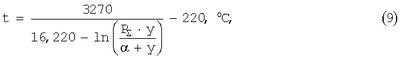
где Р – общее давление в узле дозирования реагентов, мм рт. ст.; – общее давление в узле дозирования реагентов, мм рт. ст.;
 – мольное соотношение кислород: перхлорэтилен, моль/моль; – мольное соотношение кислород: перхлорэтилен, моль/моль;
y – мольная доля кислорода в кислородсодержащем газе.
Уравнение (9) вытекает из закона Дальтона

где pnxэ, 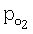 , Puн – парциальные давления паров перхлорэтилена, кислорода и инертных газов в исходной парогазовой смеси, которая направляется на процесс окислительного пиролиза. , Puн – парциальные давления паров перхлорэтилена, кислорода и инертных газов в исходной парогазовой смеси, которая направляется на процесс окислительного пиролиза.
Поскольку 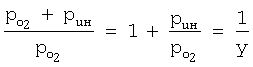 , , 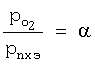 , из уравнения (10) вытекает соотношение , из уравнения (10) вытекает соотношение
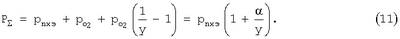
При использовании чистого перхлорэтилена парциальное давление его паров в парогазовой смеси равняется давлению насыщенных паров 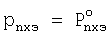 , которое может быть рассчитано по уравнению Антуана , которое может быть рассчитано по уравнению Антуана
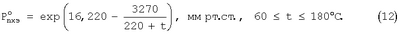
Совместное рассмотрение зависимостей (11) и (12) с учетом равенства 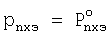 дает приведенное выше расчетное уравнение (9). дает приведенное выше расчетное уравнение (9).
Полученный фосген используют в газообразном виде или выделяют его в жидком виде методом конденсации с последующим улавливанием остатка фосгена и хлора из газовых сдувок исходным захоложенным перхлорэтиленом.
На чертеже представлена блок-схема производства фосгена из перхлорэтилена предлагаемым способом. При получении фосгена в газообразном виде используют блоки и потоки, изображенные сплошными линиями, а при получении сжиженного фосгена – дополнительно блоки и потоки, изображенные пунктирными линиями.
В таблице представлены результаты лабораторных опытов получения фосгена предлагаемым способом.
Схема производства фосгена, см.чертеж, включает:
– блок 1 получения однородной смеси кислорода и паров перхлорэтилена с заданным мольным соотношением,
– блок 2 проведения процесса окислительного пиролиза,
– блок 3 синтеза газообразного фосгена.
При получении сжиженного фосгена схема включает также:
– блок 4 конденсации фосгена,
– блок 5 абсорбции остатка фосгена и хлора исходным перхлорэтиленом,
– блок 6 нейтрализации газовых сдувок нейтрализующим агентом.
Экспериментальная проверка предлагаемого способа проведена на лабораторной установке производительностью по фосгену 99 г/час (1,0 моль/час).
Исходную парогазовую смесь получали в склянке Дрекселя с жидким перхлорэтиленом, нагретым до температуры 96-98°С, через которую со скоростью 0,5 моль/час (0,2 дм3/мин при 20°С) пропускали кислород.
Полученный парогазовый поток подавали в реактор окислительного пиролиза, который представлял собой кварцевую трубку, размещенную в трубчатой электрической печи с регулятором мощности. В нем парогазовую смесь нагревали и проводили процесс окислительного пиролиза.
Полученную смесь газов процесса окислительного пиролиза, содержащую хлор и окись углерода, направляли в трубчатый реактор с активным углем, в котором при температуре 50-150°С осуществляли процесс синтеза фосгена.
Реакционные газы охлаждали смесью льда и соли до температуры минус 15°С и отделяли сжиженный фосген и остатки хлорорганических соединений от газов.
Несконденсированные газы пропускали через три последовательно соединенные склянки Дрекселя: первая – сухая, вторая – с захоложенным перхлорэтиленом, третья – с водным раствором гидроокиси натрия. До начала опыта и после его завершения установку продували воздухом.
В опыте по условиям прототипа, а именно при совмещении процессов окисления и синтеза на одной стадии, в приемнике конденсата узла ожижения фосгена получена смесь фосгена и продуктов частичного окисления перхлорэтилена, из которой фосген отделен перегонкой. Максимальный выход фосгена в условиях прототипа составил 47%.
При синтезе фосгена предлагаемым способом выход фосгена на израсходованный перхлорэтилен составил 83-93%.
Выход 93% получен при мольном соотношении кислород: перхлорэтилен 1,05:1, температуре окисления 1020°С и температуре синтеза фосгена 100°С, опыт 1.
При мольном соотношении кислород: перхлорэтилен 1:1 наблюдалось неполное окисление перхлорэтилена даже при температуре в реакторе окисления 1450°С, опыт 2. При мольном соотношении кислород: перхлорэтилен 1,15:1 кислород частично окислял углерод до двуокиси, в результате чего в газах окисления создавался существенный избыток хлора, опыт 3.
Проведенные опыты показывают, что предлагаемым способом из перхлорэтилена фосген можно получить на компактной установке с высоким выходом.
Таблица.
Опытные данные процесса получения фосгена из перхлорэтилена |
| Наименование показателя |
Значение показателя в опыте |
| Прототип |
1 |
2 |
3 |
| 1 Температура склянки Дрекселя с жидким перхлорэтиленом, °С |
97,3 |
97,3 |
98,1 |
95,9 |
| 2 Состав исходной парогазовой смеси, мольная доля: |
|
|
|
|
| перхлорэтилен |
0,49 |
0,49 |
0,50 |
0,465 |
| кислород |
0,51 |
0,51 |
0,50 |
0,535 |
| 3 Мольное соотношение кислород: перхлорэтилен, моль/моль |
1,05 |
1,05 |
1,00 |
1,15 |
| 4 Температура в реакторе окисления, °С |
230 |
1020 |
1450 |
510 |
| 5 Состав газов после окислительного пиролиза, мольная доля: |
Совмещенный процесс окисления и синтеза |
|
|
|
| хлор |
0,50 |
0,49 |
0,50 |
| окись углерода |
0,47 |
0,46 |
0,42 |
| двуокись углерода |
0,03 |
0,03 |
0,08 |
| хлорорганические соединения в пересчете на перхлорэтилен |
менее 0,01 |
0,02 |
менее 0,01 |
| 6 Температура в реакторе синтеза фосгена, °С |
230 |
100 |
150 |
50 |
| 7 Выход фосгена, % |
47 |
93 |
89 |
83 |
Формула изобретения
Способ получения фосгена из перхлорэтилена, отличающийся тем, что на первой стадии смесь перхлорэтилена и кислорода, взятых в мольном соотношении 1:1,00-1,15, при температуре 500-1500°С подвергают окислительному пиролизу, а затем на второй стадии из полученной газовой смеси, содержащей окись углерода и хлор, получают фосген.
РИСУНКИ
|
|