|
|
(21), (22) Заявка: 2005120397/15, 30.06.2005
(24) Дата начала отсчета срока действия патента:
30.06.2005
(46) Опубликовано: 10.08.2006
(56) Список документов, цитированных в отчете о
поиске:
US 6344276 А, 05.02.2002. RU 2191842 С2, 27.10.2002. RU 2114580 C1, 10.07.1998. RU 2115388 C1, 20.07.1998.
Адрес для переписки:
119049, Москва, ГСП-1, Ленинский пр-т, 4, МИСиС, отдел защиты интеллектуальной собственности
|
(72) Автор(ы):
Левашов Евгений Александрович (RU),
Штанский Дмитрий Владимирович (RU),
Глушанкова Наталья Александровна (RU),
Решетов Игорь Владимирович (RU)
(73) Патентообладатель(и):
Левашов Евгений Александрович (RU),
Штанский Дмитрий Владимирович (RU),
Государственное образовательное учреждение высшего профессионального образования “Московский государственный институт стали и сплавов” (технологический университет) (RU)
|
(54) БИОСОВМЕСТИМЫЕ МНОГОКОМПОНЕНТНЫЕ НАНОСТРУКТУРНЫЕ ПОКРЫТИЯ ДЛЯ МЕДИЦИНЫ
(57) Реферат:
Изобретение относится к медицинской технике, а именно к биосовместимым износостойким наноструктурным тонкопленочным материалам, используемым в качестве покрытий при изготовлении имплантатов, работающих под нагрузкой: ортопедические и стоматологические протезы, зубные коронки, имплантаты, используемые в челюстно-лицевой хирургии, искусственные сочленения, фиксаторы и др. Эти материалы должны обладать высокой твердостью, усталостной прочностью, износо- и коррозионной стойкостью, биосовместимостью и отсутствием токсичности. В изобретении достигается технический результат, заключающийся в создании многокомпонентного наноструктурного покрытия (МНП), обладающего высокой твердостью, низким модулем упругости, высокой прочностью сцепления с подложкой, низким коэффициентом трения и скоростью износа, высокой стойкостью к упругой деформации разрушения и пластической деформации, низкой шероховатостью поверхности, отрицательным зарядом поверхности в физиологических средах (4,5<рН<9), биоактивной поверхностью, биосовместимостью и отсутствием токсичности. Указанный технический результат достигается следующим образом. Биосовместимые многокомпонентные наноструктурные покрытия для имплантатов, работающие под нагрузкой, выполнены на основе карбонитрида титана с введением дополнительных элементов, улучшающих механические и трибологические свойства покрытия, а также обеспечивающих его биоактивность, биосовместимость и нетоксичность. Суммарные концентрации основных и дополнительных элементов в покрытии имеют следующее соотношение: 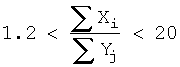
где Xi – суммарная концентрация основных элементов Ti, С, N в покрытии, Yj – суммарная концентрация дополнительных элементов Са, Zr, Si, К, Mn, О, Р в покрытии, при этом концентрацию элементов в покрытии выбирают при следующем соотношении компонентов, ат. %: Ti 30-50, С 15-40, N 0.5-30, О 5-25, Са 0-7, Zr 0-20, Si 0-30, Р 0-1.5, Mn 0-1.0, К 0-1.0. 1 табл.
Изобретение относится к медицинской технике, а именно к биосовместимым износостойким наноструктурным тонкопленочным материалам, используемым в качестве покрытий при изготовлении имплантатов, работающих под нагрузкой: ортопедические и стоматологические протезы, зубные коронки, имплантаты, используемые в челюстно-лицевой хирургии, искусственные сочленения, фиксаторы и др. Эти материалы должны обладать высокой твердостью, усталостной прочностью, износо- и коррозионной стойкостью, биосовместимостью и отсутствием токсичности.
Известно биосовместимое покрытие на имплантат из титана и его сплавов (RU 2154463, опублик. 20.08.2000), содержащее оксид титана, кальцийфосфатные соединения (пересчет на оксиды) при следующем соотношении компонентов, мас.%:
Оксид титана 52-74
Оксид кальция 6-12
Оксид фосфора 20-36
Однако биоактивная керамика не пригодна в качестве покрытий на поверхности имплантатов, работающих под нагрузкой, вследствие низкой трещиностойкости.
Известно биосовместимое покрытие на основе нитрида титана и карбида натрия (SU 1803096, опублик. 23.03.93) при следующем соотношении компонентов, мас.%:
Нитрид титана 20-50
Силицид титана 2-5
Гидрированный карбид натрия 25-30
Оксиды кремния остальное
Данное покрытие обладает повышенной прочностью сцепления пластмассы с металлической основой в ортопедической стоматологии, однако не обладает достаточно высокой износостойкостью, необходимой для долгого срока службы, и требуемыми остеоиндуктивными свойствами.
Прототипом заявленного изобретения является покрытие с аморфным слоем гидрооксиапатита и титана (патент US №6344276, опубл. 05.02.02).
Данное покрытие имеет повышенную прочность его соединения с субстратом и низкую скорость растворения материала покрытия, однако оно не обладает всем комплексом физических, механических, химических и биологических свойств, необходимых для материала имплантата, работающего под нагрузкой.
В изобретении достигается технический результат, заключающийся в создании многокомпонентного наноструктурного покрытия (МНП), обладающего высокой твердостью, низким модулем упругости, высокой прочностью сцепления с подложкой, низким коэффициентом трения и скоростью износа, высокой стойкостью к упругой деформации разрушения и пластической деформации, низкой шероховатостью поверхности, отрицательным зарядом поверхности в физиологических средах (4,5<рН<9), биоактивной поверхностью, биосовместимостью и отсутствием токсичности.
Указанный технический результат достигается следующим образом.
Биосовместимые многокомпонентные наноструктурные покрытия для имплантатов, работающие под нагрузкой, выполнены на основе карбонитрида титана с введением дополнительных элементов, улучшающих механические и трибологические свойства покрытия, а также обеспечивающих его биоактивность, биосовместимость и нетоксичность. Суммарные концентрации основных и дополнительных элементов в покрытии имеют следующее соотношение:
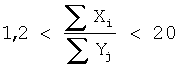
где Xi – суммарная концентрация основных элементов Ti, C, N в покрытии,
Yj – суммарная концентрация дополнительных элементов Са, Zr, Si, К, Mn, О, Р в покрытии.
При этом концентрацию элементов в покрытии выбирают при следующем соотношении компонентов, ат. %:
Ti 30-50
С 15-40
N 0.5-30
О 5-25
Са 0-7
Zr 0-20
Si 0-30
Р 0-1.5
Mn 0-1.0
К 0-1.0
Необходимое сочетание физических, механических, химических, трибологических и биологических свойств биосовместимых МНП достигается за счет включения в состав покрытий компонентов в количественных соотношениях, указанных выше.
Карбонитрид титана обладает высокой твердостью, износо- и коррозионной стойкостью.
Осаждение покрытий в среде аргона приводит к формированию грубой столбчатой структуры с повышенной пористостью. Содержание в составе покрытия азота приводит к измельчению и уплотнению структуры, а в отдельных случаях и к полному подавлению колонной структуры. Размер кристаллитов, как правило, не превышает 20 нм. Шероховатость пленок снижается при введении азота в состав покрытия.
Оптимальным является отношение металлических (Me) к неметаллическим элементам (NMe) Me/NMe=1.0-1.7, при котором покрытия имели кубическую структуру типа NaCl.
Образование слоя апатита связывается с формированием гидроксил функциональных групп на отрицательно заряженной поверхности биоактивной керамики во внутренней среде организма. Для этого в покрытие вводятся такие элементы, как Са, Р и О в заявляемом количестве. Наличие ионов кальция стимулирует рост клеток на поверхности имплантата. Увеличение содержания Са, Р и О свыше заявляемого количества приводит к снижению механических и трибологических свойств покрытий, а также к разрушению актинового цитоскелета клеток и ухудшению адгезионных свойств поверхности (таблица).
Во всем исследованном диапазоне значений рН (4,5<рН<9) поверхность МНП имеет отрицательный заряд. Покрытия с азотом, как правило, имеют более отрицательный заряд поверхности. Это означает, что поверхность покрытий может притягивать положительно заряженные ионы Са2+, которые находятся во внутренней среде организма, что способствует образованию сначала промежуточных, кальцийсодержащих фаз, а затем слоя гидроксиапатита, который является устойчивой фазой в физиологической среде.
Введение в покрытия элементов Са, Zr и О приводит к существенному снижению коэффициента трения до 0.17-0.25 по сравнению с покрытиями на основе карбида (0.85) или нитрида (0.55) титана.
Прикрепление клеток к поверхности имплантата определяется образованием интегрин-опосредованных фокальных контактов клеток с подлежащей поверхностью. Добавка Mn в количестве <1 ат.% приводит к активации интегринов и улучшению адгезии клеток. Дальнейшее увеличение содержания Mn приводит к снижению механических свойств покрытий и уменьшению распластывания и размножения клеток. Кремний способствует увеличению активности остеобластов и образованию слоя апатита. При его содержании менее 30 ат.% покрытия обладают однофазной гранецентрированной кубической структурой типа NaCl, что благоприятно сказывается на механических и трибологических свойствах.
Композиционные мишени и электроды могут быть получены методом самораспространяющегося высокотемпературного синтеза (СВС). В отличие от других известных методов получения композиционных катодов из тугоплавких соединений (прессование-спекание, газостатическое прессование, газотермическое напыление и др.) технология СВС имеет следующие преимущества: самоочистка продуктов горения от вредных растворимых и адсорбированных примесей в результате достижения высоких значений температуры (2500-3000°С) и скорости горения (2-10 см/с), развиваемых в волне горения СВС-систем; достижение высоких значений относительной плотности (97-99%) керамических материалов и тугоплавких соединений при сравнительно низких давлениях прессования; получение метастабильных состояний – пересыщенных твердых растворов; получение функциональных градиентных материалов (Левашов Е.А., Рогачев А.С., Юхвид В.И., Боровинская И.П. Физико-химические и технологические основы самораспространяющегося высокотемпературного синтеза, М., БИНОМ, 1999, 174 с).
При этом неорганические добавки, например гидроксилапатит (Са10(PO4)6(ОН)2), CaO, ZrO2, KMnO4 и TiO2 и др., могут вводиться на этапе получения композиционных катодов-мишеней для ионно-плазменного и/или ионно-лучевого распыления и электродов для электроискрового осаждения.
Основным технологическим преимуществом биосовместимых МНП является наличие целого комплекса свойств, необходимых для материалов-имплантатов, работающих под нагрузкой:
– высокая твердость Н=15-35 ГПа;
– низкий модуль упругости Е=150-300 ГПа;
– высокая адгезия покрытия к подложке, измеряемая величиной критической нагрузки Lc -не ниже 35 Н
– низкий коэффициент трения  =0.1-0.25; =0.1-0.25;
– низкая скорость износа Vw – менее 5·10-6 мм3/Нм;
– высокая стойкость к упругой деформации разрушения и пластической деформации 0.13/E2<0.9 ГПа;
– отрицательный заряд поверхности в физиологических средах;
– отсутствие разрушения актинового цитоскелета клеток при наличии биоактивности поверхности, биосовместимости и отсутствии токсичности.
Отклонение хотя бы по одному из приведенных выше свойств покрытий влечет за собой ухудшение служебных характеристик всего изделия (имплантата) в целом.
Низкий модуль упругости покрытий благоприятен с точки зрения уменьшения напряжений между покрытием и имплантатом, в качестве которого часто используется нержавеющая сталь Е=190-200 ГПа или титан Е=116 ГПа. Низкий модуль Юнга также приводит к лучшему переносу костью функциональных нагрузок и стимулирует нарастание костной ткани. Комбинация высокой твердости и упругого восстановления характеризует МНП как новый уникальный твердый и в то же время упругий материал, что является важнейшим фактором для материалов медицинского назначения, работающих под нагрузкой.
Изобретение осуществляют следующим образом.
Пример 1.
Технологический цикл получения биосовместимого МНП Ti-Zr-C-O-N состоит из двух основных стадий: получение композиционной мишени TiC0.5+ZrO2, например, методом самораспространяющегося высокотемпературного синтеза (СВС) и ее последующее магнетронное распыление на подложку.
Осаждение покрытия Ti-Zr-C-O-N осуществляли в газовой среде Ar+N2. Получено покрытие следующего состава, ат.%:
С 18.0
O 7.9
N 27.6
Ti 44.5
Zr 2.0
Для измерения физико-механических и трибологических свойств МНП осаждались на подложки из титанового сплава марки ВТ 1-0, никелевого сплава Целит-Н, кобальтового сплава Целит-К, а также никелида титана.
Физико-механические и трибологические свойства МНП определялись при использовании следующих высокопрецизионных приборов: Нанотвердомер (Nano-Hardness Tester, CSM Instruments, Швейцария); Скратч-тестер (Revetest, CSM Instruments, Швейцария); Машина трения (Tribometer, CSM Instruments, Швейцария); Сканирующий силовой микроскоп, оборудованный модулем для измерения твердости материалов по методу склерометрии с помощью игл из ультратвердого фуллерита С60 (NanoScan, Россия); Оптический микроскоп AXIOVERT, оборудованный цифровой камерой и системой анализа изображения (Карл Цейс, Германия). Твердость и модуль упругости определялись по методу Оливера и Фара [G.M.Pharr, W.C.Oliver, F.R.Brotzen. J. Mater. Res. 3, 613 (1992)] с использованием индентора Берковича. Величину упругого восстановления (We) покрытий рассчитывали по кривым нагружение-разгрузка по формуле We=(hmax-hr)/hmax, где hmax – максимальная глубина проникновения индентора, a hr – остаточная глубина после снятия нагрузки. Коэффициент трения и скорость износа покрытий измерялись с помощью машины трения по схеме “шарик-диск” при нагрузке 1 N и линейной скорости 10 см/с. Испытания проводились в физиологическом растворе (100 мл H2O + 0.9 г NaCl). В качестве контртела использовался неподвижный шарик из спеченного Al2О3 диаметром 3 мм.
Полученное покрытие имело твердость 37 ГПа, модуль упругости 270 ГПа, упругое восстановление 70%, коэффициент трения 0.16 и скорость износа 10-6 мм3/Нм.
Разрушения актинового цитоскелета клеток не обнаружено. Крысиные фибробласты Rat-1 и эпителиоциты IAR-2 рассеивали на поверхность пленок, осажденных на стекла. Клетки инкубировали 24, 48 и 72 часа при температуре 37°С. Стекла фиксировали в 3.7% параформальдегиде на фосфатном буфере в течение 10 мин, после чего окрашивали гематоксилином и заключали в смесь глицерина с фосфатным буфером. С помощью световой микроскопии подсчитывали количество клеток в поле зрения. Клетки распластывались и размножались одинаково хорошо как на контрольных стеклах, так и на тестируемых покрытиях, что свидетельствует о том, что покрытия адгезионны и нетоксичны для клеток.
Эксперименты in-vivo проводились на мышах. Образцы из тефлона с осажденными на них покрытиями вводились под кожу мышей. Через 16 недель имплантат с образовавшейся вокруг него капсулой извлекали и исследовали на биосовместимость. Результаты исследований показали отсутствие воспалительной реакции внутри капсулы, а клетки тканей плотно прилегали к поверхности покрытий.
Пример 2.
Осаждение МНП осуществляли путем магнетронного распыления композиционной СВС мишени TiC0.5+CaO в атмосфере аргона. Композиционная мишень содержала азот в количестве 3,3 ат.% вследствие активного взаимодействия титана с азотом при осуществлении химической реакции в режиме горения на воздухе. Получено покрытие следующего состава, ат.%:
С 30.2
O 22.9
N 3.3
Ti 38.2
Ca 5.4
Полученное покрытие имело твердость 31 ГПа, модуль упругости 220 ГПа, упругое восстановление 70% и коэффициент трения 0.17.
Разрушения актинового цитоскелета клеток не обнаружено. Исследования in-vitro и in-vivo показали, что покрытие Ti-Ca-C-O-N является биосовместимым, нетоксичным, не вызывает воспалительной реакции при его имплантации под кожу мышей. Клетки фибробластов и эпителиоцитов хорошо размножались и обладали высокой адгезией к поверхности покрытия.
Примеры 3-16.
Для оптимизации состава МНП были проведены многочисленные эксперименты по получению катодов-мишеней различных составов и осаждению покрытий по технологии магнетронного распыления. В таблице в обобщенном виде представлены результаты исследований и свойства МНП, подтверждающие правомерность заявляемых составов МНП.
МНП обладают одним или несколькими конкурентными преимуществами, необходимыми для материалов имплантатов, работающих под нагрузкой: высокой твердостью; низким модулем упругости; высокой адгезией; низким коэффициентом трения и скоростью износа; высокой стойкостью к упругой деформации разрушения и пластической деформации; низкой шероховатостью поверхности; отрицательным зарядом поверхности в физиологических средах (4,5<рН<9); биоактивной поверхностью; биосовместимостью и отсутствием токсичности.
| Элементный состав и свойства покрытий |
| № |
Элементный состав |
Н, ГПа |
Е, ГПа |
Lс, Н |
We, % |
 |
Vw 10-6 мм3/Нм |
Разрушение актинового цитоскелета клеток |
| Ti |
С |
N |
О |
Са |
Zr |
Si |
Mn |
К |
Р |
| Оптимальные покрытия, соответствующие заявляемому составу |
| 1 |
38.2 |
30.2 |
3.3 |
22.9 |
5.4 |
– |
– |
– |
– |
– |
31 |
220 |
40 |
70 |
0.17 |
1.0 |
– |
| 2 |
32.5 |
25.6 |
17.0 |
19.3 |
5.6 |
– |
– |
– |
– |
– |
16 |
160 |
42 |
53 |
0.21 |
1.2 |
– |
| 3 |
47.1 |
33.7 |
3.0 |
14.0 |
– |
2.2 |
– |
– |
– |
– |
28 |
270 |
50 |
58 |
0.16 |
1.0 |
– |
| 4 |
44.5 |
18.0 |
27.6 |
7.9 |
– |
2.0 |
– |
– |
– |
– |
37 |
270 |
46 |
70 |
0.16 |
0.9 |
– |
| 5 |
41.8 |
16.5 |
26.6 |
12.6 |
1.8 |
– |
– |
– |
– |
0.7 |
27 |
240 |
40 |
66 |
0.21 |
4.0 |
– |
| 6 |
47.0 |
22.0 |
23.2 |
7.0 |
0.6 |
– |
– |
– |
– |
0.2 |
22 |
230 |
44 |
61 |
0.24 |
4.8 |
– |
| 7 |
43.7 |
36.6 |
– |
15.2 |
3.7 |
– |
– |
0.6 |
0.2 |
– |
16 |
180 |
38 |
57 |
0.2 |
4.2 |
– |
| 8 |
38.1 |
22.8 |
22.8 |
12.8 |
3.0 |
|
|
0.4 |
0.1 |
|
15 |
160 |
39 |
56 |
0.2 |
3.8 |
– |
| 9 |
34.1 |
– |
22.8 |
16.0 |
– |
2.1 |
25.0 |
– |
– |
– |
26 |
250 |
45 |
60 |
0.4 |
4.0 |
– |
| Неоптимальные составы, за пределами заявляемых диапазонов |
| 10 |
53.0 |
12.0 |
35.0 |
– |
– |
– |
– |
– |
– |
– |
22 |
450 |
32 |
55 |
0.55 |
5.2 |
+ |
| 11 |
55.0 |
13.2 |
19.5 |
2.5 |
8.8 |
– |
– |
– |
– |
– |
11 |
120 |
40 |
45 |
0.5 |
6.7 |
+ |
| 12 |
36.0 |
9.3 |
23.0 |
8.0 |
– |
23.7 |
– |
– |
– |
– |
13 |
140 |
37 |
51 |
0.42 |
5.8 |
– |
| 13 |
44.2 |
13.1 |
23.2 |
10.1 |
7.6 |
– |
– |
– |
– |
1.8 |
8 |
115 |
30 |
48 |
0.38 |
7.4 |
+ |
| 14 |
41.7 |
17.4 |
31.6 |
3.2 |
3.5 |
– |
– |
1.4 |
1.2 |
– |
11 |
120 |
25 |
49 |
0.45 |
6.2 |
+ |
| 15 |
51.5 |
– |
4.1 |
7.2 |
– |
4.8 |
32.4 |
– |
– |
– |
6 |
80 |
32 |
45 |
0.5 |
7.0 |
+ |
| 16 |
33.2 |
12.1 |
20.8 |
28.5 |
5.4 |
– |
– |
– |
– |
– |
10.5 |
130 |
20 |
49 |
0.35 |
5.6 |
+ |
Н – твердость, Е – модуль упругости, Lc – критическая нагрузка. We – упругое восстановление,  – коэффициент трения, Vw – скорость износа. – коэффициент трения, Vw – скорость износа. |
Формула изобретения
Биосовместимые многокомпонентные наноструктурные покрытия для имплантатов, работающих под нагрузкой, на основе карбонитрида титана с введением дополнительных элементов, улучшающих механические и трибологические свойства покрытия, а также обеспечивающих его биоактивность, биосовместимость и нетоксичность, при следующем соотношении суммарных концентраций основных и дополнительных элементов:
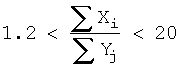
где Xi – суммарная концентрация основных элементов Ti, С, N в покрытии;
Yj – суммарная концентрация дополнительных элементов Са, Zr, Si, К, Mn, О, Р в покрытии,
при этом концентрацию элементов в покрытии выбирают при следующем соотношении компонентов, ат.%:
| Ti |
30-50 |
| С |
15-40 |
| N |
0,5-30 |
| О |
5-25 |
| Са |
0-7 |
| Zr |
0-20 |
| Si |
0-30 |
| Р |
0-1,5 |
| Mn |
0-1,0 |
| К |
0-1,0 |
|
|