|
|
(21), (22) Заявка: 2004138243/15, 27.12.2004
(24) Дата начала отсчета срока действия патента:
27.12.2004
(46) Опубликовано: 27.07.2006
(56) Список документов, цитированных в отчете о
поиске:
БЕРГЕЛЬСОН Л.Д. Препаративная биохимия липидов. – М.: Наука, 1981, с.256. RU 2166332 С2, 10.05.2001. В. Xiao X.F. Sun Run Cang Sun. Extraction and characterization of lipophilic extractives from rice straw, i. Chemical composition. Journal of Wood Chemistry and Technology, 2001, v.21, №4, p.397-411.
Адрес для переписки:
690022, г.Владивосток, пр-кт 100-летия Владивостока, 159, Институт химии ДВО РАН, отдел интеллектуальной собственности, Н.С. Василюк
|
(72) Автор(ы):
Земнухова Людмила Алексеевна (RU),
Исай Светлана Викторовна (RU)
(73) Патентообладатель(и):
Институт химии Дальневосточного отделения Российской академии наук (статус государственного учреждения) (Институт химии ДВО РАН) (RU),
Бурмистров Александр Сергеевич (RU),
Тен Петр Владимирович (RU)
|
(54) СПОСОБ ВЫДЕЛЕНИЯ МОНОГАЛАКТОЗИЛДИАЦИЛГЛИЦЕРИНОВ ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ
(57) Реферат:
Изобретение относится к биохимии. Проводят экстракцию общих липидов из отходов переработки зерна риса. Разделение липидов осуществляют с использованием метода двумерной тонкослойной хроматографии с использованием смеси растворителей: по первому направлению – хлороформ, ацетон, метанол, муравьиная кислота, вода; по второму направлению – ацетон, бензол, муравьиная кислота, вода. Изобретение позволяет повысить чистоту продукта. 2 табл., 2 ил.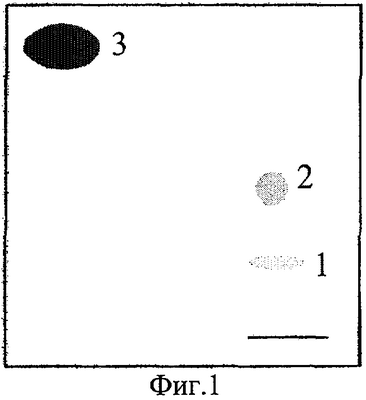
Изобретение относится к биохимии, конкретно к области получения гликолипидов, которые могут быть использованы в фармацевтической и косметологической промышленности, а также в качестве промежуточных соединений для синтеза новых материалов в биохимии, медицине, в том числе в иммунологии, и в других отраслях промышленности.
Было показано, что гликолипиды, в основном в виде глицерогликолипидов: моногалактозилдиацилглицеринов и дигалактозилдиацилглицеринов, присутствуют во всех растениях, но их количество и соотношение между ними в каждом растении индивидуально.
Определенный набор липидов выделяют из хвойных растений, однако содержание гликолипидов в них незначительно (патент РФ №2089208, опубл. 10.09.1997; Кислухина О.В. Выделение биологически активных липидов из низко-масличного сырья. Пищ. и перераб. Пром-сть: Сер. Масло-жировая пром-сть: Научно-технический инфор. Сб. 1995 Вып.1. – С.10-17). Как правило, они представляют собой набор неполярных и кислых липидов, получаемых путем обработки измельченного сырья 5-10% водным раствором щелочи при комнатной температуре и последующего их извлечения из полученной эмульсии экстракцией петролейным и диэтиловым эфирами.
Большой набор гликолипидов (ГЛ), включающий галактозилглицерины (ТТЛ) – ацил-моногалактозилдиацилглицерины (Ас-МГДГ), моногалактозилдиацилглицерины (МГДГ), а также сфинголипиды (СФЛ), цереброзиды (ЦЗ) и керамидолигогексозиды (КОГ) – содержит экстракт липидной фракции семян аконита северного. Идентификацию этих соединений проводили по данным ИК-спектроскопии, химических превращений и хроматографической подвижности (С.Г.Юнусова, Э.Г.Зинурова, М.С.Юнусов. Гликолипиды семян аконита северного. Всероссийская конференция «Химия и технология растительных веществ», Сыктывкар, 25-30 сентября 2000 г, 48 с.).
Однако разделение полученной смеси ГЛ с выделением отдельных фракций, в том числе фракции моногалактозилдиацилглицеринов (МГДГ), из этой смеси известными методами колоночной хроматографии и препаративной хроматографии на силикагеле является чрезвычайно трудоемким и неэффективным процессом, в том числе и из-за используемого сырьевого источника, запасы которого незначительны.
На сегодняшний день актуальной задачей является не только поиск нетрадиционных источников липидов, но и получение липидов определенного состава, тем более, что растительные ГЛ и их отдельные фракции являются остродефицитной продукцией, а их выделение связано с переработкой значительного количества растительного сырья, в частности пищевого зерна, и большими капиталовложениями.
О возросших потребностях в липидных препаратах говорит и появление ряда фирм, которые стали выпускать разные вещества этого класса, в том числе МГДГ (Galactosyi diglyceride), структурной формулой
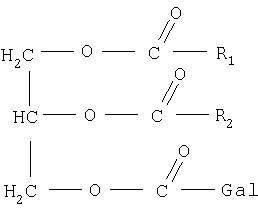
где R1 и R2 – ацильные остатки. Gal – галактоза.
Стоимость реактива “Galactosyl diglycerid “с содержанием основного вещества примерно 95%, получаемого из непросеянной пшеничной муки, высушенного в вакууме, составляет (долл. США): 1 мг – 12.10; 5 мг – 39.30 и 10 мг – 65.00. (SIGMA (Chemical company): Biochemicals organic compounds for research and diagnostic reagents. 1992. P.454).
Основным источником выделения МГДГ на сегодня остается пшеничная мука, содержащая смесь гликолипидов, главным образом моногалактозилдиацилглицеринов – МГДГ и дигалактозилдиацилглицеринов – ДГДГ. Способ выделения фракции МГДГ из нее является наиболее близким к заявляемому. Способ состоит из нескольких стадий, включающих экстракцию и переэкстракцию общих липидов (ОЛ) с применением в качестве экстрагентов метанола и гексана, затем выделение из полученного экстракта смеси неочищенных ГЛ с последовательным использованием эфира и системы растворителей (бензол – ацетон и метанол) для очистки полученной фракции ГЛ, последующее разделение МГДГ и ДГДГ с помощью одномерной тонкослойной хроматографии (ТСХ) в системе хлороформ – уксусная кислота – вода и на заключительном этапе – выделение МГДГ экстракцией соответствующей зоны метанолом (Препаративная биохимия липидов. Под ред. Л.Д.Бергельсона. М.: Наука, 1981. 256 с.).
Однако известный способ выделения моногалактозилдиацилглицеринов основан, во-первых, на использовании сырья, представляющего собой ценный пищевой продукт и, во-вторых, содержащего как минимум смесь двух ГЛ, что приводит к необходимости использования больших объемов растворителей и делает известный способ многостадийным, а использование одномерной ТСХ не позволяет разделить с достаточной полнотой близкородственные по структуре гликолипиды.
Задача изобретения состоит в упрощении способа выделения фракции МГДГ из растительного сырья и повышении ее чистоты, что достигается за счет использования нового источника растительного происхождения.
Поставленная задача решается тем, что в способе выделения моногалактозилдиацилглицеринов из растительного сырья путем экстракции общих липидов, последующего их разделения и выделения целевого продукта, в качестве исходного сырья используют отходы переработки риса, а разделение липидов осуществляют с использованием двумерной тонкослойной хроматографии (ТСХ).
Отходы переработки риса (РО) представляют собой возобновляемую биомассу, образующуюся в качестве отхода при очистке зерна на крупяных заводах и состоящую из рисовой шелухи, мучки или рисовых отрубей. Как правило, непереработанный отход риса используют как упаковочный материал, термо- и звукоизолирующий наполнитель в пластмассах, в производстве стройматериалов, в качестве адсорбента маслоподобных веществ, абразивов, топлива, в сельском хозяйстве в качестве добавки в корм животным, подстилочного материала, разрыхлителя почв. Подвергнутый физико-химической переработке отход используют для получения неорганических соединений кремния, углерода, а также ксилозы, сахарозы, фруктозы, фурфурола и фитиновых кислот.
Проведенные заявителем исследования состава липидных фракций из различных растительных отходов показали, что в отличие от известных растительных источников липидов, в том числе и пшеничной муки, липидная фракция отходов переработки риса содержит один доминирующий гликолипид – моногалактозилдиацилглицерин. Впервые обнаруженное заявителем данное свойство рисового отхода позволило значительно упростить процесс выделения МГДГ за счет сокращения количества технологических операций, повысить чистоту выделяемого продукта и дополнительно значительно удешевить стоимость способа.
Способ осуществляют следующим образом.
В качестве отхода рисового производства используют отходы переработки зерна риса (РО), которые образуются при получении крупы на заводах. В частности, были исследованы образцы РО, полученные на крупяных заводах в Краснодарском крае (образцы РО1-3) и Ростовской области (образец РО-4). Для сравнения липидного состава использовали также образец зерна сои, выращенной в Амурской обл.
Двумерную ТСХ проводили по общепринятым методикам с использованием смеси известных растворителей, взятых в определенном соотношении, которая показала наилучший результат: 1-е направление: хлороформ, ацетон, метанол, муравьиная кислота, вода; 2-е направление: ацетон, бензол, муравьиная кислота, вода (М.Кейтс. – Техника липидологии. М.: Мир, 1975. 221 с.).
Качественный состав ОЛ различных образцов РО определяли по известной методике с помощью одномерной ТСХ с использованием одного из реагентов, проявляющих пятна (например, раствора серной кислоты в метаноле или раствора фосфорномолибденовой кислоты), а их идентификацию проводили по литературным значениям величин Rf (М.Кейтс. – Техника липидологии. М.: Мир, 1975. 221 с.; W.W. Christie. – Lipid analysis. Isolation, separation, identification and structural analysis of lipids – L., 1973. – P.153-154). Результаты представлены в табл. 1, где приведен состав полярных липидов в образцах РО и для сравнения – сои.

Анализ полярных липидов, полученных по заявляемому способу из отходов рисового производства, проведенный с помощью двумерной ТСХ, представлен в табл.2 и на фиг.1, где приведена двумерная микро-ТСХ полярных липидов образца РО-1: 1-ФИ; 2-ФХ; 3-МГДГ. Для остальных образцов микро-ТСХ идентичны. Для сравнения на фиг.2 приведена двумерная микро-ТСХ полярных липидов образца сои, где 1-ФИ, 2-ФХ, 3-МГДГ, 4-ФС, 5-ФЭ, 6-СХДГ: 7-ДГТС, 8-Х1, 9-X2, где X1 и Х2 – неидентифицированные соединения.
| Таблица 2 |
| Образец сырья |
Выход ОЛ, % (относ, исх. сырья) |
Выход, % (относительно ОЛ) |
| МГДГ |
ФЛ |
| РО-1 |
1,44 |
0,60 |
0,12 |
| РО-2 |
2,65 |
1,10 |
0,22 |
| РО-3 |
2,64 |
1,60 |
0,32 |
| РО-4 |
1,54 |
1,10 |
0,22 |
| СОЯ |
2,43 |
6,00 |
1,20 |
Полученные данные показывают, что во всех образцах РО идентифицированы по одному ГЛ, представляющему собой МГДГ, и по два фосфолипида (ФЛ): ФИ, ФХ. По составу полярных липидов (ПЛ) образцы РО существенно отличаются от образца сои, который демонстрирует наличие большего числа полярных липидов.
Известно, что длина цепи ацильных групп и их степень ненасыщенности влияют на хроматографическую подвижность ГЛ (С.В.Хотимченко. Липиды морских водорослей-макрофитов и трав: Структура, распределение, анализ. Владивосток: Дальнаука, 2003, 234 с.). Поскольку при хроматографическом разделении ГЛ и ФЛ методом ТСХ не наблюдается деления МГДГ на две зоны, т.е. МГДГ образует одно пятно (пятно 3 на фиг.1), можно считать, что ацильные остатки моногалактозилдиацилглицерина R1 и R2 одинаковы, и следовательно, выделяемый МГДГ является гомогенным соединением, в котором R1 равно R2.
Предложенный способ иллюстрируется следующим примером.
Навеску 20 г сырья – РО-2 – заливают 200 мл смеси хлороформ-этанол (2:1) и экстрагируют ОЛ. Полученный экстракт упаривают на роторном испарителе при температуре 40°С, высушивают под вакуумом до постоянной массы и получают 0.52 г ОЛ, которые затем растворяют в 5 мл гексана и проводят двумерную ТСХ на хроматографической пластине в следующей системе растворителей: 1-е направление: хлороформ, ацетон, метанол, муравьиная кислота, вода; 2-е направление: ацетон, бензол, муравьиная кислота, вода. Для количественного выделения МГДГ хроматограмму опрыскивают дистиллированной водой, проявляющей пятна; отмечают нужное пятно, соскребают его с хроматографической пластины вместе с адсорбентом и помещают в сосуд. Затем проводят десорбцию (элюирование), обрабатывая вещество с адсорбентом этанолом. Раствор отфильтровывают от адсорбента центрифугированием и проводят вакуумное испарение растворителя. Выход МГДГ составляет 0.0057 г или 1,1 мас.% от массы общих липидов.
Формула изобретения
Способ выделения моногалактозилдиацилглицеринов из растительного сырья путем экстракции общих липидов, разделения и последующего выделения из них целевого продукта, отличающийся тем, что в качестве исходного сырья используют отходы переработки зерна риса, а разделение осуществляют с использованием метода двумерной тонкослойной хроматографии с использованием смеси растворителей: по первому направлению – хлороформ, ацетон, метанол, муравьиная кислота, вода; по второму направлению – ацетон, муравьиная кислота, вода.
РИСУНКИ
|
|