|
|
(21), (22) Заявка: 2004127573/04, 04.02.2003
(24) Дата начала отсчета срока действия патента:
04.02.2003
(30) Конвенционный приоритет:
11.02.2002 ES 200200328
(45) Опубликовано: 10.05.2006
(56) Список документов, цитированных в отчете о
поиске:
ЕР 748806 А1, 18.12.1996. ЕР 151477 А2, 14.08.1985. SU 622405, 10.06.1978.
(85) Дата перевода заявки PCT на национальную фазу:
13.09.2004
(86) Заявка PCT:
EP 03/01089 (04.02.2003)
(87) Публикация PCT:
WO 03/068770 (21.08.2003)
Адрес для переписки:
127055, Москва, а/я 11, пат.пов. Н.К.Попеленскому
|
(72) Автор(ы):
АНГЛАДА Луис (ES),
ГУГЛЬЕТТА Антонио (ES),
ПАЛАСИН Селия (ES),
РАМЕНТОЛЬ Хорхе (ES),
ФОГЕТ Рафаэль (ES)
(73) Патентообладатель(и):
Феррер Интернасионал, С.А. (ES)
|
(54) R-(-)-1-[2-(7-ХЛОРБЕНЗО[b]ТИОФЕН-3-ИЛМЕТОКСИ)-2-(2,4-ДИХЛОРФЕНИЛ)ЭТИЛ]-1H-ИМИДАЗОЛ И ЕГО СОЛИ, СПОСОБ ИХ ПОЛУЧЕНИЯ, КОМПОЗИЦИЯ, ОБЛАДАЮЩАЯ ПРОТИВОГРИБКОВЫМ ДЕЙСТВИЕМ
(57) Реферат:
Описывается R-(-)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазол формулы (I) и его соли, в частности его мононитрат, 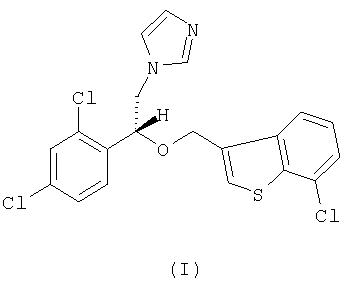 способ получения соединения формулы (I), композиция, обладающая противогрибковым действием, на основе соединения формулы (I) и применение соединения формулы (I) в качестве активного ингредиента противогрибковой композиции. Технический результат – соединение формулы (I) можно использовать в композициях для лечения грибковых инфекций у человека или животных и для борьбы с болезнями сельскохозяйственных культур. 5 н. и 10 з.п. ф-лы, 1 табл. способ получения соединения формулы (I), композиция, обладающая противогрибковым действием, на основе соединения формулы (I) и применение соединения формулы (I) в качестве активного ингредиента противогрибковой композиции. Технический результат – соединение формулы (I) можно использовать в композициях для лечения грибковых инфекций у человека или животных и для борьбы с болезнями сельскохозяйственных культур. 5 н. и 10 з.п. ф-лы, 1 табл.
Область техники, к которой относится изобретение
Настоящее изобретение относится к R-(-)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазолу(R-(-)-сертаконазолу) и его солям, способу его получения, к композициям, которые содержат упомянутое соединение, и к применению указанных композиций для лечения грибковых инфекций и борьбы с болезнями сельскохозяйственных культур.
Уровень техники
Рацемический 1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазол является известным соединением с названием сертаконазол (WHO, INN), которое используют в качестве противогрибкового агента для лечения заболеваний, вызванных грибами и дрожжами у человека и животных. Получение указанного соединения и его мононитрата описано в европейском патенте No 151477.
Раскрытие изобретения
Настоящее изобретение относится к R-(-)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазолу формулы I
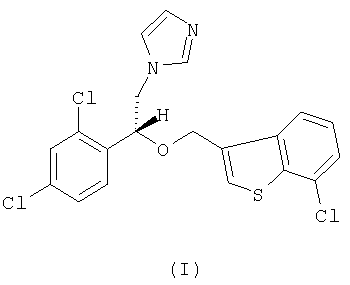
а также к его фармацевтически приемлемым аддитивным солям.
R-(-)-энантиомер сертаконазола обладает активностью в отношении грибов и дрожжей, которая приблизительно в 2 раза выше по сравнению с рацемической смесью, (так как его сродство к мишени в 2 раза выше), как показано в таблице 1. Эти данные позволяют предположить, что введение R-(-)-сертаконазола в дозе, составляющей 1/2 дозы рацемического сертаконазола, таким образом позволит снизить риск побочных действий и обеспечит подавление неспецифической токсичности, связанной с нежелательной примесью S-(+)-энантиомера.
Мононитрат является предпочтительной солью R-(-)-сертаконазола.
Настоящее изобретение относится также к способу получения R-(-)-энантиомера сертаконазола и его фармацевтически приемлемых солей, причем способ включает взаимодействие R-(-)-1-(2,4-дихлорфенил)-2-имидазол-1-илэтанола формулы ((R)-(-)-III)
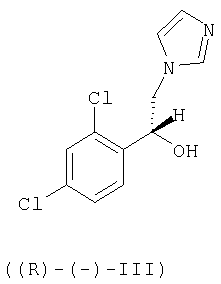
с 3-галогенметил-7-хлорбензо[b]тиофеном формулы IV
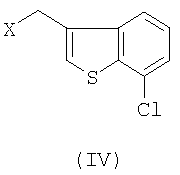
где Х означает галоген.
Соединение можно выделить из реакционной смеси известными в данной области способами. При необходимости неочищенный продукт можно затем очистить известными в данной области способами, например кристаллизацией и/или хроматографией.
Получение S-(+)-энантиомера сертаконазола можно проводить соответствующим способом с использованием S-(+)-1-(2,4-дихлорфенил)-2-имидазол-1-илэтанола вместо R-(-)-энантиомера.
Необходимым условием для получения энантиомеров сертаконазола упомянутым выше способом является получение соответствующих энантиомеров промежуточного производного 1-(2,4-дихлорфенил)-2-имидазол-1-илэтанола (III).
Два энантиомера 1-(2,4-дихлорфенил)-2-имидазол-1-илэтанола (III) можно получить путем разделения соответствующей рацемической смеси с использованием оптически активной кислоты, предпочтительно L-винной кислоты, D-винной кислоты, дибензоил-L-винной кислоты, дибензоил-D-винной кислоты или т.п., и с использованием метода, описанного в патенте Великобритании No 1244530 и в статье Lammerhofer M. and Lindner W., Chiralitiy, 6:261-269,1994.(R)-(-)-1-(2,4-Дихлорфенил)-2-имидазол-1-илэтанол получают также методом энантиоселективного восстановления 1-(2,4-дихлорфенил)-2-имидазол-1-илэтанона (II) с использованием (-)- -хлордиизопинокамфенилборана [(-)-DIP-хлорида] с образованием (R)-(-)-1-(2,4-дихлорфенил)-2-имидазол-1-илэтанола ((R)-(-)-III) с приемлемой оптической чистотой. -хлордиизопинокамфенилборана [(-)-DIP-хлорида] с образованием (R)-(-)-1-(2,4-дихлорфенил)-2-имидазол-1-илэтанола ((R)-(-)-III) с приемлемой оптической чистотой.
Взаимодействие одного из энантиомеров промежуточного производного формулы (III) с 3-галогенметил-7-хлорбензо[b]тиофеном (IV) приводит к образованию соответствующего энантиомера сертаконазола в виде свободного основания. В качестве 3-галогенметил-7-хлорбензо[b]тиофена предпочтительными являются 3-хлорметил-7-хлорбензо[b]тиофен и 3-бромметил-7-хлорбензо[b]тиофен.
Энантиомеры сертаконазола в виде свободного основания могут быть превращены в фармацевтически приемлемые соли известными в данной области способами. Предпочтительно получают мононитраты с помощью обработки азотной кислотой.
Стадии получения энантиомеров сертаконазола представлены на следующей схеме.
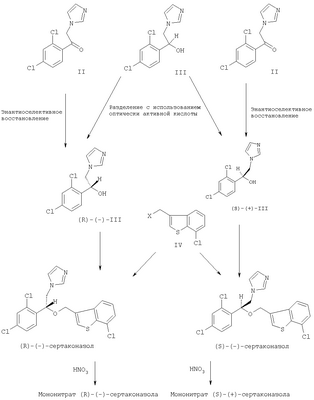
Кроме того, настоящее изобретение относится к фармацевтическим композициям, включающим (R)-(-)-сертаконазол и/или его соль, и к применению (R)-(-)-сертаконазола и/или его соли для лечения инфекций, вызванных грибами и дрожжами, у человека и животных, а также для борьбы с болезнями сельскохозяйственных культур, вызванными такими микроорганизмами.
Соединения по настоящему изобретению, по выбору смешанные с фармацевтически приемлемыми носителями, можно вводить человеку или животным пероральным путем в форме таблеток, капсул, таблеток с покрытием, сиропов, растворов, порошков, гранул, эмульсий, гелей для перорального применения, паст для перорального применения, буккофарингеальных растворов, буккофарингеальных суспензий, буккофарингеальных гелей, буккофарингеальных паст и т.п.; инъекционным способом, ректальным способом и вагинально-внутриматочным способом в форме, подобной яйцеклетке, вагинальной таблетки, вагинальной капсулы, лечебного вагинального тампона, мази, крема, геля, пены, раствора, эмульсии, суспензии, пессария, лосьона и т.п., в суточной дозе от 50 до 400 мг; и местным способом в форме крема, лосьона, пасты, суспензии, мази, эмульсии, раствора, пены, шампуня, порошка, геля и т.п., в концентрации в диапазоне от 0,05 до 3%.
Соединения по настоящему изобретению можно также по выбору смешивать с разбавителем или носителем и использовать для борьбы с болезнями сельскохозяйственных культур посредством нанесения на почву путем поливки, распыления, орошения, опыливания или в форме порошка, крема, пасты и т.п. при норме нанесения 0,05-10 кг на 1 гектар почвы.
Осуществление изобретения
Следующие примеры представлены для иллюстрации способов получения энантиомеров сертаконазола, их содержащих фармацевтических составов и их биологической активности в отношении различных микроорганизмов.
Пример 1: R-(-)-1-(2,4-дихлорфенил)-2-имидазол-1-илэтанол
В одногорлой колбе объемом 50 мл, снабженной капельной воронкой, охлаждающей баней, магнитной мешалкой и баллоном с азотом, смешивают 3,14 г (9,8 ммоль, 2,5 экв.) хлорида (-)-DIP и 9 мл безводного этилового эфира (молекулярные сита 4 å). К полученной смеси по каплям при комнатной температуре в атмосфере азота добавляют раствор 1 г (3,92 ммоль, 1 экв.) 1-(2,4-дихлорфенил)-2-имидазол-1-илэтанона в 10 мл безводного тетрагидрофурана (молекулярные сита 4 å). Смесь перемешивают в течение 24 ч при комнатной температуре в атмосфере азота. К смеси добавляют 0,4 мл метанола, перемешивают в течение 10 мин и растворители удаляют упариванием при пониженном давлении.
К полученному неочищенному продукту добавляют 10 мл н-гексана и 10 мл воды. Смесь подкисляют добавлением 1,6 мл 6 М соляной кислоты. Две фазы разделяют и органический слой удаляют. Водную фазу нейтрализуют 3 М NaOH до значения рН 10-11 в присутствии 10 мл этилового эфира. Две фазы разделяют и органический слой промывают 10 мл этилового эфира. Два слоя эфира сушат над безводным сульфатом натрия и упаривают досуха при пониженном давлении, при этом получают 1,27 г неочищенного продукта, который кристаллизуют из смеси 5 мл смеси этанол/вода, 1:1 об./об., при этом получают 0,8 г (выход 80%) R-(-)-1-(2,4-дихлорфенил)-2-имидазол-1-илэтанола. Результаты анализа:
ДСК: пик при 107,4°С
ИК-спектр: соответствует указанной структуре
1H-13С-ЯМР (ДМСО) спектр: соответствует указанной структуре
[ ]D 20 (С=1%, МеОН)=-80 ]D 20 (С=1%, МеОН)=-80
Пример 2: R-(-)-1-(2,4-Дихлорфенил)-2-имидазол-1-илэтанол
Раствор 5 г 1-(2,4-дихлорфенил)-2-имидазол-1-илэтанола в смеси ацетон/метанол (25 мл/20 мл) медленно добавляют к D-винной кислоте (3,21 г), растворенной в смеси ацетон/метанол (25 мл-10 мл) при комнатной температуре. После завершения добавления реагента реакционную смесь перемешивают в течение еще 30 мин при комантной температуре. Образующееся твердое вещество отфильтровывают и перекристаллизовывают из метанола. Выход составляет 1,85 г (37%), энанатиомерная чистота R-изомера >98%.
Пример 3: (R)-(-)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазол
В трехгорлой колбе объемом 100 мл, снабженной обратным холодильником, погружным термометром, капельной воронкой, охлаждающей баней и баллоном с азотом, смешивают 10 мл сухого N,N-диметилформамида (молекулярные сита 4 å) и 1,27 г (11,3 ммоль, 1,03 экв.) трет-бутоксида калия. К полученной смеси, охлажденной на водяной бане, по каплям добавляют раствор 2,83 г (11 ммоль) (R)-(-)-1-(2,4-дихлорфенил)-2-имидазол-1-илэтанола в 15 мл сухого N,N-диметилформамида. После завершения добавления смесь перемешивают в течение 45 мин и к раствору добавляют 2,93 г (11,2 ммоль, 1,02 экв.) 3-бромметил-7-хлорбензо[b]тиофена в 7 мл сухого N,N-диметилформамида. Реакционную смесь перемешивают в течение 4 ч при комнатной температуре. Растворитель удаляют отгонкой при пониженном давлении и остаток обрабатывают 50 мл хлористого метилена. Полученный раствор промывают 2 раза по 30 мл воды, сушат над безводным сульфатом натрия, фильтруют и упаривают досуха при пониженном давлении, при этом получают 4,62 г неочищенного продукта. Полученный неочищенный продукт очищают колоночной хроматографией на силикагеле с использованием в качестве элюента градиента хлористый метилен/метанол. Полученную смолу (2,0 г) кристаллизуют из этилового эфира (10 мл). Твердое вещество отфильтровывают и сушат, при этом получают 1,22 г (выход 25,1%) (R)-(-)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазола.
Результаты анализа:
ДСК: пик при 74,5°С
ИК-спектр: соответствует указанной структуре
1H-13С-ЯМР (ДМСО) спектр: соответствует указанной структуре
[ ]D 20 (С=1%, МеОН)=-61,0 ]D 20 (С=1%, МеОН)=-61,0
Пример 4: (S)-(+)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазол
В трехгорлой колбе объемом 100 мл, снабженной обратным холодильником, погружным термометром, капельной воронкой, охлаждающей баней и баллоном с азотом, смешивают 16 мл сухого N,N-диметилформамида (молекулярные сита 4 å) и 2,04 г (18,43 ммоль, 1,05 экв.) трет-бутоксида калия. К полученной смеси, охлажденной на водяной бане, по каплям добавляют раствор 4,44 г (17,2 ммоль) (S)-(+)-1-(2,4-дихлорфенил)-2-имидазол-1-илэтанола в 25 мл сухого N,N-диметилформамида. После завершения добавления смесь перемешивают в течение 45 мин и к раствору добавляют 4,61 г (17,62 ммоль, 1,02 экв.) 3-бромметил-7-хлорбензо[b]тиофена в 13 мл сухого N,N-диметилформамида. Реакционную смесь перемешивают в течение 4 ч при комнатной температуре. Растворитель удаляют отгонкой при пониженном давлении и остаток обрабатывают 80 мл хлористого метилена. Полученный раствор промывают 2 раза по 50 мл воды, сушат над безводным сульфатом натрия, фильтруют и упаривают досуха при пониженном давлении, при этом получают 7,30 г неочищенного продукта. Полученный неочищенный продукт очищают колоночной хроматографией на силикагеле с использованием в качестве элюента градиента хлористый метилен/метанол. Полученную смолу (3,78 г) кристаллизуют из этилового эфира (18 мл). Твердое вещество отфильтровывают и сушат, при этом получают 2,61 г (выход 34,5%) (S)-(+)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазола.
Результаты анализа:
ДСК: пик при 83,4°С
ИК-спектр: соответствует указанной структуре
1H-13С-ЯМР (ДМСО) спектр: соответствует указанной структуре
[ ]D 20 (С=1%, МеОН)=+69 ]D 20 (С=1%, МеОН)=+69
Пример 5: Мононитрат (R)-(-)-сертаконазола (мононитрат (R)-(-)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазола)
880 мг(2,01 ммоль)(R)-(-)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазола растворяют в 5 мл 96% этанола. К раствору добавляют 1 мл воды и нагревают при температуре 35-37°С. К полученному раствору добавляют 0,23 мл 60% азотной кислоты (3 ммоль, 1,5 экв.). Затем добавляют 3 мл воды и охлаждают сначала до комнатной температуры, а затем при 10°С в течение 1 ч. Полученное твердое вещество отфильтровывают, промывают 2 раза по 4 мл воды и сушат в вакууме в течение 24 ч, при этом получают 0,9 г (выход 89%) мононитрата (R)-(-)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазола.
Результаты анализа:
ДСК: пик при 116,87°С
ИК-спектр: соответствует указанной структуре
1H-13С-ЯМР (ДМСО) спектр: соответствует указанной структуре
[ ]D 20 (С=1%, МеОН)=-85,00 ]D 20 (С=1%, МеОН)=-85,00
Пример 6: Мононитрат (R)-(-)-сертаконазола (мононитрат R-(-)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазола
В колбу объемом 500 мл, оборудованную механической мешалкой, загружают 15,72 г R-(-)-1-(2,4-дихлорфенил)-2-имидазол-1-илэтанола, 45 мл толуола, 1,05 г гидросульфата тетрабутиламмония и 24,5 г 18 н. водного NaOH. Смесь нагревают при 35-40°С и эту температуру поддерживают в течение еще 15 мин. Затем добавляют раствор 3-бромметил-7-хлорбензо[b]тиофена в 376 мл толуола в течение 30 мин. В реакционной смеси поддерживают температуру от 37 до 40°С в течение 2,5 ч и затем добавляют воду. Органический слой промывают водой. После концентрирования при пониженном давлении неочищенный продукт растворяют в 150 мл абсолютного этанола. Затем медленно добавляют смесь 9,1 г 60% HNO3 и 130 мл воды и после завершения добавления реагентов реакционную смесь охлаждают до 0°С. Полученное твердое вещество отфильтровывают, перекристаллизовывают из смеси ацетон/этанол и сушат. Выход составляет 24,5 г (80%).
Пример 7: Мононитрат (S)-(+)-сертаконазола (мононитрат (S)-(+)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазола)
2,35 мг (5,37 ммоль)(S)-(+)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазола растворяют в 17 мл 96% этанола. К раствору добавляют 3 мл воды и нагревают при температуре 35-40°С. К полученному раствору добавляют 0,61 мл 60% азотной кислоты (8,06 ммоль, 1,5 экв.). Затем добавляют 13 мл воды и охлаждают сначала при комнатной температуре, а затем при 10°С в течение 1 ч. Полученное твердое вещество отфильтровывают, промывают 2 раза по 10 мл воды и сушат в вакууме в течение 24 ч, при этом получают 2,65 г (выход 98,5%) мононитрата (S)-(+)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазола.
Результаты анализа:
ДСК: пик при 168,91°С
ИК-спектр: соответствует указанной структуре
1H-13С-ЯМР (ДМСО) спектр: соответствует указанной структуре
[ ]D 20 (С=1%, МеОН)=+89,00 ]D 20 (С=1%, МеОН)=+89,00
Пример 8: Состав 1% крема
| Состав на 100 г |
| Мононитрат R-(-)-сертаконазола |
1,00 г |
| Моно- и диглицериды пальмитиновой и стеариновой кислот |
6,00 г |
| Кетостеариловый спирт, содержащий 20 моль этиленоксида |
1,00 г |
| Дециловый эфир олеиновой кислоты |
5,00 г |
| Моноэтаноламин ундециленовой кислоты |
2,00 г |
| Карбомер |
1,00 г |
| Триэтаноламин |
0,60 г |
| Метилпарабен |
0,15 г |
| Пропилпарабен |
0,05 г |
| Дистиллированная вода до объема |
100,00 г |
Пример 9: Состав 1% геля
| Состав на 100 г |
| Мононитрат R-(-)-сертаконазола |
1,00 г |
| Пропиленгликоль |
10,00 г |
| Кабомер |
1,00 г |
| Твин 20 |
0,10 г |
| Феноксиэтанол |
0,35 г |
| Динатриевая соль ЭДТУ |
0,15 г |
| Лимонная кислота |
0,25 г |
| 1 н. гидроксид натрия |
1,50 г |
| Триэтаноламин |
1,55 г |
| Дистиллированная вода до объема |
100,00 г |
Пример 10: Биологические данные
Величины минимальной ингибирующей концентрации (МИК) определяют с использованием модифицированного метода микроразбавлений М27-А, рекомендованного Национальным комитетом по клиническим лабораторным стандартам, в среде RPMI-1640 (фирмы Sigma), дополненной глюкозой до концентрации 2% и доведенной до рН 7,0 с помощью 0,165 М буферного раствора, содержащего морфолин-пропансульфоновую кислоту (MOPS). Из исходных растворов соединений готовят серийные двухкратные разведения в модифицированной среде RPMI-1640. Величины МИК определяют по минимальной концентрации лекарственного средства, при которой наблюдается ингибирование роста на 50% по сравнению с ростом контрольного микроорганизма. Микробиологическая активность R-(-)-сертаконазола по сравнению с S-(+)-энантиомером, который значительно менее активен, и с рацемическим сертаконазолом представлена в виде среднегеометрических величин в таблице. Число штаммов, использованных в экспериментах, показано в скобках рядом с названием каждого микроорганизма.
| |
| МИК (мкг/мл) нитрата сертаконазола и его энантиомеров |
| Микроорганизм |
R-(-)-энантиомер |
Рацемат |
S-(+)энантиомер |
| Candida spp (42) |
0,125 |
0,256 |
3,217 |
| Dermatophytes (17) |
0,04 |
0,08 |
0,17 |
| Filamentous fungi (11) |
1,76 |
3,11 |
16 |
| Malassezia spp (11) |
0,64 |
1,37 |
10,96 |
Формула изобретения
1. R-(-)-1-[2-(7-Хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазол формулы (I)
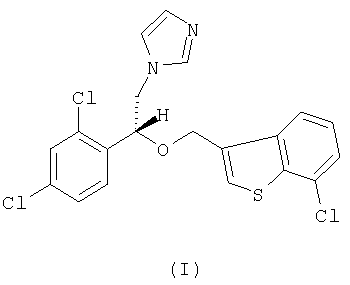
или его фармацевтически приемлемые соли.
2. Мононитрат R-(-)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1H-имидазола.
3. Способ получения соединения по п.1 или 2, отличающийся тем, что проводят взаимодействие R-(-)-1-(2,4-дихлорфенил)-2-имидазол-1-илэтанола формулы ((R)-(-)-III)
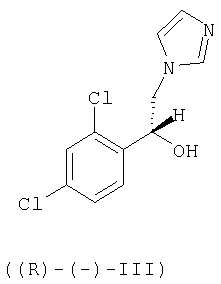
с 3-галогенметил-7-хлорбензо[b]тиофеном формулы (IV)
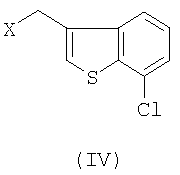
где X означает галоген, и по выбору обрабатывают полученный R-(-)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазол солеобразующей кислотой.
4. Способ по п.3, отличающийся тем, что Х означает хлор или бром.
5. Способ по п.3 или 4, отличающийся тем, что соединением является мононитрат R-(-)-1 -[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлор-фенил)этил]-1Н-имидазола, а солеобразующей кислотой является азотная кислота.
6. Способ по п.3 или 4, отличающийся тем, что R-(-)-1-(2,4-дихлорфенил)-2-имидазол-1-илэтанол формулы ((R)-(-)-III) получают посредством энантиоселективного восстановления 1-(2,4-дихлорфенил)-2-имидазол-1-илэтанона с использованием (-)- -хлордиизопинокамфенил-борана. -хлордиизопинокамфенил-борана.
7. Способ по п.5, отличающийся тем, что R-(-)-1-(2,4-дихлорфенил)-2-имидазол-1-илэтанол формулы ((R)-(-)-III) получают посредством энантиоселективного восстановления 1-(2,4-дихлорфенил)-2-имидазол-1-илэтанона с использованием (-)- -хлордиизопинокамфенилборана. -хлордиизопинокамфенилборана.
8. Композиция, обладающая противогрибковым действием, содержащая R-(-)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлор-фенил)этил]-1Н-имидазол или его соль.
9. Композиция по п.8, в которой указанной солью является мононитрат.
10. Композиция по любому из п.8 или 9, которая является фармацевтической композицией.
11. Композиция по любому из п.8 или 9, которая является сельскохозяйственной композицией.
12. Применение R-(-)-1-[2-(7-хлорбензо[b]тиофен-3-илметокси)-2-(2,4-дихлорфенил)этил]-1Н-имидазола или его соли в качестве активного ингредиента противогрибковой композиции.
13. Применение по п.12, в котором указанной солью является мононитрат.
14. Применение по любому из п.12 или 13, в котором указанная композиция используется для лечения грибковых инфекций у человека или животных.
15. Применение по любому из п.12 или 13, в котором указанная композиция используется для борьбы с болезнями сельскохозяйственных культур.
|
|