Патент на изобретение №2276145
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 5,6-ФТАЛИЛФЕНОТИАЗИН-S, S-ДИОКСИДА
(57) Реферат:
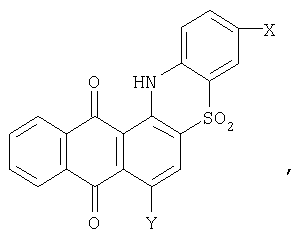
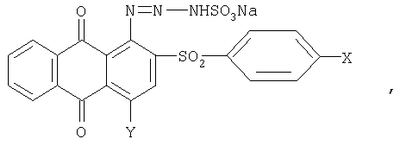
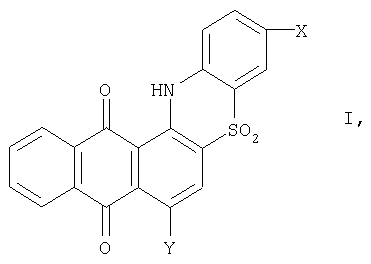
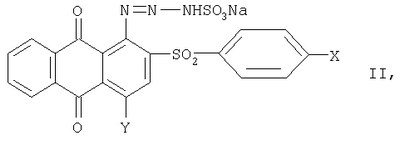
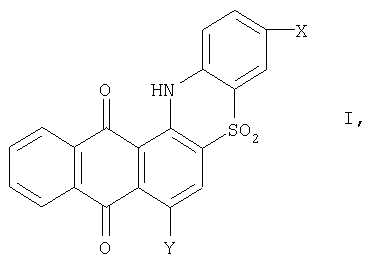
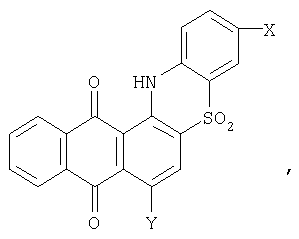
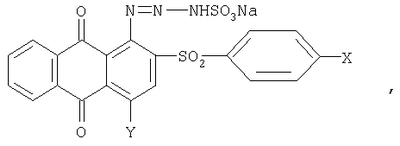
Изобретение относится к способу получения производных 5,6-фталилфенотиазин-S,S-диоксида, которые могут быть использованы на предприятиях анилинкрасочной промышленности для получения антрахиноновых красителей. Описывается способ получения производных 5,6-фталилфенотиазин-S,S-диоксида общей формулы где X – водород, галоген или низший алкил; Y – водород или гидроксигруппа, нагреванием производного 2-фенилсульфонилантрахинона в органическом растворителе, при этом в качестве производного 2-фенилсульфонилантрахинона используют 1-(триазен-N-сульфонат)-2-фенилсульфонилантрахинон общей формулы где X и Y имеют указанные значения, который в присутствии щелочи кипятят в этиленгликоле или нагревают в глицерине при температуре 190-230°С. Технический результат – упрощение технологии процесса и расширение ассортимента целевых продуктов. 2 табл.
Изобретение относится к химии и технологии органических красителей и может быть использовано на предприятиях анилинокрасочной промышленности для получения антрахиноновых красителей. Известен способ получения 5,6-фталилфенотиазин-S,S-диоксидов, который заключается в окислении соответствующих 5,6-фталилфенотиазинов пероксидом водорода в уксусной кислоте (Патент 3519623. 1970. США. С.А. V.73, 121548а). Недостатком этого способа является использование взрывоопасного пероксида водорода, продолжительность проведения процесса окисления, а также то, что используемые для окисления 5,6-фталилфенотиазины сами являются превосходными красителями для полиэфирных волокон (Ред. К.Венкатараман. Изд. «Химия», 1974.3.205). Недостатком получения 1-азидо-2-фенилсульфонилантрахинонов является использование азотистоводородной кислоты или ее солей щелочных металлов, которые могут образовывать взрывоопасные смеси как с воздухом (азотистоводородная кислота), так и в присутствии тяжелых металлов (азиды тяжелых металлов взрывоопасны), что делает процесс небезопасным. Задача решаемая изобретением заключается в создании нового способа получения производных 5,6-фталилфенотиазин-S,S-диоксида. Технический результат – упрощение технологии процесса и расширение ассортимента целевых продуктов. Указанный технический результат достигается способом получения соединений общей формулы I, который заключается в том, что 1-(триазен-N-сульфонат)-2-фенилсульфонилантрахинон общей формулы II где Х и Y имеют вышеуказанные значения, кипятят в этиленгликоле или нагревают в глицерине в присутствии щелочи при температуре 190-230°С. Полученную массу охлаждают, нейтрализуют уксусной кислотой, осадок отфильтровывают, промывают на фильтре водой и получают чистый продукт. Сущность изобретения: продукт: производные 5,6-фталилфенотиазин-S,S-диоксида формулы I где Х – водород, галоген или низший алкил, Y – водород или гидроксигруппа. Реагент: 1-(триазен-N-сульфонат)-2-фенилсульфонилантрахинон формулы II Условия реакции: кипячение в этиленгликоле или нагревание в глицерине в присутствии щелочи при температуре до 230°С. Предлагаемый способ позволяет получать производные 5,6-фталилфенотиазин-S,S-диоксида с высоким выходом из неиспользованных ранее для этой цели 1-(триазен-N-сульфонат)-2-фенилсульфонилантрахинонов. Состав и строение полученных 5,6-фталилфенотиазин-S,S-диоксидов установлены с помощью элементного анализа и физико-химических методов. Пример 1. 5,6-Фталилфенотиазин-S,S-диоксид 4,93 г (0,01 моль) 1-(триазен-N-сульфонат)-2-фенилсульфонилантрахинона, кипятят в колбе с обратным холодильником при перемешивании в 40 мл этиленгликоля, содержащего 0,4 г (0,01 моль) гидроксида натрия, в течение 2,5 часов. Реакционную массу охлаждают до 10-15°С, нейтрализуют уксусной кислотой, выпавшие кристаллы отфильтровывают, промывают на фильтре 20-25 мл горячей воды, высушивают при комнатной температуре. Выход продукта составил 2,96 г (82%) Тпл=284-286°С. Найдено, %: N 4,18, 3,94; S 8,66, 9,01. C20H11NO4S. Вычислено, %: N 3,88; S 8,86. Пример 2. 5,6-Фталил-7-гидроксифенотиазин-S,S-диоксид В колбу, снабженную обратным холодильником, загружают 5,09 г (0,01 моль) 1-(триазен-N-сульфонат)-2-фенилсульфонил-4-гидроксилантрахинона заливают 50 мл глицерина, содержащего 0,4 г (0,01 моль) гидроксида калия и нагревают на масляной бани при температуре 230°С в течение 2,5 часов (нагревание в глицерине при более высокой температуре нежелательно, т.к. начинается процесс его разложения). Реакционную массу охлаждают до 10-15°С, нейтрализуют уксусной кислотой, выпавшие кристаллы отфильтровывают, промывают на фильтре 20-25 мл горячей воды, высушивают при комнатной температуре. Выход продукта составил 3,18 г (85%) Тпл=304-306°С. Найдено, %: N 3,87, 4,20; S 8,30, 8,52. C20H11NO5S. Вычислено, %: N 3,71; S 8,49. Пример 3. 5,6-Фталилфенотиазин-S,S-диоксид 4,93 г (0,01 моль) 1-(триазен-N-сульфонат)-2-фенилсульфонилантрахинона кипятят в колбе с обратным холодильником при перемешивании в 40 мл глицерина, содержащего 0,4 г (0,01 моль) гидроксида калия, в течение 2 часов. Реакционную массу охлаждают до 10-15°С, нейтрализуют уксусной кислотой, выпавшие кристаллы отфильтровывают, промывают на фильтре 20-25 мл горячей воды, высушивают при комнатной температуре. Выход продукта составил 2,96 г (82%) Тпл=284-286°С. Найдено, %: N 4,17, 3,95; S 8,67, 9,00. C20H11NO4S. Вычислено, %: N 3,88; S 8,86. Синтез остальных 5,6-фталилфенотиазин-S,S-диоксидов проводят аналогично при нагревании в глицерине, в присутствии щелочи при температуре до 230°С, их характеристики приведены в таблице 1. Синтез исходных 1-(триазен-N-сульфонат)-2-фенилсульфонилантрахинонов, используемых для получения 5,6-фталилфенотиазин-S,S-диоксидов осуществляют следующим образом. Пример 4. 1-(Триазен-N-сульфонат)-2-фенилсульфонилантрахинон Раствор 3,63 г (0,01 моль) 1-амино-2-фенилсульфонилантрахинона в 100 мл уксусной кислоты диазотируют при 5-10°С в течение 2 часов, раствором нитрозилсерной кислоты, приготовленной из 0,83 г (0,012 моль) нитрита натрия и 10 мл 95% серной кислоты. Затем реакционную массу разбавляют 10-15 мл воды, добавляют активированный уголь и отфильтровывают от примеси. Затем в фильтрат при перемешивании и охлаждении прибавляют 1,43 г (0,012 моль) натриевой соли сульфаминовой кислоты и 0,098 г (0,012 моль) ацетата натрия. Выдерживают 15-20 минут при перемешивании, затем реакционную смесь разбавляют 100-150 мл холодной воды, выпавшие кристаллы 1-(триазен-N-сульфонат)-2-фенилсульфонилантрахинона отфильтровывают, промывают на фильтре холодной водой, сушат при комнатной температуре. Выход продукта составил 4,14 г (84%) Тпл=141°С. Найдено, %: N 8,38, 8,65; S 12,81, 13,05. C20H12N3O7S2Na. Вычислено, %: N 8,52; S 12,98. Синтез остальных 1-(триазен-N-сульфонат)-2-фенилсульфонилантрахинонов проводится в аналогичных условиях. Характеристики полученных соединений приведены в таблице 2. Исходные 1-амино-2-фенилсульфонилантрахиноны получены известным способом, при взаимодействии 1-амино-2-хлорантрахинона и 1-амино-2-хлор-4-гидроксиантрахинона с натриевыми солями фенилсульфиновых кислот (Патент 1266902. 1968. ФРГ. С.А. V.69. 28600 и). Полученные производные 5,6 фталилфенотиазин-S,S-диоксида могут найти применение в качестве красителей для полиэфирных волокон.
Формула изобретения
Способ получения производных 5,6-фталилфенотиазин-S,S-диоксида общей формулы где Х – водород, галоген или низший алкил; Y – водород или гидроксигруппа, нагреванием производного 2-фенилсульфонилантрахинона в органическом растворителе, отличающийся тем, что в качестве производного 2-фенилсульфонилантрахинона используют 1-(триазен-N-сульфонат)-2-фенилсульфонилантрахинон общей формулы где Х и Y имеют указанные значения, который в присутствии щелочи кипятят в этиленгликоле или нагревают в глицерине при температуре 190-230°С.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 08.02.2007
Извещение опубликовано: 27.09.2008 БИ: 27/2008
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||