Патент на изобретение №2155767
|
||||||||||||||||||||||||||
(54) БИОДОСТУПНАЯ
(57) Реферат: Изобретение относится к биодоступной  -кристаллической форме цефуроксимаксетила, полученной в результате обработки известной кристаллической или аморфной формы цефуроксимаксетила водой или смешивающегося с водой органическим растворителем или их смесью при температуре 20-100oС, с последующим охлаждением и выделением кристаллического продукта. 2 с. и 2 з.п. ф-лы, 4 ил. -кристаллической форме цефуроксимаксетила, полученной в результате обработки известной кристаллической или аморфной формы цефуроксимаксетила водой или смешивающегося с водой органическим растворителем или их смесью при температуре 20-100oС, с последующим охлаждением и выделением кристаллического продукта. 2 с. и 2 з.п. ф-лы, 4 ил.
Настоящее изобретение относится к биодоступной кристаллической форме цефуроксимаксетила, т. е. к (6R, 7R)-3-карбамоилоксиметил-7-[(Z)-2-(фур-2-ил)-2- метоксииминоацетамидо] -3-цефем-4-карбоновой кислоты 1-ацетоксиэтиловому сложному эфиру. Цефуроксим является известным продуктом, его получение описано в патенте США А-3974153. Он отличается широким спектром антибактериальной активности, распространяясь как на грам-положительные, так и на грам-отрицательные микроорганизмы. Цефуроксим невозможно использовать как таковой для орального введения, так как он не абсорбируется, и не попадает в циркулирующие в организме жидкости. Цефуроксимаксетил представляет собой пролекарство для орального введения, которое отличается высокой стабильностью относительно штаммов, продуцирующих  -лактамазу. В этом плане, после того, как сложный эфир абсорбируется и попадает в циркулирующие жидкости организма, он гидролизуется с высвобождением цефуроксима, который на самом деле и отвечает за антибактериальную активность.
В примере 1 GB-А-1571683 впервые раскрыто получение цефуроксимаксетила в кристаллической форме, известную далее как “ -лактамазу. В этом плане, после того, как сложный эфир абсорбируется и попадает в циркулирующие жидкости организма, он гидролизуется с высвобождением цефуроксима, который на самом деле и отвечает за антибактериальную активность.
В примере 1 GB-А-1571683 впервые раскрыто получение цефуроксимаксетила в кристаллической форме, известную далее как “ -кристалл”: далее приводится характеристика -кристалл”: далее приводится характеристика  -кристалла с помощью ИК полностью по данным примера 1 GB-А-2145409 Glaxo Group Ltd.
Однако -кристалла с помощью ИК полностью по данным примера 1 GB-А-2145409 Glaxo Group Ltd.
Однако  -кристаллическая форма цефуроксимаксетила не обладает необходимыми характеристиками биодоступности, тогда как известно, что вводимые перорально цефалоспорины (и вообще медикаменты) должны быть в высокой биодоступной форме.
В этом отношении коммерчески доступный цефуроксимаксетил, зарегистрированный по всему миру, находится в по-существу аморфной форме, как заявлено и раскрыто в патенте США US-А-4562181 от имени Glaxo Group Ltd, в которой указывается, что “кристаллический продукт” ( -кристаллическая форма цефуроксимаксетила не обладает необходимыми характеристиками биодоступности, тогда как известно, что вводимые перорально цефалоспорины (и вообще медикаменты) должны быть в высокой биодоступной форме.
В этом отношении коммерчески доступный цефуроксимаксетил, зарегистрированный по всему миру, находится в по-существу аморфной форме, как заявлено и раскрыто в патенте США US-А-4562181 от имени Glaxo Group Ltd, в которой указывается, что “кристаллический продукт” ( -кристалл) “не обладает наилучшим балансом свойств для коммерческого использования” (колонка 2, строки 3-6), тогда как “по-существу аморфная форма имеет более высокую биодоступность после перорального введения, нежели кристаллическая форма” (колонка 2, строки 10-15). В этом плане следует отметить, что, как указывают Glaxo в своем патенте US-А-4562181, вообще, кристаллические формы имеют наилучший баланс между физико-химическими и биологическими свойствами и хорошую стабильность как в процессе хранения, так и при продаже (колонка 1, строки 57-61).
Как следует из дальнейшего примера 1, который составляет часть настоящего описания, процедура, раскрытая в примере 1 GB-А-2145409 и в примере получения 2 US-А-4562181, была повторена, чтобы получить цефуроксимаксетил в -кристалл) “не обладает наилучшим балансом свойств для коммерческого использования” (колонка 2, строки 3-6), тогда как “по-существу аморфная форма имеет более высокую биодоступность после перорального введения, нежели кристаллическая форма” (колонка 2, строки 10-15). В этом плане следует отметить, что, как указывают Glaxo в своем патенте US-А-4562181, вообще, кристаллические формы имеют наилучший баланс между физико-химическими и биологическими свойствами и хорошую стабильность как в процессе хранения, так и при продаже (колонка 1, строки 57-61).
Как следует из дальнейшего примера 1, который составляет часть настоящего описания, процедура, раскрытая в примере 1 GB-А-2145409 и в примере получения 2 US-А-4562181, была повторена, чтобы получить цефуроксимаксетил в  -кристаллической форме, для которого ИК анализ был проведен в KBr.
Этот ИК анализ подтвержден, особенно в интервале частот между 1000 и 500 см-1, спектром, опубликованным в упомянутом патенте, показывая значительную идентичность между двумя ИК спектрами.
Таким образом, даже сегодня, несмотря на исследования, проводимые во всем мире в этой области, известны только -кристаллической форме, для которого ИК анализ был проведен в KBr.
Этот ИК анализ подтвержден, особенно в интервале частот между 1000 и 500 см-1, спектром, опубликованным в упомянутом патенте, показывая значительную идентичность между двумя ИК спектрами.
Таким образом, даже сегодня, несмотря на исследования, проводимые во всем мире в этой области, известны только  -кристаллическая форма цефуроксимаксетила (который не является биодоступным) и по-существу аморфная форма (которая является биодоступной).
В соответствии с настоящим изобретением было неожиданно обнаружено, что, если цефуроксимаксетил в -кристаллическая форма цефуроксимаксетила (который не является биодоступным) и по-существу аморфная форма (которая является биодоступной).
В соответствии с настоящим изобретением было неожиданно обнаружено, что, если цефуроксимаксетил в  -кристаллической форме или в по-существу аморфной форме обработать смесью воды и смешивающегося с водой органического растворителя, в весовом отношении от 100:0 до 0:100 при температуре от +20oC до 100oC с последующим охлаждением, можно получить цефуроксимаксетил в кристаллической форме, которая отличается от -кристаллической форме или в по-существу аморфной форме обработать смесью воды и смешивающегося с водой органического растворителя, в весовом отношении от 100:0 до 0:100 при температуре от +20oC до 100oC с последующим охлаждением, можно получить цефуроксимаксетил в кристаллической форме, которая отличается от  -кристаллической формы, и будет обозначаться здесь, как -кристаллической формы, и будет обозначаться здесь, как  -кристаллическая форма, или -кристаллическая форма, или  -кристалл.
И снова было неожиданно обнаружено, что -кристалл.
И снова было неожиданно обнаружено, что  -кристалл отличается прекрасными характеристиками биодоступности, что обеспечивает возможность его применения в терапии, при прекрасном балансе между физико-химическими и биологическими свойствами и хорошей стабильностью при хранении и продаже, о чем заявлено Glaxo в их патенте US-А-4562181.
Как будет видно из экспериментальной части, ИК спектр -кристалл отличается прекрасными характеристиками биодоступности, что обеспечивает возможность его применения в терапии, при прекрасном балансе между физико-химическими и биологическими свойствами и хорошей стабильностью при хранении и продаже, о чем заявлено Glaxo в их патенте US-А-4562181.
Как будет видно из экспериментальной части, ИК спектр  -кристалла получают тем же способом, что и для -кристалла получают тем же способом, что и для  -кристалла. Обнаружено, что два ИК спектра существенно отличаются друг от друга, особенно в интервале частот между 1000 и 5000 см-1.
Для большей определенности были также получены рентгеновские спектры для -кристалла. Обнаружено, что два ИК спектра существенно отличаются друг от друга, особенно в интервале частот между 1000 и 5000 см-1.
Для большей определенности были также получены рентгеновские спектры для  – и – и  -кристаллов, которые отчетливо свидетельствуют о различии их структур.
Реакции, приводимые в нижеследующих примерах, контролировали с помощью ВЭЖХ (подвижная фаза: 30% ацетонитрил, 70% 0,03 М фосфатный буфер; колонка Lichrospher RP60 Select В 5 мк, температура 45oC; детектор УФ 270 нм; скорость элюирования 1,7 мл/мин).
ИК спектр снят в твердом состоянии (в таблетках KBr) на спектрофотометре FT-JR 8101 М SHIMADZU.
Дифракционный спектр рентгеновских лучей получен для измельченных в порошок кристаллов на дифрактометре PHILIPS PW 1710 с излучением при длине волны 1,54051 -кристаллов, которые отчетливо свидетельствуют о различии их структур.
Реакции, приводимые в нижеследующих примерах, контролировали с помощью ВЭЖХ (подвижная фаза: 30% ацетонитрил, 70% 0,03 М фосфатный буфер; колонка Lichrospher RP60 Select В 5 мк, температура 45oC; детектор УФ 270 нм; скорость элюирования 1,7 мл/мин).
ИК спектр снят в твердом состоянии (в таблетках KBr) на спектрофотометре FT-JR 8101 М SHIMADZU.
Дифракционный спектр рентгеновских лучей получен для измельченных в порошок кристаллов на дифрактометре PHILIPS PW 1710 с излучением при длине волны 1,54051 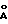 и 1,54433 и 1,54433 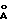 , производимых рентгеновской трубкой с медным анодом, напряжением генератора 40 кB и силой тока в генераторе 40 мА.
Образцы, подвергавшиеся исследованию, устанавливали в NISKAMEN на держатель образца, чтобы избежать предпочтительной ориентации. Данные получены после калибровки прибора с помощью внешнего стандарта, показания и графическое построение спектра получены с помощью ADP 3.6 PC программы.
ПРИМЕР 1 , производимых рентгеновской трубкой с медным анодом, напряжением генератора 40 кB и силой тока в генераторе 40 мА.
Образцы, подвергавшиеся исследованию, устанавливали в NISKAMEN на держатель образца, чтобы избежать предпочтительной ориентации. Данные получены после калибровки прибора с помощью внешнего стандарта, показания и графическое построение спектра получены с помощью ADP 3.6 PC программы.
ПРИМЕР 1 -кристаллическую форму синтезировали в соответствии со способом получения, представленным в примере 1 GB-А-2145409 и в примере получения 2 US-А-4562181. Таким образом получили 12,5 г (R,S)-1-ацетоксиэтилбромида путем взаимодействия 3,30 г ацетальдегида с 9,20 г ацетилбромида в 30 мл DMAC и 12 мг безводного хлорида цинка в течение 4 часов при -10oC. Полученный раствор добавляют к перемешенной суспензии 20 г цефуроксима натрия в 80 мл DMAC. Реакцию ведут в течение 90 минут при -1oC с добавлением 0,5 г карбоната калия и оставляют для завершения реакции еще на два часа при температуре от +1 до +3oC. Затем полученную смесь быстро добавляют к смеси 200 мл этилацетата и 200 мл 3% раствора бикарбоната натрия. После перемешивания в течение одного часа органическую фазу отделяют, снова промывают 100 мл нормального раствора соляной кислоты и затем 30 мл 20% раствора NaCl, содержащего 2% бикарбоната натрия. Собирают все водные фазы и снова экстрагируют 100 мл этилацетата, собранные органические фазы обесцвечивают углем (2 г) при температуре окружающей среды в течение 30 минут. После фильтрования растворитель удаляют в вакууме при 20oC, систему концентрируют до 150 г и перемешивают в течение 1 часа при температуре окружающей среды до получения значительной кристаллизации. Медленно добавляют 250 мл диизопропилового эфира (45 минут) и перемешивание продолжают в течение одного часа. Полученный продукт отфильтровывают в вакууме и промывают смесью 1:2 ацетат/простой эфир. Затем полученный продукт сушат в вакууме при 50oC, в результате чего получают продукт, образец которого (идентифицированный как 115/5 FP) исследуют для получения ИК спектра и рентгеновского спектра, показанных на фиг. 1 и 2, соответственно, характеристика -кристаллическую форму синтезировали в соответствии со способом получения, представленным в примере 1 GB-А-2145409 и в примере получения 2 US-А-4562181. Таким образом получили 12,5 г (R,S)-1-ацетоксиэтилбромида путем взаимодействия 3,30 г ацетальдегида с 9,20 г ацетилбромида в 30 мл DMAC и 12 мг безводного хлорида цинка в течение 4 часов при -10oC. Полученный раствор добавляют к перемешенной суспензии 20 г цефуроксима натрия в 80 мл DMAC. Реакцию ведут в течение 90 минут при -1oC с добавлением 0,5 г карбоната калия и оставляют для завершения реакции еще на два часа при температуре от +1 до +3oC. Затем полученную смесь быстро добавляют к смеси 200 мл этилацетата и 200 мл 3% раствора бикарбоната натрия. После перемешивания в течение одного часа органическую фазу отделяют, снова промывают 100 мл нормального раствора соляной кислоты и затем 30 мл 20% раствора NaCl, содержащего 2% бикарбоната натрия. Собирают все водные фазы и снова экстрагируют 100 мл этилацетата, собранные органические фазы обесцвечивают углем (2 г) при температуре окружающей среды в течение 30 минут. После фильтрования растворитель удаляют в вакууме при 20oC, систему концентрируют до 150 г и перемешивают в течение 1 часа при температуре окружающей среды до получения значительной кристаллизации. Медленно добавляют 250 мл диизопропилового эфира (45 минут) и перемешивание продолжают в течение одного часа. Полученный продукт отфильтровывают в вакууме и промывают смесью 1:2 ацетат/простой эфир. Затем полученный продукт сушат в вакууме при 50oC, в результате чего получают продукт, образец которого (идентифицированный как 115/5 FP) исследуют для получения ИК спектра и рентгеновского спектра, показанных на фиг. 1 и 2, соответственно, характеристика  -кристалла.
На фиг. 1 по горизонтальной оси отложены см-1, а по вертикальной – процент пропускания (%Т). На фиг. 2 по горизонтальной оси отложены величины углов, а по вертикальной – пиковые интенсивности.
Из фиг. 2 видно, что спектр дифракции рентгеновских лучей -кристалла.
На фиг. 1 по горизонтальной оси отложены см-1, а по вертикальной – процент пропускания (%Т). На фиг. 2 по горизонтальной оси отложены величины углов, а по вертикальной – пиковые интенсивности.
Из фиг. 2 видно, что спектр дифракции рентгеновских лучей  -кристалла имеет следующие характеристики.
Угол (20o) – Относительная интенсивность (%) -кристалла имеет следующие характеристики.
Угол (20o) – Относительная интенсивность (%)5.555 – 18.1 5.850 – 7.7 7.770 – 100.0 8.765 – 39.6 9.055 – 42.0 11.120 – 23.2 11.855 – 34.4 12.525 – 26.2 14.160 – 13.3 15.695 – 23.2 17.950 – 63.4 18.170 – 45.3 18.725 – 66.4 19.140 – 85.7 19.590 – 37.3 20.025 – 49.5 20.600 – 36.6 20.860 – 38.1 21.485 – 27.5 22.565 – 67.4 23.815 – 47.8 24.900 – 50.4 26.075 – 23.8 26.700 – 35.1 28.015 – 13.3 29.170 – 11.5 30.235 – 10.3 30.830 – 6.7 31.780 – 15.1 33.120 – 9.9 33.735 – 6.7 36.695 – 6.7 40,850 – 8.1 43.870 – 4.7 46.505 – 3.2 54,590 – 0.0 55.640 – 14.4 57.215 – 3.2 58.135 – 4.4 ПРИМЕР 2  -кристалл, полученный в примере 1, переводят в -кристалл, полученный в примере 1, переводят в  -форму следующим способом: 15 г цефуроксимаксетила суспендируют в 150 мл воды, систему нагревают до 40oC в течение трех часов, продукт отфильтровывают в вакууме и промывают водой. Полученный продукт сушат в вакууме при 40oC для получения 14 г твердого вещества ( -форму следующим способом: 15 г цефуроксимаксетила суспендируют в 150 мл воды, систему нагревают до 40oC в течение трех часов, продукт отфильтровывают в вакууме и промывают водой. Полученный продукт сушат в вакууме при 40oC для получения 14 г твердого вещества ( -кристалл), имеющего соотношение R/S такое же, что и в исходном продукте. Образец кристаллического продукта -кристалл), имеющего соотношение R/S такое же, что и в исходном продукте. Образец кристаллического продукта  -формы, полученного таким образом (идентифицированный как 104/5 FP) анализируют, и полученные спектры представлены на фиг. 3 (ИК спектр) и 4 (XR спектр). По горизонтали и вертикали отложены те же величины, что и на фиг. 1 и 2.
Видно, что спектр дифракции рентгеновских лучей -формы, полученного таким образом (идентифицированный как 104/5 FP) анализируют, и полученные спектры представлены на фиг. 3 (ИК спектр) и 4 (XR спектр). По горизонтали и вертикали отложены те же величины, что и на фиг. 1 и 2.
Видно, что спектр дифракции рентгеновских лучей  -кристалла имеет следующие характеристики: -кристалла имеет следующие характеристики:Угол (20o) – Относительная интенсивность (%) 7.585 – 35.7 8.200 – 15.3 9.195 – 62.9 9.405 – 6.3 10.385 – 21.5 11.875 – 23.6 12.530 – 62.0 12.605 – 53.6 12.840 – 19.5 13.960 – 19.0 14.460 – 7.2 14.870 – 2.8 15.535 – 10.1 15.895 – 29.4 16.270 – 17.1 16.545 – 12.8 16.910 – 68.4 18.270 – 71.2 18.830 – 21.5 19.135 – 25.8 19.680 – 14.0 20.500 – 28.8 21.260 – 100.0 21.930 – 28.8 22.495 – 31.8 22.785 – 36.4 23.080 – 19.0 23.565 – 14.4 24.865 – 46.5 25.425 – 42.7 26.225 – 15.7 26.880 – 14.4 27.950 – 10.1 28.910 – 11.2 30.270 – 8.8 30.965 – 10.5 31.990 – 8.4 32.405 – 5.0 33.340 – 3.6 34.820 – 17.6 36.355 – 5.5 37.500 – 4.3 38.560 – 5.0 39.320 – 6.6 40.590 – 3.4 41.300 – 3.0 42.360 – 4.3 43.410 – 5.0 44.840 – 2.3 46.605 – 2.6 49.615 – 1.1 51.045 – 1.2 52.620 – 2.3 ПРИМЕР 3 20 г цефуроксимаксетила (полученного по способу GB-А-1571683) растворяют в 500 мл метанола при 40oC; поддерживая этот раствор в горячем состоянии, 1000 мл воды с температурой 40oC медленно добавляют. После завершения добавления систему охлаждают до температуры окружающей среды и фильтруют в вакууме, промывая продукт водой. Высушенный продукт (13,5 г) имеет соотношение R/S 0,85:1, тогда как исходный продукт имел соотношение R/S 0,94:1. Твердое вещество (  -кристалл) дает спектры ИК и XR, отличающиеся от спектров исходного продукта, что представлено на фиг. 3 и 4.
ПРИМЕР 4 -кристалл) дает спектры ИК и XR, отличающиеся от спектров исходного продукта, что представлено на фиг. 3 и 4.
ПРИМЕР 450 г высушенного распылением цефуроксимаксетила в по-существу аморфной форме суспендируют в 500 мл воды и нагревают до 40oC, продолжая перемешивание в течение трех часов. Систему охлаждают до температуры окружающей среды и фильтруют, промывая продукт водой. Высушенное твердое вещество дает 46 г продукта, ИК и XR спектры которого показывают превращение в  -кристалл. При этом соотношение R/S составляет величину 1,2:1,0.
ПРИМЕР 5 -кристалл. При этом соотношение R/S составляет величину 1,2:1,0.
ПРИМЕР 55 г аморфного цефуроксимаксетила (полученного по способу примера 22 US-А-4562181) обрабатывают при 40oC в течение 3 часов 50 мл воды. Высушенный продукт (4,8 г) имеет соотношение R/S 0,64, и его ИК спектр аналогичен спектру, представленному на фиг. 3 (  – кристалл). – кристалл).
Формула изобретения
 -кристаллическая форма цефуроксимаксетила, имеющая следующий рентгеновский спектр: -кристаллическая форма цефуроксимаксетила, имеющая следующий рентгеновский спектр:Угол (20o) – Отн. интенсивность (%) 7.585 – 35.7 8.200 – 15.3 9.195 – 62.9 9.405 – 6.3 10.385 – 21.5 11.875 – 23.6 12.530 – 62.0 12.605 – 53.6 12.840 – 19.5 13.960 – 19.0 14.460 – 7.2 14.870 – 2.8 15.535 – 10.1 15.895 – 29.4 16.270 – 17.1 16.545 – 12.8 16.910 – 68.4 18.270 – 71.2 18.830 – 21.5 19.135 – 25.8 19.680 – 14.0 20.500 – 28.8 21.260 – 100.0 21.930 – 28.8 22.495 – 31.8 22.785 – 36.4 23.080 – 19.0 23.565 – 14.4 24.865 – 46.5 25.425 – 42.7 26.225 – 15.7 26.880 – 14.4 27.950 – 10.1 28.910 – 11.2 30.270 – 8.8 30.965 – 10.5 31.990 – 8.4 32.405 – 5.0 33.340 – 3.6 34.820 – 17.6 36.355 – 5.5 37.500 – 4.3 38.560 – 5.0 39.320 – 6.6 40.590 – 3.4 41.300 – 3.0 42.360 – 4.3 43.410 – 5.0 44.840 – 2.3 46.605 – 2.6 49.615 – 1.1 51.045 – 1.2 52.620 – 2.3 2. Биодоступная  -кристаллическая форма цефуроксимаксетила по п.1, отличающаяся тем, что является смесью R/S диастереоизомеров в отношении от 0 : 1,0 до 1,0 : 0.
3. Биодоступная -кристаллическая форма цефуроксимаксетила по п.1, отличающаяся тем, что является смесью R/S диастереоизомеров в отношении от 0 : 1,0 до 1,0 : 0.
3. Биодоступная  -кристаллическая форма цефуроксимаксетила по п.2, отличающаяся тем, что соотношение диастереоизомеров в смеси составляет величину от 0,9 : 1,1 до 1,1 : 0,9.
4. Способ получения биодоступной -кристаллическая форма цефуроксимаксетила по п.2, отличающаяся тем, что соотношение диастереоизомеров в смеси составляет величину от 0,9 : 1,1 до 1,1 : 0,9.
4. Способ получения биодоступной  -кристаллической формы цефуроксимаксетила по п.1, отличающийся тем, что цефуроксимаксетил в -кристаллической формы цефуроксимаксетила по п.1, отличающийся тем, что цефуроксимаксетил в  -кристаллической форме или по существу аморфной форме обрабатывают смесью воды и смешивающегося с водой органического растворителя в весовом отношении от 100 : 0 до 0 : 100 при температуре 20 – 100oC в течение промежутка времени от нескольких минут до нескольких часов, с последующим охлаждением и выделением кристаллического соединения. -кристаллической форме или по существу аморфной форме обрабатывают смесью воды и смешивающегося с водой органического растворителя в весовом отношении от 100 : 0 до 0 : 100 при температуре 20 – 100oC в течение промежутка времени от нескольких минут до нескольких часов, с последующим охлаждением и выделением кристаллического соединения.
РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 03.08.2002
Извещение опубликовано: 20.11.2004 БИ: 32/2004
|
||||||||||||||||||||||||||
