Патент на изобретение №2274635
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ТЕРБИНАФИНА ИЛИ ЕГО ГИДРОХЛОРИДА
(57) Реферат:
Изобретение относится к химии аллиламинов, а именно к способу получения тербинафина или его гидрохлорида. Способ включает взаимодействие избытка N-метил-нафт-1-илметиламина с 1-галоген-6,6-диметилгептен-2-ен-4-ином в воде или в водном растворе неорганического основания с последующей, при необходимости, обработкой полученного продукта соляной кислотой. Как правило, в качестве исходного реагента используют как 1-бром-6,6-диметилгепт-2-ен-4-ин, так и 1-хлор-6,6-диметилгепт-2-ен-4-ин. Обычно используют 5-50% мольный избыток N-метил-нафт-1-илметиламина в случае использования неорганического основания. Способ позволяет повысить выход целевого соединения, упростить процесс, а также расширить сырьевую базу использованием более дешевого алкилирующего агента – 1-хлор-6,6-диметилгепт-2-ен-4-ина. 2 з.п. ф-лы.
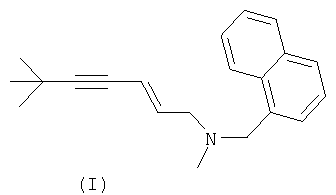
Изобретение относится к химии аллиламинов, а именно к способу получения (E)-N-(6,6-диметилгепт-2-ен-4-инил)-N-метил-нафт-1-илметиламина (I) (тербинафина). Тербинафин гидрохлорид – эффективный антимикотический препарат нового поколения, применение которого позволяет полностью излечивать грибковые заболевания без побочных явлений. К настоящему времени известно несколько методов получения тербинафина. Так, восстановлением N-(6,6-диметил-2,4-гептадиинил)-N-метил-нафт-1-илметиламина диизобутилалюминий гидридом образуется тербинафин с выходом 46% после хроматографического выделения (Европейский патент 0024587, Chem. Abstr., 1981, v.95, 169006d; A.Stutz and G.Petranyi, J. Med. Chem., 1984, v.27, p.1539-1543, A.Stutz, and W.Granitzer, and S.Roth, Tetrahedron, 1985, v.41, p.5685-5696). Тербинафин также может быть получен восстановительным аминированием из (E)-6,6-диметил-гепт-2-ен-4-ин-1-аля и N-метил-нафт-1-илметиламина (Европейский патент 0024587, Chem. Abstr., 1981, v.95, 169006d). Однако применение пожароопасных и дорогостоящих элементоорганических восстановителей затрудняет широкое использование данных способов для получения тербинафина. Конденсация N-метил-N-(3-галогенпроп-2-енил)-нафт-1-илметиламина (III) с элементоорганическими (олово, бор) производными трет-бутилацетилена в присутствии гомогенных палладиевых катализаторов позволяет получить тербинафин с выходом 87-98% (D.E.Radisill, and L.A.Castonguay, and J.K.Still, Tetrahedron Lett, 1988, v.29, p.1509-1512; C.H.Oh, and S.H.Jung, Tetrahedron Lett, 2000, v.41, p.8513-8516; M.Alami, and F.Ferri, and Y.Gaslain, Tetrahedron Lett, 1996, v.37, p.57-58; M.Alami, and B.Crousse, and F.Ferri, J. Organomet. Chem., 2001, v.624, p.114-123; Европейский патент 0421302; Chem. Abstr., 1991, v.115, 48409k). Практическое использование этого способа затруднено из-за высокой стоимости катализаторов и исходных элементоорганических соединений. Известен способ получения тербинафина алкилированием N-метил-нафт-1-илметиламина 1-бром-6,6-диметилгепт-2-ен-4-ином (в виде смеси Е- и Z-изомеров, соотношение 3:1) (P.D.Croce, and R.Ferraccioli, and C.L.Rosa, Gazz. Chim. Ital., 1996, v.126, p.107-110). Конденсацию осуществляют в толуоле при комнатной температуре в течение 16-24 часов в присутствии твердого карбоната калия и катализатора межфазного переноса – тетрабутиламмоний бромида. Однако для очистки целевого соединения (в том числе и катализатора межфазного переноса) требуется колоночная хроматография. Наиболее близким к предлагаемому является способ получения тербинафина алкилированием N-метил-нафт-1-илметиламина 1-бром-6,6-диметилгепт-2-ен-4-ином (в виде смеси Е- и Z-изомеров, соотношение 3:1) в диметилформамиде (Европейский патент 0024587; Chem. Abstr., 1981, v.95, 169006d). Выход целевого соединения составляет 43,5%. Так, 601 г (3 моля) 1-бром-6,6-диметилгепт-2-ен-4-ина (смесь Е- и Z-изомеров, соотношение 3:1) добавляют при охлаждении льдом к смеси 536,7 г (3,13 моля) N-метил-нафт-1-илметиламина, 332 г (3,13 моля) карбоната натрия в 3 л диметилформамида (высушен над молекулярными ситами) и смесь перемешивают ночь при комнатной температуре. Растворитель отгоняют в вакууме, остаток распределяют между водой и эфиром. Органический слой промывают 2% раствором винной кислоты, насыщенным раствором бикарбоната натрия, сушат сульфатом натрия, эфир отгоняют. Остаток наносят на 1,5 кг силикагеля и промывают смесью толуол/этилацетат (4/1). Растворители отгоняют, вязкий остаток (633,4 г) растворяют в этаноле, добавляют эквимолярное количество хлороводорода, растворенного в этаноле. Растворитель отгоняют, кристаллический остаток растворяют в 1,2 л горячего изопропанола, добавляют 4 л эфира. Осадок фильтруют, промывают смесью изопропанол/эфир (1/1). После перекристаллизации из смеси изопропанол/эфир получают 427,9 г тербинафина гидрохлорида (в виде Е-изомера) (выход 43,5%). К недостаткам известного метода можно отнести невысокий выход и необходимость в сложном выделении целевого соединения из реакционной смеси с использованием значительного количества тщательно высушенных различных растворителей и нехимических операций (отгонка, растворение, промывки и т.д.). Настоящее изобретение направлено на повышение выхода целевого соединения, упрощение процесса (сокращение количества нехимических операций, уменьшение количества растворителей), а также на расширение сырьевой базы (использование более дешевого алкилирующего агента – 1-хлор-6,6-диметилгепт-2-ен-4-ина). Сущность предлагаемого изобретения состоит в способе получения тербинафина взаимодействием N-метил-нафт-1-илметиламина с 1-галоген-6,6-диметилгепт-2-ен-4-ином в воде или в водном растворе неорганического основания с использованием избытка исходного N-метил-нафт-1-илметиламина, что позволяет значительно упростить выделение целевого соединения. На синтез тербинафина не оказывает заметного влияния добавление дополнительного органического водонерастворимого растворителя, в качестве которого могут выступать углеводороды, простые эфиры и др. Для связывания выделяющегося в ходе реакции галогеноводорода используют как неорганические основания, так и соответствующий мольный избыток N-метил-нафт-1-илметиламина. В качестве неорганических оснований используют водные растворы гидроксидов натрия или калия, карбоната калия, причем концентрация неорганического основания в водных растворах не оказывает существенного влияния на процесс получения тербинафина. При использовании неорганических оснований в качестве акцептора галогеноводорода для достижения полного расходования алкилирующего агента используют 5-50% мольный избыток N-метил-нафт-1-илметиламина, при этом достигается количественный выход N-(6,6-диметилгепт-2-ен-4-инил)-N-метил-нафт-1-илметиламина, в котором содержание E-изомера (тербинафина) соответствует количеству E-изомера в исходном 1-галоген-6,6-диметилгепт-2-ен-4-ине. Алкилирующий агент (1-галоген-6,6-диметилгепт-2-ен-4-ин) используют в виде смеси геометрических изомеров (Е- и Z-), с содержанием E-изомера не менее 75%, при этом выделение тербинафина гидрохлорида из реакционной смеси осуществляют кристаллизацией в присутствии водного раствора соляной кислоты. Заключительную очистку тербинафина гидрохлорида осуществляют стандартными операциями (промывка, перекристаллизация), при этом потери целевого соединения не превышают 5-10%. Природа галогена (бром или хлор) в 1-галоген-6,6-диметилгепт-2-ен-4-ине не оказывает существенного влияния на выход целевого соединения. Температурные параметры процесса не оказывают существенного влияния на выход целевого соединения в интервале от 0 до 100°С. Сущность данного изобретения иллюстрируется, но не ограничивается следующими примерами. Пример 1. Смесь 20 мл 15% водного раствора гидроксида натрия, 14,4 г (0,084 моль) N-метил-нафт-1-илметиламина и 11,0 г (0,07 моль) (E)-1-хлор-6,6-диметил-2-гепт-2-ен-4-ина (содержит 95% E-изомера) перемешивают при 70°С 5 часов (по данным ВЭЖХ исходное хлорпроизводное отсутствует). Затем при охлаждении водой добавляют по каплям 4,0 мл соляной кислоты, осадок отделяют, моют водой, сушат. Получают 22,5 г бледно-кремового вещества (по данным ВЭЖХ – 92% (I) и 6% (II)). Перекристаллизовывают из изо-пропанола. Получают 20,6 г (E)-N-(6,6-диметилгепт-2-ен-4-инил)-N-метил-нафт-1-илметиламина гидрохлорида, выход 94,5%, т.пл. 205°С, содержание (E)-изомера более 99%. Спектр ЯМР 1H (в виде основания, CDCl3, Пример 2. Смесь 26,7 г (0,156 моль) N-метил-нафт-1-илметиламина, 10,5 г (0,067 моль) 1-хлор-6,6-диметил-2-гепт-2-ен-4-ина (содержит 85% Е-изомера) и 50 мл воды перемешивают при комнатной температуре 15-20 часов (до отсутствия по данным ВЭЖХ исходного хлорпроизводного). Добавляют 100 мл диэтилового эфира, органический слой отделяют, промывают водой. При перемешивании и охлаждении к эфирному раствору добавляют 20 мл соляной кислоты (1:3). Осадок отделяют фильтрованием, промывают эфиром, сушат, после перекристаллизации из изо-пропанола получают 16,8 г (E)-N-(6,6-диметилгепт-2-ен-4-инил)-N-метил-нафт-1-илметиламина гидрохлорида, выход 90%, содержание (E)-изомера более 99%. Пример 3. К раствору 13,7 г (0,08 моль) N-метил-нафт-1-илметиламина в 20 мл диэтилового эфира добавляют 13,5 г (0,067 моль) 1-бром-6,6-диметил-2-гепт-2-ен-4-ина (содержит 75% E-изомера). Перемешивают 1 час при 40°С и добавляют 20 мл 15% водного раствора гидроксида натрия. Энергично перемешивают 10-12 часов при 40°С (до отсутствия по данным ВЭЖХ исходного хлорпроизводного). Далее, как в примере 2, получают 14,8 г (E)-N-(6,6-диметилгепт-2-ен-4-инил)-N-метил-нафт-1-илметиламина гидрохлорида, выход 89%, содержание (Е)-изомера более 99%. Спектральные параметры и физико-химические константы тербинафина в приведенных выше примерах идентичны. Таким образом, предлагаемый способ легко реализуется в промышленных условиях и позволяет получать тербинафин гидрохлорид с высоким выходом. Источники информации 1. Европейский патент 0024587; Chem. Abstr., 1981, v.95, 169006d. 2. A.Stutz and G.Petranyi, J. Med. Chem., 1984, v.27, p.1539-1543. 3. A.Stutz, and W.Granitzer, and S.Roth, Tetrahedron, 1985, v.41, p.5685-5696. 4. D.E.Radisill, and L.A.Castonguay, and J.K.Still, Tetrahedron Lett, 1988, v.29, p.1509-1512. 5. C.H.Oh, and S.H.Jung, Tetrahedron Lett, 2000, v.41, p.8513-8516. 6. M.Alami, and F.Ferri, and Y.Gaslain, Tetrahedron Lett, 1996, v.37, p.57-58. 7. M.Alami, and В.Crousse, and F.Ferri, J. Organomet. Chem., 2001, v.624, p.114-123. 8. Европейский патент 0421302; Chem. Abstr., 1991, v.115, 48409k. 9. P.D.Croce, and R.Ferraccioli, and C.L.Rosa, Gazz. Chim. Ital., 1996, v.126, p.107-110.
Формула изобретения
1. Способ получения тербинафина или его гидрохлорида взаимодействием N-метил-нафт-1-илметиламина с 1-галоген-6,6-диметилгепт-2-ен-4-ином с последующей при необходимости обработкой полученного продукта соляной кислотой, отличающийся тем, что взаимодействие проводят в воде или в водном растворе неорганического основания с использованием избытка исходного N-метил-нафт-1-илметиламина. 2. Способ по п.1, отличающийся тем, что в качестве исходного реагента используют как 1-бром-6,6-диметилгепт-2-ен-4-ин, так и 1-хлор-6,6-диметилгепт-2-ен-4-ин. 3. Способ по п.1, отличающийся тем, что используют 5-50%-ный мольный избыток N-метил-нафт-1-илметиламина в случае использования неорганического основания.
|
||||||||||||||||||||||||||

 , м.д. J, Гц,): 1,32 с (9Н, С(СН3)3), 2,29 с (3Н, СН3N), 3,2 дд (J 6,4 Гц и 1,5 Гц, 2Н, NCH2CH=), 3,96 с (2Н, NCH2C10H7), 5,76 дт (J 15,8 Гц и 1,5 Гц, 1Н, СН=СН-С=), 6,23 дт (J 15,8 Гц и 6,4 Гц, 1Н, СН2-СН=СН), 7,44-7,61 м (4Н, аром. Н), 7,83-7,91 м (2Н, аром. Н), 8,33-8,36 м (1Н, аром. Н).
, м.д. J, Гц,): 1,32 с (9Н, С(СН3)3), 2,29 с (3Н, СН3N), 3,2 дд (J 6,4 Гц и 1,5 Гц, 2Н, NCH2CH=), 3,96 с (2Н, NCH2C10H7), 5,76 дт (J 15,8 Гц и 1,5 Гц, 1Н, СН=СН-С=), 6,23 дт (J 15,8 Гц и 6,4 Гц, 1Н, СН2-СН=СН), 7,44-7,61 м (4Н, аром. Н), 7,83-7,91 м (2Н, аром. Н), 8,33-8,36 м (1Н, аром. Н).