Патент на изобретение №2155748
|
||||||||||||||||||||||||||
(54) ПРОИЗВОДНЫЕ ЦИКЛОГЕКСАДИЕНА, СМЕСЬ ИХ ИЗОМЕРОВ ИЛИ ОТДЕЛЬНЫЕ ИЗОМЕРЫ И ИХ СОЛИ И ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ С ИЗБИРАТЕЛЬНЫМ МОДУЛИРУЮЩИМ ДЕЙСТВИЕМ НА ЗАВИСИМЫЕ ОТ КАЛЬЦИЯ КАЛИЕВЫЕ КАНАЛЬЦЫ ВЫСОКОЙ ПРОВОДИМОСТИ
(57) Реферат: Описываются новые производные циклогексадиена общей формулы Ia или Ib, где А – фенил или нефтил, незамещенный или замещенный 1 – 3 одинаковыми или различными остатками из группы, включающей нитро, галоид, трифторметил, неразветвленным или разветвленным алкилом с 1 – 6 атомами углерода, R1 – водород или неразветвленный или разветвленный алкил с 1 – 8 атомами углерода, R2 и R3 – одинаковы или различны и означают водород или неразветвленный или разветвленный алкил с 1 – 6 атомами углерода, D – неразветвленный или разветвленный алкоксикарбонил с 1 – 8 атомами углерода, смесь их изомеров или отдельные изомеры и их соли. Вышеуказанные новые соединения могут представлять собой активное начало фармацевтической композиции с избирательным модулирующим действием на зависимые от кальция калиевые канальцы высокой проводимости. Описывается также фармацевтическая композиция. 2 c. и 2 з.п. ф-лы, 3 табл. 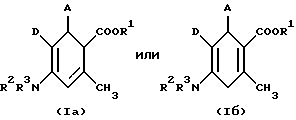
Изобретение относится к новым химическим веществам с ценными биологическими свойствами, в частности к производным циклогексадиена, а также к фармацевтической композиции на их основе. Известны производные циклогексадиена, например сложный эфир 3,6-цикло-гексадиен-2-фенил-1,3-дикарбоновой кислоты, обладающие ингибирующим сокращение мышц действием (см. Chem. Pharm. Bull., 39 (II), стр. 2915 – 23, 1991 г. ). Задачей изобретения является разработка производных циклогексадиена, обладающих избирательным модулирующим действием на зависимые от кальция калиевые канальцы высокой проводимости. Поставленная задача решается предлагаемыми производными циклогексадиена общих формул (Iа) или (Iб) 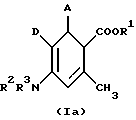 или 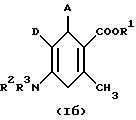 где A – фенил или нафтил, незамещенный или замещенный 1 – 3 одинаковыми или различными остатками из группы, включающей нитро, галоид, трифторметил, неразветвленным или разветвленным алкилом с 1-6 атомами углерода, R1– водород или неразветвленный или разветвленный алкил с 1-8 атомами углерода, R2 и R3 одинаковы или различны и означают водород или неразветвленный или разветвленный алкил с 1-6 атомами углерода, D – неразветвленный или разветвленный алкоксикарбонил с 1-8 атомами углерода, смесью их изомеров или отдельными изомерами и их солями. В качестве солей предпочитают физиологически невредные соли. Предпочтительными являются, в общем, соли предлагаемых соединений с неорганическими или органическими кислотами. Предпочитаются соли с неорганическими кислотами, такими как, например, соляная кислота, бромистоводородная кислота, фосфорная кислота или серная кислота, или соли с органическими карбоновыми или сульфоновыми кислотами, такими как, например, уксусная кислота, малеиновая кислота, фумаровая кислота, яблочная кислота, лимонная кислота, винная кислота, молочная кислота, бензойная кислота или метансульфокислота, этансульфокислота, фенилсульфокислота, толуолсульфокислота или нафталиндисульфокислота. Предлагаемые соединения могут иметься в виде стереоизомеров, которые представляют собой прямую форму и обратную форму (энантиомеры) или не являются таковыми (диастереомеры). Изобретение относится к антиподам, а также к рацемическим формам и смесям диастереомеров. Рацемические формы, а также диастереомеры известным образом можно разделять на чистые стереоизомеры. Предпочтительными являются соединения общих формул (Iа) или (Iб), где A – фенил или нафтил, незамещенные или замещенные 1 – 3 одинаковыми или различными остатками из группы, включающей нитро, фтор, хлор, бром, йод, трифторметил, неразветвленным или разветвленным алкилом с 1-4 атомами углерода, R1 – водород или неразветвленный или разветвленный алкил с 1-6 атомами углерода, R2 и R3 – одинаковы или различны и означают водород или неразветвленный или разветвленный алкил с 1-4 атомами углерода, D – неразветвленный или разветвленный алкоксикарбонил с 1 – 6 атомами углерода, смесь их изомеров или отдельные изомеры и их соли. Особенно предпочтительными являются соединения общих формул (Iа) или (Iб), где A – фенил, незамещенный или замещенный 1 – 3 одинаковыми или различными остатками из группы, включающей нитро, фтор, хлор, бром, йод, трифторметил, метил, R1 – водород или неразветвленный или разветвленный алкил с 1 – 4 атомами углерода, R2 и R3 одинаковы или различны и означают водород или неразветвленный или разветвленный алкил с 1-3 атомами углерода, D – неразветвленный или разветвленный алкоксикарбонил с 1-4 атомами углерода, смесь их изомеров или отдельные изомеры и их соли. Предлагаемые соединения общих формул (Iа) или (Iб) можно получать, например, следующим путем: Соединения общей формулы (II) 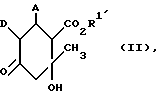 где A и D имеют вышеукзанное значение, R1′ имеет вышеуказанное значение R1, но не означает водород, на первой стадии путем взаимодействия с аминами общей формулы (III) R2R3NH, (III) где R2 и R3 имеют вышеуказанное значение, в среде инертного растворителя и в присутствии вспомогательного вещества переводят в соединения общей формулы (IV) 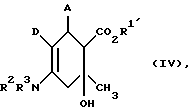 где A, D, R1, R2 и R3 имеют вышеуказанное значение, а получаемые при этом соединения на второй стадии реагируют в среде инертного растворителя и, при необходимости, в присутствии основания и в присутствии водоотделяющего вспомогательного вещества, и получаемые при этом изомеры с двойными связями выделяют путем хроматографии и/или кристаллизации, и если R1 = H, то сложный эфир обычными приемами подвергают гидролизу, и если R2 и/или R3  H, то осуществляют алкилирование или ацилирование.
Данный способ поясняется схемой 1 (см. в конце описания).
В качестве растворителей для обеих стадий пригодны любые инертные органические растворители, не меняющиеся в условиях реакции. Предпочтительными растворителями являются спирты, такие как метанол, этанол, пропанол или изопропанол, простые эфиры, такие как диэтиловый эфир, диоксан, тетрагидрофуран, гликольдиметиловый эфир или диэтиленгликольдиметиловый эфир, ацетонитрил, амиды, такие как триамид гексаметилфосфорной кислоты или диметилформамид, галогенированные углеводороды, такие как, хлористый метилен, четыреххлористый углерод, углеводороды, такие как бензол или толуол, или пиридин. Можно также применять смеси приведенных растворителей. Особенно предпочтительными растворителями являются толуол для первой стадии реакции и пиридин для второй стадии.
Амин в общем берут в количестве 1 – 5 моль, предпочтительно 1 – 2 моль в пересчете на 1 моль соединений общей формулы (II).
В качестве вспомогательных веществ для реакции соединений общей формулы (II) в общем пригодны органические сульфокислоты, такие как п-толуолсульфокислота, или безводные минеральные кислоты, такие как фосфорная кислота или серная кислота. Предпочтительной является гидрат п-толуолсульфокислоты.
Вспомогательное вещество в общем берут в количестве 0,1 – 1 моль, предпочтительно 0,1 – 0,2 моль, в пересчете на 1 моль соединений общих формул (II) и (III).
Реакцию с аминами общей формулы (III) в общем проводят при температурах между 10oC и 150oC, предпочтительно между 40oC и 80oC.
Реакции можно осуществлять как при атмосферном давлении, так и при повышенном или пониженном давлении (например, при 0,5 – 3 бар). В общем работают при атмосферном давлении.
В качестве вспомогательного вещества для реакции с соединениями формулы (IV) пригодны карбодиимиды, такие как, например, диизопропилкарбодиимид, дициклогексилкарбодиимид или гидрохлорид N-(3-диметиламинопропил)-N’-этилкарбодиимида, или карбонильные соединения, такие как, например, карбонилдиимидазол, или соединения 1,2-оксазолия, такие как, например, 2-этил-5-фенил-1,2-оксазолий-3-сульфонат или ангидрид пропанфосфоновой кислоты или изобутилхлорформат или гексафторфосфат бензотриазолилокси-трис-(диметиламино)фосфония, или амид сложного дифенилового эфира фосфорной кислоты, или хлорид метансульфоновой кислоты, или тионилхлорид, ангидрид трифторуксусной кислоты, при необходимости в присутствии оснований, таких как, например, триэтиламин, пиридин или N-этилморфолин или N-метилпиперидин или дициклогексилкарбодиимид и N-оксисукцинимид, гидроокиси алкоксикарбонилсульфонилтриалкиламмония, смеси ацетангидрида с ацетатом натрия и фосфорной кислотой, минеральные кислоты, такие как, например, серная кислота или органические сульфоновые кислоты, такие как, например, п-толуолсульфокислота. Преимущественно применяется тионилхлорид в присутствии пиридина.
Реакцию соединений общей формулы (IV) в общем проводят при температурах между 0oC и 150oC, предпочтительно между 30oC и 80oC.
Реакции можно осуществлять как при атмосферном давлении, так и при повышенном или пониженном давлении (например, при 0,5 – 3 бар). В общем работают при атмосферном давлении.
В качестве растворителей для алкилирования тоже пригодны обычные органические растворители, не меняющиеся в условиях реакции. Предпочтительными растворителями являются простые эфиры, такие как, например, диэтиловый эфир, диоксан, тетрагидрофуран, простой гликольдиметиловый эфир, углеводороды, как, например, бензол, толуол, ксилол, гексан, циклогексан, нефтяные фракции, галогенированные углеводороды, такие как, например, дихлорметан, трихлорметан, тетрахлорметан, дихлорэтилен, трихлорэтилен или хлорбензол, простой эфир уксусной кислоты, триэтиламин, пиридин, диметилсульфоксид, диметилформамид, триамид гексаметилфосфорной кислоты, ацетонитрил, ацетон или нитрометан. Можно также применять смеси приведенных растворителей. Предпочтительным растворителем является диметилформамид.
В качестве оснований в общем пригодны гидриды или алкоголяты щелочного металла, например гидрид натрия или трет.бутилат калия, циклические амины, например пиперидин, диметиламинопиридин или алкиламины с 1-4 атомами углерода, например триэтиламин. Предпочтительным является гидрид натрия.
Температуры реакции можно варьировать в широком диапазоне. В общем работают при температурах между +10oC и +150oC, предпочтительно между +20oC и +100oC, в частности при комнатной температуре.
Алкилирование в среде вышеприведенных растворителей осуществляют при температурах от 0oC до +150oC, предпочтительно при комнатной температуре до +100oC.
Реакции можно осуществлять как при атмосферном давлении, так и при повышенном или пониженном давлении (например, при 0,5 – 3 бар). В общем работают при атмосферном давлении.
Основание в общем применяют в количестве 1 – 5 моль, предпочтительно 1 – 2 моль, в пересчете на 1 моль подвергаемого алкилированию соединения.
В качестве оснований для ацилирования пригодны неорганические или органические основания. Предпочтительными основаниями являются, например, гидроокиси щелочного металла, как, например, гидроокись натрия или калия, гидроокиси щелочноземельного металла, как, например, гидроокись бария, карбонаты щелочного металла, как, например, карбонат натрия или калия, карбонаты щелочноземельного металла, как, например, карбонат кальция, или органические амины, такие как, например, триалкиламины с 1-6 атомами углерода в аминой части, как, например, триэтиламин, или гетероциклы, как пиридин, метилпиперидин, пиперидин или морфолин. Особенно предпочтительным является триэтиламин.
В качестве растворителей для ацилирования также пригодны стандартные органические растворители, не меняющиеся в условиях реакции. Предпочтительными растворителями являются простые эфиры, такие как диэтиловый эфир, диоксан, тетрагидрофуран, гликольдиметиловый эфир, углеводороды, такие как бензол, толуол, ксилол, гексан, циклогексан или нефтяные фракции, галогенированные углеводороды, такие как дихлорметан, трихлорметан, тетрахлорметан, дихлорэтилен, трихлорэтилен или хлорбензол, сложный этиловый эфир уксусной кислоты, или триэтиламин, пиридин, диметилсульфоксид, диметилформамид, триамид гексаметилфосфорной кислоты, ацетонитрил, ацетон или нитрометан. Можно также применять смеси приведенных растворителей или же соответствующий агент ацилирования можно также использовать в качестве растворителя. Предпочтительными растворителями являются ацетангидрид и пиридин.
Ацилирование в общем осуществляют в температурном диапазоне от 0oC до +120oC, предпочтительно от +30oC до +90oC, и при атмосферном давлении.
Омыление сложных эфиров карбоновой кислоты осуществляют известными приемами путем обработки стандартными основаниями в среде инертных растворителей.
В качестве оснований для омыления пригодны стандартные для этой реакции неорганические основания. Предпочтительными являются, например, гидроокиси щелочных или щелочноземельных металлов, такие как, например, гидроокись натрия, калия или бария, или карбонаты щелочного металла, как, например, карбонат натрия или калия, или бикарбонат натрия. Особенно предпочтительными являются гидроокись натрия или калия.
В качестве растворителей для омыления пригодны вода или стандартные для этой реакции органические растворители. Предпочтительными являются, например, спирты, как метанол, этанол, пропанол, изопропанол или бутанол, простые эфиры, как тетрагидрофуран или диоксан, диметилформамид или диметилсульфоксид. Особенно предпочтительными являются спирты, как метанол, этанол, пропанол или изопропанол. Также возможно применение смесей приведенных растворителей.
Омыление в общем осуществляют в температурном диапазоне от 0oC до +100oC, предпочтительно от +20oC до +80oC.
В общем омыление осуществляют при атмосферном давлении. Можно, однако, также работать при пониженном или повышенном давлении (например, от 0,5 до 5 бар).
Чистые энантиомеры получают, например, в результате разделения известным методом смесей диастереомеров соединений общих формул (Iа) или (Iб), где R1 означает оптически активный остаток сложного эфира, после чего либо непосредственно осуществляют переэтерификацию, либо сначала получают хиральные карбоновые кислоты, которые затем путем этерификации переводят в чистые энантиомерные соединения.
Разделение диастереомеров в общем осуществляют фракционной кристаллизацией, колоночной хроматографией или распределением по Крейгу. В каждом конкретном случае необходимо определить, какой метод является оптимальным для данной цели. Иногда также целесообразно использовать комбинацию указанных методов. Особенно пригодным является разделение кристаллизацией или распределением по Крейгу или же их комбинация.
Чистые энантиомерные соединения также доступны путем хроматографии рацемических сложных эфиров на хиральных фазах.
Амины общей формулы (III) известны. Соединения общей формулы (IV) известны или их можно получать, например, вышеописанным методом.
Соединения общей формулы (II) известны или их можно получать путем взаимодействия H, то осуществляют алкилирование или ацилирование.
Данный способ поясняется схемой 1 (см. в конце описания).
В качестве растворителей для обеих стадий пригодны любые инертные органические растворители, не меняющиеся в условиях реакции. Предпочтительными растворителями являются спирты, такие как метанол, этанол, пропанол или изопропанол, простые эфиры, такие как диэтиловый эфир, диоксан, тетрагидрофуран, гликольдиметиловый эфир или диэтиленгликольдиметиловый эфир, ацетонитрил, амиды, такие как триамид гексаметилфосфорной кислоты или диметилформамид, галогенированные углеводороды, такие как, хлористый метилен, четыреххлористый углерод, углеводороды, такие как бензол или толуол, или пиридин. Можно также применять смеси приведенных растворителей. Особенно предпочтительными растворителями являются толуол для первой стадии реакции и пиридин для второй стадии.
Амин в общем берут в количестве 1 – 5 моль, предпочтительно 1 – 2 моль в пересчете на 1 моль соединений общей формулы (II).
В качестве вспомогательных веществ для реакции соединений общей формулы (II) в общем пригодны органические сульфокислоты, такие как п-толуолсульфокислота, или безводные минеральные кислоты, такие как фосфорная кислота или серная кислота. Предпочтительной является гидрат п-толуолсульфокислоты.
Вспомогательное вещество в общем берут в количестве 0,1 – 1 моль, предпочтительно 0,1 – 0,2 моль, в пересчете на 1 моль соединений общих формул (II) и (III).
Реакцию с аминами общей формулы (III) в общем проводят при температурах между 10oC и 150oC, предпочтительно между 40oC и 80oC.
Реакции можно осуществлять как при атмосферном давлении, так и при повышенном или пониженном давлении (например, при 0,5 – 3 бар). В общем работают при атмосферном давлении.
В качестве вспомогательного вещества для реакции с соединениями формулы (IV) пригодны карбодиимиды, такие как, например, диизопропилкарбодиимид, дициклогексилкарбодиимид или гидрохлорид N-(3-диметиламинопропил)-N’-этилкарбодиимида, или карбонильные соединения, такие как, например, карбонилдиимидазол, или соединения 1,2-оксазолия, такие как, например, 2-этил-5-фенил-1,2-оксазолий-3-сульфонат или ангидрид пропанфосфоновой кислоты или изобутилхлорформат или гексафторфосфат бензотриазолилокси-трис-(диметиламино)фосфония, или амид сложного дифенилового эфира фосфорной кислоты, или хлорид метансульфоновой кислоты, или тионилхлорид, ангидрид трифторуксусной кислоты, при необходимости в присутствии оснований, таких как, например, триэтиламин, пиридин или N-этилморфолин или N-метилпиперидин или дициклогексилкарбодиимид и N-оксисукцинимид, гидроокиси алкоксикарбонилсульфонилтриалкиламмония, смеси ацетангидрида с ацетатом натрия и фосфорной кислотой, минеральные кислоты, такие как, например, серная кислота или органические сульфоновые кислоты, такие как, например, п-толуолсульфокислота. Преимущественно применяется тионилхлорид в присутствии пиридина.
Реакцию соединений общей формулы (IV) в общем проводят при температурах между 0oC и 150oC, предпочтительно между 30oC и 80oC.
Реакции можно осуществлять как при атмосферном давлении, так и при повышенном или пониженном давлении (например, при 0,5 – 3 бар). В общем работают при атмосферном давлении.
В качестве растворителей для алкилирования тоже пригодны обычные органические растворители, не меняющиеся в условиях реакции. Предпочтительными растворителями являются простые эфиры, такие как, например, диэтиловый эфир, диоксан, тетрагидрофуран, простой гликольдиметиловый эфир, углеводороды, как, например, бензол, толуол, ксилол, гексан, циклогексан, нефтяные фракции, галогенированные углеводороды, такие как, например, дихлорметан, трихлорметан, тетрахлорметан, дихлорэтилен, трихлорэтилен или хлорбензол, простой эфир уксусной кислоты, триэтиламин, пиридин, диметилсульфоксид, диметилформамид, триамид гексаметилфосфорной кислоты, ацетонитрил, ацетон или нитрометан. Можно также применять смеси приведенных растворителей. Предпочтительным растворителем является диметилформамид.
В качестве оснований в общем пригодны гидриды или алкоголяты щелочного металла, например гидрид натрия или трет.бутилат калия, циклические амины, например пиперидин, диметиламинопиридин или алкиламины с 1-4 атомами углерода, например триэтиламин. Предпочтительным является гидрид натрия.
Температуры реакции можно варьировать в широком диапазоне. В общем работают при температурах между +10oC и +150oC, предпочтительно между +20oC и +100oC, в частности при комнатной температуре.
Алкилирование в среде вышеприведенных растворителей осуществляют при температурах от 0oC до +150oC, предпочтительно при комнатной температуре до +100oC.
Реакции можно осуществлять как при атмосферном давлении, так и при повышенном или пониженном давлении (например, при 0,5 – 3 бар). В общем работают при атмосферном давлении.
Основание в общем применяют в количестве 1 – 5 моль, предпочтительно 1 – 2 моль, в пересчете на 1 моль подвергаемого алкилированию соединения.
В качестве оснований для ацилирования пригодны неорганические или органические основания. Предпочтительными основаниями являются, например, гидроокиси щелочного металла, как, например, гидроокись натрия или калия, гидроокиси щелочноземельного металла, как, например, гидроокись бария, карбонаты щелочного металла, как, например, карбонат натрия или калия, карбонаты щелочноземельного металла, как, например, карбонат кальция, или органические амины, такие как, например, триалкиламины с 1-6 атомами углерода в аминой части, как, например, триэтиламин, или гетероциклы, как пиридин, метилпиперидин, пиперидин или морфолин. Особенно предпочтительным является триэтиламин.
В качестве растворителей для ацилирования также пригодны стандартные органические растворители, не меняющиеся в условиях реакции. Предпочтительными растворителями являются простые эфиры, такие как диэтиловый эфир, диоксан, тетрагидрофуран, гликольдиметиловый эфир, углеводороды, такие как бензол, толуол, ксилол, гексан, циклогексан или нефтяные фракции, галогенированные углеводороды, такие как дихлорметан, трихлорметан, тетрахлорметан, дихлорэтилен, трихлорэтилен или хлорбензол, сложный этиловый эфир уксусной кислоты, или триэтиламин, пиридин, диметилсульфоксид, диметилформамид, триамид гексаметилфосфорной кислоты, ацетонитрил, ацетон или нитрометан. Можно также применять смеси приведенных растворителей или же соответствующий агент ацилирования можно также использовать в качестве растворителя. Предпочтительными растворителями являются ацетангидрид и пиридин.
Ацилирование в общем осуществляют в температурном диапазоне от 0oC до +120oC, предпочтительно от +30oC до +90oC, и при атмосферном давлении.
Омыление сложных эфиров карбоновой кислоты осуществляют известными приемами путем обработки стандартными основаниями в среде инертных растворителей.
В качестве оснований для омыления пригодны стандартные для этой реакции неорганические основания. Предпочтительными являются, например, гидроокиси щелочных или щелочноземельных металлов, такие как, например, гидроокись натрия, калия или бария, или карбонаты щелочного металла, как, например, карбонат натрия или калия, или бикарбонат натрия. Особенно предпочтительными являются гидроокись натрия или калия.
В качестве растворителей для омыления пригодны вода или стандартные для этой реакции органические растворители. Предпочтительными являются, например, спирты, как метанол, этанол, пропанол, изопропанол или бутанол, простые эфиры, как тетрагидрофуран или диоксан, диметилформамид или диметилсульфоксид. Особенно предпочтительными являются спирты, как метанол, этанол, пропанол или изопропанол. Также возможно применение смесей приведенных растворителей.
Омыление в общем осуществляют в температурном диапазоне от 0oC до +100oC, предпочтительно от +20oC до +80oC.
В общем омыление осуществляют при атмосферном давлении. Можно, однако, также работать при пониженном или повышенном давлении (например, от 0,5 до 5 бар).
Чистые энантиомеры получают, например, в результате разделения известным методом смесей диастереомеров соединений общих формул (Iа) или (Iб), где R1 означает оптически активный остаток сложного эфира, после чего либо непосредственно осуществляют переэтерификацию, либо сначала получают хиральные карбоновые кислоты, которые затем путем этерификации переводят в чистые энантиомерные соединения.
Разделение диастереомеров в общем осуществляют фракционной кристаллизацией, колоночной хроматографией или распределением по Крейгу. В каждом конкретном случае необходимо определить, какой метод является оптимальным для данной цели. Иногда также целесообразно использовать комбинацию указанных методов. Особенно пригодным является разделение кристаллизацией или распределением по Крейгу или же их комбинация.
Чистые энантиомерные соединения также доступны путем хроматографии рацемических сложных эфиров на хиральных фазах.
Амины общей формулы (III) известны. Соединения общей формулы (IV) известны или их можно получать, например, вышеописанным методом.
Соединения общей формулы (II) известны или их можно получать путем взаимодействияальдегидов общей формулы (V) A-CHO, (V) где A имеет вышеуказанное значение, с двумя эквивалентами соединений общей формулы (VI) H3C-CO-CH2-CO2R1′, (VI) где R1′ имеет вышеуказанное значение, в среде органического растворителя и в присутствии основания, такого как, напри мер, гидриды или алкоголяты щелочного металла, циклические амины, или алкиламины с 1-4 атомами углерода. Реакцию можно осуществлять как при атмосферном давлении, так и при пониженном или повышенном давлении (например, от 0,5 до 3 бар), и при температурах между +10oC и +150oC, предпочтительно между +20oC и +100oC, в частности при температуре кипения используемого растворителя. Соединения общих формул (V) и (VI) известны или их можно получать стандартными методами. Предлагаемые соединения общих формул (Iа) и (Iб) обладают неожиданным, ценным фармакологическим спектром действия, они обладают действием на церебральную систему, в частности они представляют собой модуляторы, обладающие селективностью в отношении зависящих от кальция калиевых канальцев высокой проводимости, в частности центральной нервной системы. На основе их фармакологических свойств их можно использовать для приготовления лекарственных средств для лечения дегенеративных заболеваний центральной нервной системы, в случае появления деменций, таких как, например, многоинфарктное слабоумие, первично дегенеративное слабоумие, пресенильное и старческое слабоумие (болезнь Альцгеймера), слабоумие в связи со СПИДом и других видов деменций, кроме того, для лечения болезни Паркинсона, бокового амиотрофического склероза, множественного склероза, а также серповидно-клеточной анемии. Кроме того, новые соединения пригодны для лечения функциональной слабости мозга в старости, мозгоорганического психосиндрома и расстройств памяти в старости. Они пригодны для профилактики и борьбы с последствиями нарушений мозгового кровообращения, таких как, например, церебральные ишемии, апоплексические удары, черепно-мозговые травмы и субарахноидальные кровоизлияния. Кроме того, они пригодны для лечения депрессий и психозов, например шизофрении, а также для лечения расстройств невроэндокринной секреции, секреции невротрансмиттеров и связанных с ними расстройств здоровья, таких как, например, мания, алкоголизм, злоупотребление наркотиками, болезненная страсть или болезненное отношение к еде. Дополнительными областями применения новых соединений являются лечение мигрени, расстройств сна, невропатий. К тому же, они пригодны в качестве болеутоляющих средств. Возможно применять новые соединения и для лечения расстройств иммунной системы, в частности пролиферации Т-лимфоцитов, и для воздействия на гладкую мускулатуру, в частности матки, мочевого пузыря и бронхиального тракта, и для лечения связанных с этим болезней, например астмы и недержания мочи, и для лечения повышенного кровяного давления, аритмии, ангины и диабета. На основе вышеуказанных данных дальнейшим объектом изобретения является фармацевтическая композиция с избирательным модулирующим зависящие от кальция калиевые канальцы действием, содержащая наряду по крайней мере, с одним инертным, нетоксичным, фармацевтически применяемым носителем, соединение вышеуказанных общих формул (Iа) или (Iб). Предлагаемая фармацевтическая композиция может представлять собой любой стандартный препарат. Активные начала формул (Iа) или (Iб) в такой композиции имеются в общем в концентрации 0,1 – 99,5 вес.%, предпочтительно 0,5 – 95 вес.% всей смеси. Кроме активных начал формул (Iа) или (Iб), фармацевтическая композиция может также содержать другие фармацевтически активные начала. Предлагаемую фармацевтическую композицию можно получать обычным образом по широкоизвестным методам, например измельчением и смешиванием. В общем для достижения желаемого результата активное начало или активные начала формул (Iа) или (Iб) преимущественно дают в общих количествах от примерно 0,01 мг/кг до примерно 100 мг/кг, предпочтительно в общем количестве от примерно 1 мг/кг до примерно 50 мг/кг веса тела в сутки, в случае необходимости в виде нескольких отдельных доз. Биологическую активность новых соединений формул (Iа) или (Iб) определяли следующим образом: Выделение 86рубидия из глиомных клеток C6-BU1 Опыты проводили с незначительными изменениями по методу, описанному Тас и др. (Neurosci. Let. 94, стр. 279 – 284, 1988). Для опытов используют глиомные клетки C6-BU1 крыс. По получаемым из сцинтилляции жидкости данным через базальное выделение рассчитывали вызванное иономицином повышение выделения, которое берут за 100%. Стимуляцию исследуемыми соединениями относили к этому значению. Исследуемые соединения и результаты опыта сведены в таблице 1 (см. в конце описания). Соединения согласно изобретению относятся к категории малотоксичных веществ. Нижеследующие примеры поясняют получение новых соединений формул (Iа) или (Iб). Исходные соединения Пример 1 Сложный диэтиловый эфир 4-окси-4-метил-2-(3-нитрофенил)-6-оксо-циклогексан-1,3-дикарбоновой кислоты 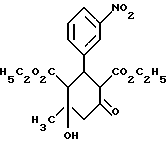 45,3 г (0,3 моль) 3-нитробензальдегида и 78 г (0,6 моль) сложного этилового эфира ацетоуксусной кислоты растворяют в 300 мл этанола и к раствору добавляют 6 мл пиперидина. Перемешивают в течение 24 часов при температуре 40oC. Осадившийся твердый материал отсасывают и перекристаллизуют из этанола. Получают 85,4 г целевого соединения (выход: 72% теории). Пример 2 Сложный диэтиловый эфир 6-окси-6-метил-4-метиламино-2-(3-нитрофенил)-циклогекс-3-ен-1,3-дикарбоновой кислоты 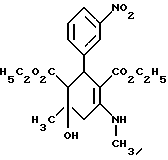 Вариант А: 3,9 г (10 ммоль) соединения примера 1 растворяют в 100 мл толуола и к раствору добавляют 0,2 г гидрата п-толуолсульфокислоты. Нагревают в течение 4 часов с обратным холодильником в водоотделяющих условиях и добавляют метиламин. Сгущают в вакууме и остаток перекристаллизуют из простого диизопропилового эфира. Получают 400 мг целевого соединения (выход: 10% теории). Вариант Б: 19,7 г (50 ммоль) соединения примера 1 растворяют в 200 мл этанола и к раствору добавляют 30 мл 11н. раствора метиламина в метаноле и 1 г гидрата п-толуолсульфокислоты. Перемешивают в течение 2 часов при температуре 60 – 65oC. После сгущения реакционной смеси остаток очищают путем хроматографии на 100 г силикагеля с применением метиленхлорида в качестве элюента. Элюат сгущают и перекристаллизуют из простого диизопропилового эфира. Получают 17,0 г целевого соединения (выход: 84% теории). Точка плавления: 112oC (простой диизопропиловый эфир) Целевые продукты Пример 3 Сложный диэтиловый эфир 4-метил-6-метиламино-2-(3-нитрофенил)-циклогекса-3,6-диен-1,3-дикарбоновой кислоты 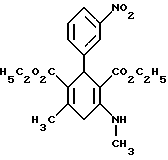 2,5 г (6,2 ммоль) соединения примера 2 подают в 30 мл пиридина, реакционную смесь нагревают до температуры 80oC и добавляют 0,95 г (80 ммоль) тионилхлорида. Эту температуру поддерживают в течение 20 минут, после чего в течение еще 20 минут нагревают с обратным холодильником. Сгущают и остаток подают в смесь метиленхлорида и воды. Органическую фазу отделяют, сушат над сульфатом магния и сгущают. В результате очисткой путем хроматографии на силикагеле с применением в качестве элюента смеси метиленхлорида и сложного этилового эфира уксусной кислоты в соотношении 20:1 и перекристаллизации из смеси изопропанола и н-гептана получают 0,8 г целевого соединения (выход: 30% теории). Получаемые при этом изомеры с двойными связями разделяют путем хроматографии и/или кристаллизации. Указанные выходы относятся к изолированным продуктам. Примеры 4 и 5 Сложный диметиловый эфир 4-метил-6-метиламино-2-(4-трифторметил-фенил)-циклогекса-3,6-диен-1,3-дикарбоновой кислоты (пример 4) Сложный диметиловый эфир 6-метил-4-метиламино-2-(4-трифторметил-фенил)-циклогекса-3,5-диен-1,3-дикарбоновой кислоты (пример 5) 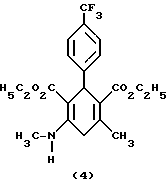 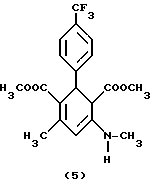 10,0 г (25 ммоль) сложного диметилового эфира 6-окси-6-метил-4-метиламино-2-(4-трифторметилфенил)-циклогекс-3-ен-1,3-дикарбоновой кислоты (получаемого аналогичным примеру 2 путем) подают в 100 мл пиридина, смесь нагревают до температуры 60oC и добавляют 2,5 мл тионилхлорида. Перемешивают в течение 10 минут при температуре 60oC, сгущают и остаток подают в метиленхлорид, трижды промывают водой, сушат и сгущают. Остаток подвергают грубой очистке путем хроматографии на 200 г силикагеля с применением в качестве элюента смеси петролейного эфира и этилацетата в соотношении 3:1, после чего разделяют путем препаративной хроматографии на слоях с применением в качестве элюента метиленхлорида и этилацетата в соотношении 30:1. Получают две фракции. Из смеси простого эфира и петролейного эфира кристаллизуют 224 мг (2,3% теории) сложного диметилового эфира 4-метил-6-метиламино-2-(4-трифторметилфенил)-циклогекса-3,6-диен-1,3-дикарбоновой кислоты (неполярный изомер (2)). Из второй фракции из этилацетата выделяют 2,29 г (22% теории) полярного изомера, т.е. сложного диметилового эфира 6-метил-4-метиламино-2-(4- трифторметилфенил)- циклогекса-3,5-диен-1,3-дикарбоновой кислоты (3) в виде гидрохлорида (Rf = 0,47; в качестве элюента применяют смесь полиэтилена с этилацетатом в соотношении 7:3). Аналогично примерам 3-5 и в соответствии с вышеуказанным общим данным получают приведенные в таблицах 2 и 3 соединения. Приведенные для каждого соединения значения Rf определяют с применением в качестве элюента смеси полиэтилена с этилацетатом в соотношении 7:3. Формула изобретения
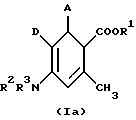 или 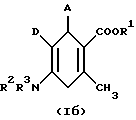 где А – фенил или нафтил, незамещенный или замещенный 1 – 3 одинаковыми или различными остатками из группы, включающей нитро, галоид, трифторметил, неразветвленным или разветвленным алкилом с 1 – 6 атомами углерода; R1 – водород или неразветвленный или разветвленный алкил с 1 – 8 атомами углерода; R2 и R3 – одинаковы или различны и означают водород или неразветвленный или разветвленный алкил с 1 – 6 атомами углерода; D – неразветвленный или разветвленный алкоксикарбонил с 1 – 8 атомами углерода, смесь их изомеров или отдельные изомеры и их соли. 2. Производные циклогексадиена общих формул Ia или Iб по п.1, где А – фенил или нафтил, незамещенные или замещенные 1 – 3 одинаковыми или различными остатками из группы, включающей нитро, фтор, хлор, бром, йод, трифторметил, неразветвленным или разветвленным алкилом с 1 – 4 атомами углерода, R1 – водород или неразветвленный или разветвленный алкил с 1 – 6 атомами углерода, R2 и R3 – одинаковы или различны и означают водород или неразветвленный или разветвленный алкил с 1 – 4 атомами углерода, D – неразветвленный или разветвленный алкоксикарбонил с 1 – 6 атомами углерода, смесь их изомеров или отдельные изомеры и их соли. 3. Производные циклогексадиена общих формул Ia или Iб по п.1, где А – фенил, незамещенный или замещенный 1 – 3 одинаковыми или различными остатками из группы, включающей нитро, фтор, хлор, бром, йод, трифторметил, метил, R1 – водород, неразветвленный или разветвленный алкилом с 1 – 4 атомами углерода, R2 и R3 – одинаковы или различны и означают водород или неразветвленный или разветвленный алкил с 1 – 3 атомами углерода, D – неразветвленный или разветвленный алкоксикарбонил с 1 – 4 атомами углерода, смесь их изомеров или отдельные изомеры и их соли. 4. Фармацевтическая композиция с избирательным модулирующим действием на зависимые от кальция калиевые канальцы высокой проводимости, содержащая активное начало и по крайней мере один инертный, нетоксичный, фармацевтически приемлемый носитель, отличающаяся тем, что она содержит в качестве активного начала соединение указанных общих формул Ia или Iб по пп.1 – 3. РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 25.08.2001
Извещение опубликовано: 20.11.2004 БИ: 32/2004
|
||||||||||||||||||||||||||
