Патент на изобретение №2155711
|
||||||||||||||||||||||||||
(54) СПОСОБ СОВМЕСТНОГО СЕЛЕКТИВНОГО ВОССТАНОВЛЕНИЯ ПЛУТОНИЯ (IV) И НЕПТУНИЯ (VI) ДЛЯ ОТДЕЛЕНИЯ ИХ ОТ УРАНА (VI)
(57) Реферат: Изобретение относится к способу совместного селективного восстановления ионов Pu и Np в азотнокислых растворах и может быть использовано при отделении этих элементов от урана в химической технологии переработки отработавшего ядерного топлива. Pu (IV) и Np (VI) совместно восстанавливают в азотнокислом растворе. Восстановитель – бессолевое органическое соединение гидразинпропионитрил NCC2H2N2H3. Получают Pu (III) и Np (V). Результат способа: сокращение времени восстановления плутония (IV), отсутствие перевосстановления нептуния (V) до нептуния (IV), более полное отделение Pu и Np от урана. 1 табл. Изобретение относится к способу совместного селективного восстановления ионов Pu и Np в азотнокислых растворах и может быть использовано при отделении этих элементов от урана в химической технологии переработки отработавшего ядерного топлива. В настоящее время процесс переработки отработавшего ядерного топлива включает стадию растворения его в азотной кислоте с получением растворов, содержащих U (VI), Pu (IV), Np (VI), а также продуктов деления. Из полученного водного раствора U, Pu и Np извлекаются экстракцией в органический раствор, например, три-н-бутилфосфата (ТБФ) с разбавителем. Основная часть продуктов деления остается в водном растворе – рафинате. Нитраты U (VI), Pu (IV) и Np (VI) образуют сольваты с экстрагентом, растворимые в органическом растворе ТБФ с разбавителем. Из полученного экстракта, содержащего в основном сольваты U (VI), Pu (IV) и Np (VI), ионы плутония и нептуния отделяются от урана на операции восстановительной реэкстракции. На этой операции органический экстракт промывается водным азотнокислым раствором, содержащим реагенты, которые восстанавливают ионы Pu (IV) и Np (VI) до неэкстрагируемых ТБФ ионов Pu (III) и Np (V), удаляемых с водным раствором. Эта разделительная операция является одной из основных стадий при переработке ядерного топлива. Известен способ совместного восстановления ионов Np (VI) и Pu (IV) и отделения их от урана в виде ионов Np (V) и Pu (III) с использованием в качестве восстановителя U (IV), стабилизированного гидразин-нитратом (Шевченко В.Б. и др. Радиохимия, 1976, т.18, N 5, с.784-789). Недостатком использования U (IV) является низкая селективность восстановления Np (VI) в Np (V). Уран (IV) с заметной скоростью восстанавливает неэкстрагируемый Np (V) далее до экстрагируемого состояния Np (IV), что приводит к уменьшению извлечения Np из органического экстракта до 75-85% при отделении его от урана на этой операции. Остаточный Np дополнительно удаляется из урана с использованием комплексообразователей на первом или на втором урановом цикле (Колтунов B.C. и др. Jnt. Conf. Actinides-89, Tashkent 1989, Abstracts, p.353). Другим недостатком данного способа является необходимость использования стабилизатора U (IV) гидразин-нитрата. Окисление гидразина ионами Pu (IV), Np (VI), азотной и азотистой кислотами приводит к образованию солей – нитрата аммония и потенциально опасных азид-ионов, усложняющих переработку и концентрирование сбросных растворов (Колтунов B.C. и др. Радиохимия, 1993, т. 35, N 6, с.11-21). Известен также способ селективного отделения Pu из органических растворителей, которые могут также содержать уран, где в качестве восстановителей Pu (IV) используется фенилгидразин или ароматические амины в смеси со стабилизатором гидразин-нитратом. Сведений о поведении ионов Np в этом случае не сообщается (патент США 3980750, B 01 D 11/00, 1976). Авторами настоящего изобретения были проведены эксперименты, оценивающие возможность использования для селективного восстановления Np (VI) в Np (V) фенилгидразина. Оказалось, что фенилгидразин и ароматические амины восстанавливают Np (VI) не только до Np (V), но и далее до Np (IV). Таким образом, использование фенилгидразина и ароматических аминов для селективного восстановления ионов Pu (IV) и Np (VI) и отделения их от урана не позволит провести четкое отделение Np от U из-за перевосстановления Np (V) до Np (IV). (Баранов С.М. и др. Радиохимия, 1984, т.26, N 5, с.686-694, Колтунов B.C. и др. Радиохимия, 1993, т.35, N 3. с.31-381.). Другим недостатком использования ароматических восстановителей в азотнокислых растворах является образование осадков малорастворимых продуктов окисления этих восстановителей и необходимость применения их в смеси со стабилизатором гидразин-нитратом. Наиболее близким техническим решением к заявленному способу является метод селективного восстановления Np (VI) и Pu (IV) до Np (V) и Pu (III), в котором в качестве бессолевых восстановителей используют этиловый эфир гидразинуксусной кислоты или 2-гидроксиэтилгидразин. Использование указанных соединений для восстановления Pu (IV) и Np (VI) без добавки стабилизатора – гидразина позволяет получать неэкстрагируемые ионы Pu (III) и Np (V), которые необходимы при отделении указанных элементов от урана в экстракционной технологии переработки облученного ядерного топлива. Скорость восстановления Np (VI) во много раз больше, чем скорость восстановления Pu (IV) до Pu (III). При этом не происходит перевосстановления Np (V) до Np (IV). Недостатком этого способа является низкая скорость восстановления Pu (IV) до Pu (III). Время полного (на 99,9%) завершения реакции в 1 моль/л HNO3, 25oC,  = 2, (азотнокислая среда HNO3 + NaNO3) при концентрации восстановителя 0,1 моль/л для этилового эфира гидразинуксусной кислоты составляет 200 мин, а для 2-гидроксиэтилгидразина – 120 мин. (Koltunov V.S. et al., Intern. Conf. “Global-95”, 1995, France, Proceed, v. 1, p. 577-584).
Технической задачей настоящего изобретения является увеличение скорости восстановления Pu (IV) при одновременном селективном восстановлении ионов Pu (IV) и Np (VI) до Pu (III) и Np (V) с использованием бессолевого восстановителя.
Сущность способа заключается в том, что восстановление Pu (IV) и Np (VI) проводят гидразинпропионитрилом – NCC2H4N2H3.
Отличительный признак изобретения заключается в том, что предлагаемое органическое производное гидразина в силу своих физико-химических свойств позволяет проводить процесс восстановления Pu (IV) и Np (VI) таким образом, что стабилизируется Pu (III) и Np (V) без примеси Np (IV). В качестве такого вещества выбран гидразинпропионитрил.
Экспериментально установлено, что гидразинпропионитрил позволяет проводить селективное восстановление ионов Pu (IV) и Np (VI) до Pu (III) и Np (V). Восстановление U (VI) при этом не наблюдается. При окислении гидразинпропионитрила не образуется солей или осложняющих переработку растворов продуктов.
Восстановление Np (V) до Np (IV) в интервале 20-35oC и концентрации HNO3 0,3-1,5 моль/л гидразинпропионитрилом не наблюдается в течение нескольких часов.
Сравнение скорости восстановления ионов Pu (IV) гидразинпропионитрилом с наиболее близкими по совокупности признаков из известных до настоящего времени селективными восстановителями – этиловым эфиром гидразинуксусной кислоты и 2-гидроксиэтилгидразином показывает, что в одинаковых условиях (температура, концентрация HNO3, концентрация восстановителя) скорость восстановления Pu (IV) в 5-18 раз выше в первом случае, чем во втором и третьем случаях.
Таким образом, в одинаковых условиях проведения селективного восстановления Pu (IV) и Np (VI) для их отделения от урана (VI) время, необходимое для полного восстановления Pu (IV) будет, по крайней мере, в 5 раз меньше, чем при использовании этилового эфира гидразинуксусной кислоты или 2-гидроксиэтилгидразина.
Пример 1.
Скорость восстановления Pu (IV) гидразинпропионитрилом описывается уравнением = 2, (азотнокислая среда HNO3 + NaNO3) при концентрации восстановителя 0,1 моль/л для этилового эфира гидразинуксусной кислоты составляет 200 мин, а для 2-гидроксиэтилгидразина – 120 мин. (Koltunov V.S. et al., Intern. Conf. “Global-95”, 1995, France, Proceed, v. 1, p. 577-584).
Технической задачей настоящего изобретения является увеличение скорости восстановления Pu (IV) при одновременном селективном восстановлении ионов Pu (IV) и Np (VI) до Pu (III) и Np (V) с использованием бессолевого восстановителя.
Сущность способа заключается в том, что восстановление Pu (IV) и Np (VI) проводят гидразинпропионитрилом – NCC2H4N2H3.
Отличительный признак изобретения заключается в том, что предлагаемое органическое производное гидразина в силу своих физико-химических свойств позволяет проводить процесс восстановления Pu (IV) и Np (VI) таким образом, что стабилизируется Pu (III) и Np (V) без примеси Np (IV). В качестве такого вещества выбран гидразинпропионитрил.
Экспериментально установлено, что гидразинпропионитрил позволяет проводить селективное восстановление ионов Pu (IV) и Np (VI) до Pu (III) и Np (V). Восстановление U (VI) при этом не наблюдается. При окислении гидразинпропионитрила не образуется солей или осложняющих переработку растворов продуктов.
Восстановление Np (V) до Np (IV) в интервале 20-35oC и концентрации HNO3 0,3-1,5 моль/л гидразинпропионитрилом не наблюдается в течение нескольких часов.
Сравнение скорости восстановления ионов Pu (IV) гидразинпропионитрилом с наиболее близкими по совокупности признаков из известных до настоящего времени селективными восстановителями – этиловым эфиром гидразинуксусной кислоты и 2-гидроксиэтилгидразином показывает, что в одинаковых условиях (температура, концентрация HNO3, концентрация восстановителя) скорость восстановления Pu (IV) в 5-18 раз выше в первом случае, чем во втором и третьем случаях.
Таким образом, в одинаковых условиях проведения селективного восстановления Pu (IV) и Np (VI) для их отделения от урана (VI) время, необходимое для полного восстановления Pu (IV) будет, по крайней мере, в 5 раз меньше, чем при использовании этилового эфира гидразинуксусной кислоты или 2-гидроксиэтилгидразина.
Пример 1.
Скорость восстановления Pu (IV) гидразинпропионитрилом описывается уравнением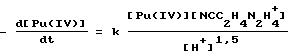 где k = 3,38 моль0,5 (л0,5мин) при 25oC и  = 2. = 2.В таблице приведены времена полного (на 99,9%) завершения реакции восстановления Pu (IV) гидразинпропионитрилом при различной концентрации азотной кислоты по сравнению с известными способами. Из таблицы видно, что использование гидразинпропионитрила приводит к существенному сокращению времени полного восстановления плутония (IV). Пример 2. В спектрофотометрическую 10 мм кювету при 25oC последовательно приливают 0,134 мл раствора 0,134 моль/л плутония (IV) в 7,0 моль/л HNO3; 2,1 мл дистиллированной воды; 0,172 мл 12,0 моль/л HNO3, 0,024 мл раствора 7,43  10-2 моль/л нептуния (VI) в 0,5 моль/л HClO4 и 0,30 мл раствора 1,0 моль/л гидразинпропионитрила в воде. Раствор перемешивают. Через 20 мин снимают спектр пропускания раствора в интервале длин волн 400 – 1000 нм на спектрофотометре СФ-8. Спектр пропускания раствора соответствует смеси валентных форм Pu (III) и Np (V), a Np (IV) в спектре отсутствует. 10-2 моль/л нептуния (VI) в 0,5 моль/л HClO4 и 0,30 мл раствора 1,0 моль/л гидразинпропионитрила в воде. Раствор перемешивают. Через 20 мин снимают спектр пропускания раствора в интервале длин волн 400 – 1000 нм на спектрофотометре СФ-8. Спектр пропускания раствора соответствует смеси валентных форм Pu (III) и Np (V), a Np (IV) в спектре отсутствует.
Формула изобретения
РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 26.12.2005
Извещение опубликовано: 10.12.2006 БИ: 34/2006
|
||||||||||||||||||||||||||
