|
|
(21), (22) Заявка: 2004132078/15, 04.11.2004
(24) Дата начала отсчета срока действия патента:
04.11.2004
(45) Опубликовано: 20.03.2006
(56) Список документов, цитированных в отчете о
поиске:
БУРЛАКОВА Е.Б. И ДР. “Хемилюминесцентный метод изучения природных антиоксидантов в липидах”, Биофизика, 1971, №1, с.39-43. RU 2102747 C1, 20.01.1998. US 6177260 A, 23.01.2001. JP 2003315323 A1, 06.11.2003.
Адрес для переписки:
127473, Москва, ул. Делегатская, 20/1, ГОУ ВПО “Московский государственный медико-стоматологический университет”, патентный отдел
|
(72) Автор(ы):
Прокопов Алексей Александрович (RU),
Шукиль Людмила Владимировна (RU),
Берлянд Александр Семенович (RU)
(73) Патентообладатель(и):
ГОУ ВПО “Московский государственный медико-стоматологический университет Министерства здравоохранения РФ” (RU)
|
(54) СПОСОБ КОЛИЧЕСТВЕННОГО ОПРЕДЕЛЕНИЯ ФЕНОЗАН-КИСЛОТЫ В БИОЛОГИЧЕСКИХ ОБЪЕКТАХ
(57) Реферат:
Изобретение относится к медицине, а именно к фармакологии – способам определения фармакологически активных веществ в биологических объектах. Предлагается способ количественного определения фенозан-кислоты в сложном многокомпонентном биологическом материале, заключающийся в том, что анализируемую пробу биожидкости (кровь, моча) после подкисления до рН=1 обрабатывают для извлечения определяемого вещества органическим экстрагентом. Фенозан-кислоту, содержащуюся в сухом остатке после упаривания экстракта, с целью увеличения летучести переводят в ее метиловый эфир, к которому добавляют раствор додекана, используемого в качестве внутреннего стандарта. Полученный раствор анализируют методом хромато-масс-спектрометрии при следующем температурном режиме: начальная температура колонки 75°С поддерживается без изменения 2 мин после ввода пробы, далее увеличивается до 280°С со скоростью 50 град/мин и поддерживается постоянной до конца программы. Концентрацию фенозан-кислоты определяют по предварительно построенному калибровочному графику. Технический результат: обеспечение возможности количественного определения фенозан-кислоты в плазме крови или моче после внутривенного или внутримышечного введения или после применения таблеток препарата, возможность его использования при выполнении клинических или фармакокинетических исследований препарата, а также при изучении его метаболизма. 3 табл.
Изобретение относится к медицине, а именно к фармакологии – способам определения фармакологически активных веществ в биологических объектах.
Фенозан-кислота (4-гидрокси-3,5-ди-трет-бутилфенилпропионовая кислота) является синтетическим антиоксидантом и изучается в качестве потенциального лекарственного препарата [Трещенкова Ю.А., Голощапов А.Н., Бурлакова Е.Б. Биоантиоксиданты: Тез. докл. V Межд. конф. – М., 1998, С.182-183].
Однако данный способ не может быть использован для определения фенозан-кислоты в биологических объектах, поскольку невозможно с необходимой достоверностью предварительно определить общее базисное содержание эндогенных антиоксидантов у каждого животного.
Задачей изобретения является обеспечение возможности количественного определения фенозан-кислоты в сложном многокомпонентном биологическом материале.
Это достигается за счет того, что анализируемую пробу биожидкости после подкисления до рН=1 обрабатывают органическим экстрагентом для извлечения фенозан-кислоты, после чего переводят ее в метиловый эфир, к которому добавляют раствор додекана, анализируют методом хромато-масс-спектрометрии при следующем температурном режиме: начальную температуру колонки 75°С поддерживают без изменения 2 мин после ввода обработанной пробы биожидкости, далее температуру увеличивают до 280°С со скоростью 50 град/мин, концентрацию фенозан-кислоты определяют по калибровочному графику.
Подкисление анализируемой пробы биожидкости до рН=1 необходимо для того, чтобы полностью подавить ионизацию фенозан-кислоты и тем самым обеспечить полный переход ее в органическую фазу в процессе экстракции. Перевод фенозан-кислоты в ее метиловый эфир осуществляется для того, чтобы повысить летучесть определяемого вещества. Предлагаемый температурный режим газожидкостного хроматографирования аналита необходим потому, что именно в этих условиях происходит удовлетворительное разделение пиков фенозан-кислоты, внутреннего стандарта и эндогенных соединений.
Способ осуществляют следующим образом.
К сухому остатку после эфирной экстракции биожидкости добавляют раствор диазометана. После завершения дериватизации эфир удаляют и к сухому остатку прибавляют хроматографически чистый внутренний стандарт, представляющий собой раствор додекана, например, в метаноле с концентрацией 15 нг/мкл. Пробу полученного раствора сразу же вводят в хромато-масс-спектрометр (например, газовый хроматограф HP 5980 серия II, масс-селективный детектор HP 5971 А и станция обработки данных HP 59970 С).
Пробу анализируют при следующем температурном режиме: начальную температуру колонки 75°С поддерживают без изменения 2 мин после ввода обработанной пробы биожидкости, далее температуру увеличивают до 280°С со скоростью 50 град/мин, концентрацию фенозан-кислоты определяют по калибровочному графику.
Пример. Количественное определение фенозан-кислоты в плазме крови кроликов (модельные растворы). Раствор “стандартной плазмы” готовят из лиофилизированной сухой плазмы добавлением соответствующего количества дистиллированной воды, перемешивания, настаивания, фильтрации. Основной стандартный раствор фенозан-кислоты концентрации 1 мг/мл готовят растворением точно взвешенного количества воздушно-сухого вещества в метаноле. Растворы-метчики получают разведением основного раствора: концентрация метчика от 10 до 1000 мкг/мл в соответствии с данными табл.1. 100 мкл каждого метчика добавляют к 1 мл плазмы для приготовления калибровочных растворов фенозан-кислоты с содержанием от 1 до 100 мкг/мл (Сплазмы). Для каждого значения концентрации готовят три раствора. “Нулевой” раствор содержит 100 мкл чистого метанола в плазме. После введения метчика растворы в плазме выдерживают не менее 1 ч при 20°С для установления равновесия.
Фенозан-кислоту из калибровочных растворов и из биожидкостей выделяют экстракцией эфиром после подкисления растворов до рН=1, эфирные экстракты упаривают в токе воздуха при 40°С. К сухим экстрактам добавляют по 1 мл эфирного раствора диазометана, смеси оставляют на 12 ч. После завершения дериватизации эфир удаляют в токе воздуха, к высушенному остатку приливают от 50 до 200 мкл раствора внутреннего стандарта, а затем 0,6-1,0 мкл полученного раствора сразу же вводят в хроматограф (Сгх).
Воспроизводимость хромато-масс-спектрометрического определения оценивали по стандартному раствору Сгх, содержащему 12,5 нг/мкл метилового эфира фенозан-кислоты (концентрация хроматографируемого раствора Сгх) и 10 нг/мкл внутреннего стандарта, при числе повторностей, равном 7: 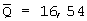 ; S=1,52; Sr=0,09; ; S=1,52; Sr=0,09;  =1,4; доверительный интервал 16,5±1,4; W=9,2%. =1,4; доверительный интервал 16,5±1,4; W=9,2%.
Воспроизводимость методики оценивали по стандартному раствору 4 мкг/мл фенозан-кислоты в плазме (Спл) при числе повторностей, равном 7: 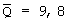 ; S=1,85; Sr=0,19; ; S=1,85; Sr=0,19;  =1,7; доверительный интервал 9,8±1,7; W=17%. Здесь W – коэффициент вариации, S – среднее квадратичное отклонение, =1,7; доверительный интервал 9,8±1,7; W=17%. Здесь W – коэффициент вариации, S – среднее квадратичное отклонение, 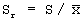 , , 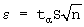 , где t , где t – коэффициент Стьюдента при n=7, – коэффициент Стьюдента при n=7,  =0,95. =0,95.
В табл.2 приведены результаты калибровки. Объединенное уравнение регрессии для интервала концентраций 0,5-100 мкг/мл имеет вид: Спл=0,245Q+1,515 мкг/мл, коэффициент линейной регрессии r=0,998. Для интервала концентраций 0,5-0,01 мкг/мл: Спл=0,097Q-0,0051 мкг/мл, коэффициент линейной регрессии r=0,989.
Для оценки методики в целом независимо приготовленный раствор – стандартный образец фенозан-кислоты в плазме концентрации 4 мкг/мл – был проанализирован среди серии калибровочных растворов. В табл.3 приведены значения определенных по калибровочному графику и рассчитанных концентраций фенозан-кислоты, 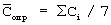 . .
Стандартная статистическая обработка полученных результатов показала их достоверность и высокую воспроизводимость для  =0,95, максимальное единичное отклонение средней величины =0,95, максимальное единичное отклонение средней величины 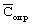 от истинной концентрации составляет 18%, отклонение, рассчитанное для средней величины от истинной концентрации составляет 18%, отклонение, рассчитанное для средней величины  С, составляет 2%. С, составляет 2%.
Из табл.3 видно, что предлагаемый способ количественного определения фенозан-кислоты в биологических объектах методом хромато-масс-спектрометрии обладает высокой чувствительностью и воспроизводимостью, он позволяет надежно и достоверно определять в биологическом материале количественное содержание фенозан-кислоты в различные интервалы времени после его введения.
Разработанный способ может быть использован для количественного определения фенозан-кислоты в плазме крови или моче после внутривенного или внутримышечного введения или после применения таблеток препарата.
| Таблица 1 |
| Приготовление калибровочных растворов фенозан-кислоты в плазме крови. |
| |
|
|
|
|
А |
В |
С |
| № |
Cисх мг/мл |
Vисх мл |
Vобщ мл (МеОН) |
Cметчика мкг/мл |
Cплазмы мкг/мл |
Cгх, нг/мкл |
m (метиловый эфир фенозан-кислоты) нг |
| |
|
|
|
|
|
200 мкл |
25 мкл |
200 мкл |
25 мкл |
| 1 |
1 |
– |
– |
1000 |
100 |
500 |
300 |
| 2 |
1 |
3,5 |
5 |
700 |
70 |
350 |
210 |
| 3 |
1 |
2,5 |
5 |
500 |
50 |
250 |
150 |
| 4 |
1 |
1,0 |
5 |
200 |
20 |
100 |
60 |
| 5 |
1 |
0,5 |
5 |
100 |
10 |
50 |
30 |
| 6 |
1 |
0,25 |
5 |
50 |
5 |
25 |
15 |
| 7 |
1 |
0,10 |
5 |
20 |
2 |
10 |
6 |
| 8 |
0,1 мкг/мл |
0,5 |
5 |
10 |
1 |
5 |
3 |
| 9 |
0,1 мкг/мл |
0,25 |
5 |
5 |
0,5 |
2,5 |
20 |
1,5 |
12 |
| 10 |
0,01 мкг/мл |
0,5 |
5 |
1,0 |
0,1 |
0,5 |
4 |
0,3 |
2,4 |
| 11 |
0,01 мкг/мл |
0,25 |
5 |
0,5 |
0,05 |
0,25 |
2 |
0,15 |
1,2 |
| 12 |
0,001 мкг/мл |
0,5 |
5 |
0,1 |
0,01 |
0,05 |
0,4 |
0,03 |
0,24 |
| А – из расчета объем метчика 100 мкл, объем плазмы 1 мл. |
| В – из расчета объем реконструирующего раствора 200 мкл и 25 мкл. |
| С – из расчета объема пробы, вводимой в хроматограф, равной 0,6 мкл. |
| Таблица 2 |
| Результаты анализа калибровочных растворов фенозан-кислоты в плазме крови. |
| № |
Спл, мкг/мл |
Cгх мкг/мл |
Q1 |
Q2 |
О3 |
| 1 |
100 |
500 |
338 |
340 |
351 |
| 2 |
70 |
350 |
238 |
242 |
242,7 |
| 3 |
50 |
250 |
170,7 |
168,3 |
190 |
| 4 |
20 |
100 |
58,5 |
51,8 |
56,4 |
| 5 |
10 |
50 |
31,12 |
39,3 |
31,6 |
| 6 |
5 |
25 |
12,4 |
10,02 |
13,6 |
| 7 |
2 |
10 |
4,44 |
4,52 |
2,66 |
| Таблица 3 |
| Оценка точности методики анализа фенозан-кислоты в плазме крови. |
| № |
Q |
 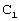 |
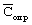 |
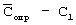 |
S |
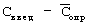 |
 С С |
| 1 |
13,157 |
4,74 |
|
0,83 |
|
0,74 |
18,5 |
| 2 |
8,93 |
3,70 |
|
0,21 |
|
0,30 |
7,5 |
| 3 |
9,57 |
3,86 |
|
0,05 |
|
0,14 |
3,5 |
| 4 |
9,80 |
3,92 |
3,91 |
0,01 |
0,455 |
0,08 |
2,0 |
| 5 |
7,44 |
3,34 |
|
0,57 |
|
0,66 |
16,5 |
| 6 |
8,56 |
3,61 |
|
0,30 |
|
0,39 |
9,75 |
| 7 |
11,01 |
4,21 |
|
0,30 |
|
0,21 |
5,25 |
Формула изобретения
Способ количественного определения фенозан-кислоты, 4-гидрокси-3,5-ди-трет-бутилфенилпропионовой кислоты в биологических жидкостях, характеризующийся тем, что анализируемую пробу биожидкости после подкисления до рН=1 обрабатывают органическим экстрагентом для извлечения фенозан-кислоты, после чего переводят ее в метиловый эфир, к которому добавляют раствор додекана, анализируют методом хромато-масс-спектрометрии при следующем температурном режиме: начальную температуру колонки 75°С поддерживают без изменения 2 мин после ввода обработанной пробы биожидкости, далее температуру увеличивают до 280°С со скоростью 50 град/мин, концентрацию фенозан-кислоты определяют по калибровочному графику.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 05.11.2006
Извещение опубликовано: 20.06.2008 БИ: 17/2008
|
|