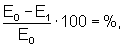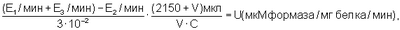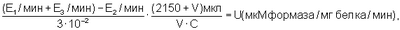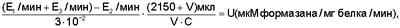Патент на изобретение №2272074
|
||||||||||||||||||||||||||
(54) СПОСОБ ОПРЕДЕЛЕНИЯ АКТИВНОСТИ СУПЕРОКСИДДИСМУТАЗЫ
(57) Реферат:
Изобретение относится к области биохимии и касается способов определения активности антиоксидантного фермента супероксиддисмутазы (СОД). Способ заключается в следующем. Перед началом измерения определяют собственную ксантиноксидазную активность исследуемого образца (Е3). Для этого в кювету к среде инкубации, содержащую растворы карбоната натрия – 50 мМ, ЭДТА – 0,1 мМ, НСТ – 37,5 мкМ в 50 мМ фосфатном буфере рН 10,2 и 73 мкл 0,1 мМ раствора ксантина в 0,5 N NaOH и не содержащую ксантиноксидазу, добавляют исследуемый образец. Регистрируют изменение оптической плотности в течение 3-5 мин при длине волны 560 нм по полученной кинетической кривой (Е3). Определяют начальную скорость восстановления НСТ без СОД по известной ранее методике. В ту же кювету добавляют исследуемый образец, содержащий СОД в количестве, приводящем к изменению оптической плотности раствора, связанному с восстановлением НСТ со скоростью 0,017-0,02 Е в минуту и подобранному для однотипных образцов так, чтобы измерение проходило в условиях избытка субстрата, приводящее к пропорциональному изменению регистрируемой скорости реакции. Рассчитывают изменение оптической плотности за одну минуту в пересчете на количество белка в пробе (E1). Измеряют количество белка в изучаемом образце. Рассчитывают активность СОД исследуемого образца по заданной формуле. Изобретение обеспечивает повышение точности и информативности способа, исключение наиболее часто встречающихся ошибок определения активности фермента и стандартизации единиц измерения активности в соответствии с международной системой.
(56) (продолжение): CLASS=”b560m”определения ее в биологических материалах. Лабораторное дело, 1985, 11, с.678-681.
Изобретение относится к области биохимии и касается способов определения активности антиоксидантного фермента супероксиддисмутазы (СОД). В биохимической практике известны способы определения активности СОД, заключающиеся в добавлении СОД в систему, содержащую супероксидные радикалы и их индикаторы (окислитель или восстановитель). Степень торможения процесса восстановления (или окисления) перехватчика в присутствии СОД характеризует активность фермента. За единицу активности СОД принимают количество белка, которое вызывает 50%-ное торможение реакции восстановления (или окисления) индикатора в определенных условиях [1-7]. Наиболее близким способом определения активности СОД (прототипом) является способ определения активности СОД путем оценки степени торможения супероксиддисмутазой реакции восстановления нитросинего тетразолия (НСТ) в формазан супероксидными радикалами, генерируемыми системой ферментативного окисления ксантина в мочевую кислоту в присутствии ксантиноксидазы [1, 2, 8]. Способ осуществляют следующим образом: 1. Реакцию начинают путем добавления ксантиноксидазы (0,05 единиц активности на пробу) в инкубационную смесь, содержащую растворы карбоната натрия – 50 мМ, ЭДТА – 0,1 мМ, НСТ – 37,5 мкМ в 50 мМ фосфатном буфере рН 10,2, и в последнюю очередь добавляют 73 мкл 0,1 мМ раствора ксантина в 0,5 N NaOH. 2. Регистрируют изменение оптической плотности раствора по кинетической кривой в течение 3-5 мин при длине волны 560 нм и определяют начальную скорость восстановления НСТ без СОД. Скорость реакции выражают в единицах оптической плотности раствора в единицу времени, в пересчете на количество белка в пробе (Е0). 3 В ту же кювету добавляют образец, содержащий СОД, и также в течение 3-5 минут регистрируют нарастание оптической плотности раствора (Е), восстанавливающего НСТ в присутствии СОД. Рассчитывают изменение оптической плотности за одну минуту в пересчете на количество белка в пробе (Е1). 4. Торможение определяют как отношение (в процентах) разности изменения оптической плотности раствора, восстанавливающего НСТ без СОД (Е0), и изменения оптической плотности раствора, восстанавливающего НСТ в присутствии СОД (E1), к изменению оптической плотности раствора, восстанавливающего НСТ без СОД (Е0). Расчет активности СОД проводят по формуле: где Е0 – изменение оптической плотности раствора восстанавливающего НСТ без СОД за одну минуту; E1 – изменение оптической плотности раствора восстанавливающего НСТ в присутствии СОД изучаемого образца за одну минуту. За единицу активности СОД принимают количество белка, вызывающее 50%-ное торможение реакции восстановления нитросинего тетразолия. Поскольку константа скорости реакции НСТ с супероксидным радикалом достаточно низка по сравнению с константой скорости реакции дисмутации супероксида в присутствии СОД, реакция восстановления НСТ чувствительна к СОД и позволяет определять наномолярные концентрации фермента. Однако данный способ недостаточно точен и информативен потому, что в нем не учитывается собственная ксантиноксидазная активность исследуемого образца. Выражение ферментативной активности СОД в процентах не позволяет с достаточной степенью точности учитывать изменения ферментативной активности, выражающиеся в долях процента. Расчет активности фермента в процентах не соответствует принятым в международной системе стандартам измерения, что может создавать определенные трудности при интерпретации результатов. Кроме того, неточный подбор количества исследуемого материала может привести к неправильному выбору участка кинетической кривой, что в свою очередь увеличивает ошибку определения активности фермента. В проанализированной авторами литературе [1-8] не найдено данной совокупности отличительных признаков, приводящих к решению новой технической задачи. Таким образом, предлагаемое техническое решение соответствует критериям изобретения: “новизна” и “изобретательский уровень”, «промышленно применимо». Способ апробирован и может использоваться в биохимической практике. Задачей предлагаемого способа является повышение его точности и информативности, исключение наиболее часто встречающихся ошибок определения активности фермента и стандартизации единиц измерения активности в соответствии с международной системой. Поставленную задачу решают предлагаемым способом определения активности СОД. Перед началом измерения определяют собственную ксантиноксидазную активность исследуемого образца (Е3). Для этого в кювету к среде инкубации, содержащую растворы карбоната натрия – 50 мМ, ЭДТА – 0,1 мМ, НСТ – 37,5 мкМ в 50 мМ фосфатном буфере рН 10,2 и 73 мкл 0,1 мМ раствора ксантина в 0,5 N NaOH и не содержащую ксантиноксидазу, добавляют исследуемый образец. Регистрируют изменение оптической плотности в течение 3-5 мин при длине волны 560 нм по полученной кинетической кривой (Е3). Определяют начальную скорость восстановления НСТ без СОД по известной ранее методике. В ту же кювету добавляют исследуемый образец, содержащий СОД в количестве, приводящем к изменению оптической плотности раствора, связанному с восстановлением НСТ со скоростью 0,017-0,02 Е в минуту и подобранному для однотипных образцов так, чтобы измерение проходило в условиях избытка субстрата, приводящее к пропорциональному изменению регистрируемой скорости реакции. Рассчитывают изменение оптической плотности за одну минуту в пересчете на количество белка в пробе. (E1). Измеряют количество белка в изучаемом образце. Рассчитывают активность СОД исследуемого образца по предлагаемой нами формуле, используя коэффициент молярной экстинции диформазана [9]: где U – единица активности фермента; 2150 мкл – объем среды инкубации; 3·10-2 – коэффициент молярной экстинции диформазана; V – объем исследуемого материала; С – концентрация белка, мг/мл; E1 – изменение оптической плотности раствора восстанавливающего НСТ до диформазана без СОД за одну минуту; Е2 – изменение оптической плотности раствора восстанавливающего НСТ до диформазана в присутствии СОД изучаемого образца за одну минуту; Е3 – изменение оптической плотности раствора восстанавливающего НСТ до диформазана супероксидом, генерируемый ксантиноксидазой изучаемого образца. За единицу активности СОД принимают разницу в количестве восстановленного диформазана без участия СОД и количеством диформазана восстановленного при ингибировании этой реакции СОД за одну минуту в 1 мл раствора, в пересчете на 1 мг белка в пробе. U = (мкМ формазана/мг белка/мин). Способ осуществляют следующим образом: Активность СОД определяют путем определения степени торможения супероксиддисмутазой реакции восстановления нитросинего тетразолия (НСТ) в формазан супероксидными радикалами, генерируемыми системой ферментативного окисления ксантина в мочевую кислоту в присутствии ксантиноксидазы. 1. Перед началом реакции определяют собственную ксантиноксидазную активность исследуемого образца (Е3). Для этого в кювету к среде инкубации, не содержащей ксантиноксидазу, добавляют исследуемый образец. Регистрируют изменение оптической плотности в течение 3-5 мин при длине волны 560 нм по полученной кинетической кривой. Скорость реакции восстановления НСТ супероксидным радикалом, генерируемым собственной ксантиноксидазой исследуемого образца, выражена в единицах нарастания оптической плотности раствора в минуту в пересчете на количество белка в пробе. При изменении оптической плотности раствора больше 0,001 единицы в минуту, то она вводится в формулу расчета активности СОД (Е3). 2. В инкубационную смесь, содержащую растворы карбоната натрия – 50 мМ, ЭДТА – 0,1 мМ, НСТ – 37,5 мкМ в 50 мМ фосфатном буфере рН 10,2 добавляют 73 мкл 0,1 мМ раствора ксантина в 0,5 N NaOH. Реакцию запускают добавлением ксантиноксидазы (0,05 единиц активности на пробу). 3. Регистрируют изменение оптической плотности раствора по кинетической кривой в течение 3-5 мин при длине волны 560 нм и определяют начальную скорость восстановления НСТ без СОД. Рассчитывают изменение оптической плотности за одну минуту в пересчете на количество белка в пробе (Е0). 4. В ту же кювету добавляют исследуемый образец, содержащий СОД в количестве, приводящем к изменению оптической плотности раствора, связанному с восстановлением НСТ 0,017-0,02 единицы в минуту и подобранному экспериментально для однотипных образцов так, чтобы измерение проходило в условиях избытка субстрата, которое приводит к пропорциональному изменению регистрируемой скорости реакции. Измеряют оптическую плотность полученной кинетической кривой (Е2). 5. Измеряют количество белка в изучаемом образце. Рассчитывают активность СОД исследуемого материала по формуле, в которой нами использован коэффициент молярной экстинции образующегося диформазана: (Е=3,0 мМ/см [1]): где U – единица активности фермента; 2150 мкл – объем среды инкубации; 3·10-2 – коэффициент молярной экстинции диформазана; V – объем исследуемого материала; С – концентрация белка, мг/мл; E1 – единицы оптической плотности раствора восстанавливающего НСТ до диформазана без СОД за одну минуту; Е2 – единицы оптической плотности раствора восстанавливающего НСТ до диформазана в присутствии СОД изучаемого образца за одну минуту; Е3 – единицы оптической плотности раствора восстанавливающего НСТ до диформазана супероксидом, генерируемым ксантиноксидазой изучаемого образца. За единицу активности СОД принимают разницу в количестве восстановленного диформазана без участия СОД и количеством диформазана восстановленного при ингибировании этой реакции СОД за одну минуту в 1 мл раствора, в пересчете на 1 мг белка в пробе. U = (мкМ формазана/мг белка/мин). Преимуществом предлагаемого способа является: 1. Проверка собственной ксантиноксидазной активности исследуемого образца дает увеличение точности расчета активности фермента до 25-35%. 2. Подбор количества исследуемого образца проводится таким образом, чтобы измерение проходило в условиях избытка субстрата и приводило к пропорциональному изменению скорости реакции. График, описывающий зависимость скорости реакции от количества белка в пробе, представляет из себя гиперболу. Для правильного и точного расчета необходимо выбирать линейный участок кривой. Правильный подбор количества исследуемого материала исключает возможность ошибки выбора нелинейного участка кинетической кривой. 3. Расчет активности СОД с помощью коэффициента молярной экстинции образующегося диформазана (Е=3,0 мМ/см) увеличивает точность расчета и приводит к стандартизации единиц активности фермента, принятой в международной системе. Рассчитывают активность СОД, используя коэффициент молекулярной экстинкции диформазана, Е=3,0 мМ/см [1]. Таким образом, предложенный способ позволяет увеличить точность расчета активности СОД, исключает возможность ошибки, обусловленной неправильно выбранным участком кинетической кривой, и стандартизирует результаты измерения активности фермента в соответствии с принятыми в международной системе единицами измерения активности. Метод апробирован на большом количестве экспериментального материала. Список литературы 1. Oberley L.W. and Spitz D.R. Assay of superoxide dismutase using nitroblue tetrazolium. In: R.A.Greenwaid (ed.). Handbook for Oxy Radical Research, Boca Raton, FL: CRC Press, in press, 1985. 2. Fridovich I. – Advanc. EnzymoL, 1974, v.41, p.35. 3. Fielden E.M., Roberts P.B. Bray R.C. et al. – Biochem. J., 1974, v.139, p.49. 4. Beauchamp Ch., Fridovich I. – Analyt. Biochem., 1971, v.44, p.276. 5. J.M.McCord, et al., J.Biol. Chem., 244, 6049 (1969). 6. С.Чеварти, И.Чаба, И.Секей. Роль супероксиддисмутазы в окислительных процессах клетки и метод определения ее в биологических материалах. Лабораторное дело, 1985, 11, с 678-681. 7. Патент 2144674 (Сирота Татьяна Валериановна) «Способ определения антиоксидантной активности супероксиддисмутазы и химических соединений» Б.И.П.М. №2, 2000 г., стр.266. Формула изобретения
Способ определения активности супероксиддисмутазы, заключающийся в определении степени торможения супероксиддисмутазой реакции восстановления нитросинего тетразолия (НСТ) в формазан супероксидными радикалами, генерируемыми системой ферментативного окисления ксантина в мочевую кислоту в присутствии ксантиноксидазы путем добавления ксантиноксидазы в количестве 0,05 единиц активности на пробу в инкубационную смесь, содержащую растворы карбоната натрия – 50 мМ, ЭДТА – 0,1 мМ, НСТ – 37,5 мкМ в 50 мМ фосфатном буфере рН 10,2 и 73 мкл 0,1 мМ раствора ксантина в 0,5 N NaOH, регистрации изменения оптической плотности раствора по кинетической кривой в течение 3-5 мин при длине волны 560 нм и определении начальной скорости восстановления НСТ без СОД по полученной кинетической кривой, расчета изменения оптической плотности за одну минуту в пересчете на количество белка в пробе, добавления в ту же кювету образца, содержащего СОД, регистрации в течение 3-5 мин нарастания оптической плотности раствора, восстанавливающего НСТ уже в присутствии СОД, расчета изменения оптической плотности за одну минуту в пересчете на количество белка в пробе и определении активности СОД, отличающийся тем, что дополнительно перед началом реакции определяют собственную ксантиноксидазную активность исследуемого образца при добавлении исследуемого образца к среде инкубации, не содержащей ксантиноксидазу путем регистрации изменения оптической плотности в течение 3-5 мин при длине волны 560 нм по полученной кинетической кривой, в кювету, содержащую среду инкубации и ксантиноксидазу, добавляют исследуемый образец, содержащий СОД в количестве, приводящем к изменению оптической плотности раствора, связанному с восстановлением НСТ 0,017-0,02 единицы в минуту так, чтобы измерение проходило в условиях избытка субстрата, которое приводит к пропорциональному изменению регистрируемой скорости реакции и рассчитывают активность СОД по формуле: где U – единица активности фермента; 2150 мкл – объем среды инкубации; 3·10-2 – коэффициент молярной экстинкции диформазана; V – объем исследуемого материала; С – концентрация белка, мг/мл; E1 – единицы оптической плотности раствора, восстанавливающего НСТ до диформазана без СОД за одну минуту; Е2 – единицы оптической плотности раствора восстанавливающего НСТ до диформазана в присутствии СОД изучаемого образца за одну минуту; Е3 – изменение оптической плотности раствора восстанавливающего НСТ до диформазана супероксидом, генерируемый ксантиноксидазой изучаемого образца, причем за единицу активности СОД принимают разницу в количестве восстановленного диформазана без участия СОД и количеством диформазана, восстановленного при ингибировании этой реакции СОД за одну минуту в 1 мл раствора, в пересчете на мг белка в пробе, U = (мкМ диформазана/ мг белка/мин).
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 14.08.2006
Извещение опубликовано: 20.08.2007 БИ: 23/2007
|
||||||||||||||||||||||||||