|
(21), (22) Заявка: 2004104032/14, 11.02.2004
(24) Дата начала отсчета срока действия патента:
11.02.2004
(43) Дата публикации заявки: 20.07.2005
(45) Опубликовано: 10.02.2006
(56) Список документов, цитированных в отчете о
поиске:
RU 2009547 С1, 15.03.1994. RU 2117997 C1, 10.08.1998. SU 568065 A1, 05.08.1977.
Адрес для переписки:
195427, Санкт-Петербург, ул. Акад. Байкова, 8, ФГУ “РНИИТО им. Р.Р.Вредена Росздрава”, патентный отдел
|
(72) Автор(ы):
Нетылько Георгий Иванович (RU),
Каныкин Александр Юрьевич (RU),
Зайцева Марина Юрьевна (RU)
(73) Патентообладатель(и):
Федеральное государственное учреждение “Российский научно-исследовательский институт травматологии и ортопедии им. Р.Р.Вредена Федерального агентства по здравоохранению и социальному развитию” (ФГУ “РНИИТО им. Р.Р.Вредена Росздрава”) (RU)
|
(54) СПОСОБ СОЗДАНИЯ МОДЕЛИ СЕГМЕНТАРНОГО ОСТЕОНЕКРОЗА МЫЩЕЛКОВ, СОСТАВЛЯЮЩИХ КОЛЕННЫЙ СУСТАВ У ЖИВОТНЫХ
(57) Реферат:
Изобретение относится к экспериментальной медицине и может быть использовано для воспроизведения модели создания сегментарного остеонекроза (асептического некроза) мыщелков, составляющих коленный сустав, при испытании различных способов лечения и средств профилактики остеонекроза. Способ включает ежедневное параартикулярное введение адреналина крысе с возрастным остеопорозом и ренальной остеодистрофией. При этом вводят 0,2 мл 0,1% раствора адреналина в течение 6 недель и два раза в неделю внутрисуставно под надколенник 0,12 мг метилпреднизалона. Способ позволяет создать полиэтиологичный экспериментальный процесс, а также получить очаговый некроз костной ткани мыщелков, составляющих коленный су стад. 1 табл., 6 ил. 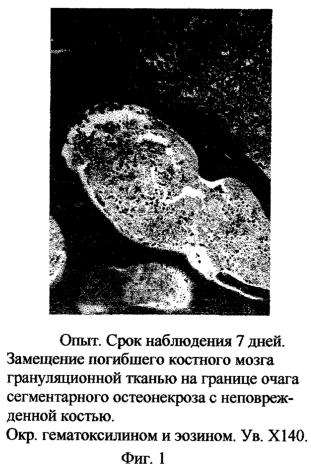
Изобретение относится к экспериментальной медицине и может быть использовано для воспроизведения модели создания сегментарного остеонекроза (асептического некроза) мыщелков, составляющих коленный сустав при испытании различных способов лечения и средств профилактики остеонекроза.
В подавляющем большинстве известных экспериментальных исследований моделировался остеонекроз головки бедренной кости.
Недостатком методики является то, что исследуемый сустав подвергается травматическому оперативному вмешательству. Поэтому последующие лечебные и профилактические мероприятия будут проводиться на суставе, имеющем тяжелые повреждения, и должны быть направлены не только на коррекцию изменений в очаге некроза, но и на восстановление сустава в целом. Исход мероприятий по лечению и профилактике остеонекроза в данном случае будут зависеть от процессов реваскуляризации и регенерации костной ткани в зоне травматического повреждения. Применение данной методики приводило к полной аваскуляризации и крупноочаговому остеонекрозу эпифизарной зоны, а не к сегментарному некроз субхондральной кости, наблюдаемому в клинике. Поэтому на модели невозможно испытание методов оперативного замещения костно-хрящевого фрагмента в очаге некроза.
Недостатком вышеприведенной методики является то, что в результате тромбоза магистральной артерии, питающей кость, помимо крупноочагового остеонекроза эпифизов наблюдается некроз костного мозга и костной ткани диафиза. Результаты последующих испытаний лечебных и профилактических методик будут извращены наличием гранулематозной воспалительной реакцией на инородный материал, возникающей в костной ткани при введение металлического серебра в артерию, питающую кость.
Применение данной методики для создания модели сегментарного остеонекроза в мыщелках, составляющих коленный сустав у крыс, не привело к ожидаемому результату. На 30-56 день у них наблюдалось лишь обеднение костного мозга и определяемое гистоморфометрически статистически недостоверное уменьшение объема костной ткани эпифизов, что свидетельствует о развитии хронической ишемии. Однако ни в одном из наблюдаемых случаев не было выявлено некроза костных структур эпифизов.
Учитывая анализ клинического материала, из которого следует, что заболевание данной локализации чаще возникает в пожилом возрасте на фоне хронической сосудистой недостаточности и смешанных остеопатий, обусловленных наличием сопутствующей патологии внутренних органов и эндокринных нарушений, а также предшествующего внутрисуставного введения кортикостероидов, сделано предположение о полиэтиологичности асептического некроза мыщелков, составляющих коленный сустав.
Результатом воспроизведения модели сегментарного остеонекроза мыщелков, составляющих коленный сустав, используемой при испытании различных способов и средств профилактики и лечения асептического некроза мыщелков, составляющих коленный сустав, достигается за счет того, что подопытным животным со смешанной остеопатией (возрастным остеопорозом и ренальной остеодистрофией) в течение 6 недель вводили ежедневно в параартикулярные ткани 0,2 мл 0,1% раствора адреналина и 2 раза в неделю внутрисуставно под надколенник – по 0,12 мг метилпреднизолона.
Преимуществом данного способа моделирования остеонекроза является полиэтиологичность экспериментально созданного патологического процесса, а также получение очагового некроза костной ткани мыщелков, составляющих коленный сустав, наиболее часто встречающегося в клинической практике.
Контрольной группе животных внутрисуставно и в параартикулярные ткани вводили физиологический раствор в том же объеме и с той же частотой. Контрлатеральный коленный сустав также служил контролем. Суставы обрабатывались антисептиком до и после инъекций.
Экспериментально исследовалось количество введения адреналина. Увеличение дозы адреналина до 0,3 мл вызывало у животных общую реакцию в виде тахиаритмии, тахипное, расширения зрачков, что считалось нежелательным. Применением 0,1% адреналина в объеме 0,2 мл нами достигалась цель создания очага хронической ишемии, о чем свидетельствовало понижение локальной температуры в области исследуемого сустава при отсутствии изменений общего состояния животных. Место введения адреналина не имело существенного значения и не влияло на конечный результат.
Дозировка метилпреднизолона соответствовала предлагаемой для внутрисуставного введения препарата в расчете на килограмм веса (0,3-0,6 мг/кг). В пересчете на массу крысы средняя доза метилпреднизолона, вводимого внутрисуставно, составила 0,12 мг.
Все манипуляции проводили в соответствии с «Правилами гуманного обращения с лабораторными животными».
В течение всего срока проведения эксперимента наблюдали за поведением животных, степенью их активности и весом. По окраске кожи, пальпаторно и по реакции животного определяли болезненность мягких тканей и наличие признаков воспаления в конечности, на которой проводились манипуляции. Сравнивалось изменение локальной температуры в исследуемом суставе по сравнению с контрлатеральным. Для определения температуры использовался бесконтактный термометр фирмы «Астрон».
При обработке данных, полученных в результате эксперимента, использовались клинический, рентгенологический и морфологический методы исследования.
Рентгенологическое обследование проводилось до начала эксперимента и после выведения животных из эксперимента через 2, 4, 6, 8 недель с увеличением в 8 раз.
Из эксперимента животных выводили на 3-и, 7-е сутки, 2-ю, 4-ю, 6-ю и 8-ю неделю наблюдения. Эвтаназию производили в соответствии с «Правилами гуманного обращения с животными» путем внутрибрюшинного введения анестетиков в летальной дозе (450 мг/кг 2% раствора гексенала).
Пример 1 (опыт). Крыса №118.
Возраст крысы 2 года, вес 200 г. За 6 месяцев до начала эксперимента крысе произведено удаление правой и повреждение левой почки. На предварительном рентгенологическом исследовании выявлен остеопороз. В биохимическом анализе крови наблюдалось повышение коеатинина до 0,085 ммоль/л, щелочной фосфатазы до 0,003 мкмоль/л, кальция до 0,62 мкмоль/л. Ежедневное параартикулярное введение 0,2мл 0,1% адреналина и внутрисуставное введение 0,12 мг (0,15 мл 0,08% р-ра) метилпреднизолона 2 раза в неделю начато 12.05.03. С первых суток и на протяжении всего срока наблюдения у крысы выявлялась локальная гипотермия сустава, на котором проводились манипуляции, по сравнению с контрлатеральным. Эвтаназия произведена через 4 недели.
Пример 2 (контроль). Крыса №249.
Возраст крысы 2 года, вес 190 г. На предварительной рентгенограмме остеопороз менее выражен. В биохимическом анализе крови показатели содержания креатинина (0,05ммоль/л), щелочной фосфатазы (0,048 мкмоль/л) и кальция (1,67 мкмоль/л) соответствуют норме. Ведение физраствора ежедневно параартикулярно в объеме 0,2 мл и внутрисуставно в объеме 0,15 мл через день начато 12.05.03. Изменения локальной температуры сустава, на котором проводились манипуляции, по сравнению с контрлатеральным не наблюдалось. Эвтаназию производили через 4 недели.
Для гистологического исследования забирался блок тканей, составляющих коленные суставы.
Гистологические препараты фиксировались в 10% растворе нейтрального формалина, декальцинировались в растворе нейтрального трилона Б. После традиционной проводки и заливки в парафин срезы толщиной 7 мкм окрашивались гематоксилином и эозином, альциановым синими пикрофуксином по ван Гизон.
При гистологическом исследовании тканей, составляющих коленный сустав, как в контрольной, так и в опытной группах животных признаков механического повреждения капсулы, связанного с внутрисуставным введением растворов в объеме 0,15 мл, не было обнаружено.
На третьи сутки после начала эксперимента в опыте наблюдалось очаговое обеднение костного мозга внутренних эпифизов бедренной и большеберцовой костей миелоидными элементами. Соответственно биомеханике движений крыс внутренние мыщелки бедренной и большеберцовой костей у них являются наиболее нагружаемой зоной.
Через 7 дней во внутреннем эпифизе бедренной и большеберцовой костей наблюдался сегментарный некроз миелоидного костного мозга, замещающийся в демаркационной зоне молодой грануляционной тканью (фиг.1).
Спустя 2 недели после начала эксперимента в сегментах внутренних мыщелков бедренной и большеберцовой костей выявлялось исчезновение остеоцитов в костных балках. В зоне, пограничной с неповрежденной костью, наблюдались остеокластическая резорбция некротизированных балок и признаки слабовыраженной репаративной регенерации в виде появления остеоидных наслоений на поверхности трабекул и островков остеогенеза в межбалочном пространстве (фиг.2).
Через 3 недели после начала эксперимента суставной хрящ над очагами остеонекроза, локализованными в нагружаемых мыщелках бедренной и большеберцовой костей, был пролабирован с крупными бесклеточными участками. Некротизированные костные балки с большим количеством микротрещин располагались среди аморфных белковых масс. В демаркационной зоне новообразованные слабообизвествленные костные балки сливались друг с другом. В очагах сегментарного остеонекроза, сформированных в менее нагружаемых наружных мыщелках, выявлялась активная репаративная регенерация костной ткани (фиг.3). До 4 недель отчетливых рентгенологических признаков изменения структуры костной и хрящевой ткани мыщелков, составляющих коленный сустав, не выявлялось.
На 4 неделе наблюдения на рентгенограммах отмечалось нарастание остеопороза, выявилась деформация суставных поверхностей мыщелков бедренной и большеберцовой костей с наличием сегментарных очагов гомогенного затемнения в эпифизарной зоне.
Гистологически при локализации патологического процесса во внутренних мыщелках бедренной и большеберцовой костей наблюдалась фрагментация суставного хряща и костной ткани в очаге некроза, отграниченного от прилежащей кости зоной остеосклероза (фиг.4). На суставной поверхности вне очага повреждения хрящ был неравномерно истончен с нарушенной зональностью строения и трещинами. При наличии очагов сегментарного остеонекроза в менее нагружаемых наружных мыщелках бедренной и большеберцовой костей, на поверхности погибших трабекул определялись массивные наслоения новообразованных сливающихся друг с другом костных структур (фиг.5).
Через 6-8 недель на рентгенограммах и гистологически выявлялась картина выраженного гонартроза. При локализации очага сегментарного некроза костной ткани во внутренних мыщелках бедренной и большеберцовой костей на его месте формировался кратероподобный дефект суставной поверхности, дно которого было представлено склерозированной костной тканью (фиг.6).
При локализации участков сегментарного остеонекроза в ненагружаемых наружных мыщелках бедренной и большеберцовой костей наблюдалось восстановление костной ткани в очаге повреждения с признаками компактизации костных структур. При этом наблюдалась деформация суставной поверхности поврежденного мыщелка с замещением гиалинового хряща над очагом остеонекроза фиброзно-хрящевой тканью.
В контрольной группе животных, которым в сустав и периартикулярные ткани вводился физраствор, выведение животных из опыта проводилось в те же сроки. Рентгенологических и гистологических признаков остеонекроза и остеоартроза не выявлялось.
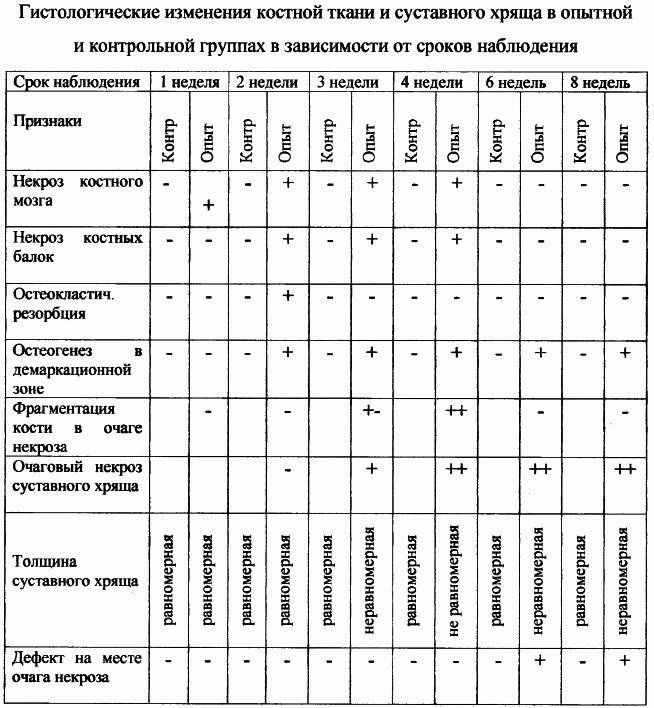
В эксперименте доказана полиэтиологичность заболевания, а также достигнуто формирование сегментарного остеонекроза мыщелков, составляющих коленный сустав, вызванного на фоне возрастного остеопороза и ренальной остеодистрофии ежедневным введением в параартикулярные ткани 2 мл 0,1% адреналина и внутрисуставным введением 0,12 мг метилпреднизолона 2 раза в неделю. Признаки, приведенные в таблице, свидетельствуют о том, что изменения, соответствующие ранней стадии остеонекроза, выявляются спустя 2 недели после начала эксперимента, а через 6-8 недель наблюдается гистологическая картина, соответствующая его поздней стадии. Таким образом, параартикулярное введение адреналина и внутрисуставное введение метилпреднизолона крысам с возрастным остеопорозом и ренальной остеопатией может служить для создания сегментарного остеонекроза коленного сустава.
На момент подачи заявки нам не известна такая или идентичная методика моделирования остеонекроза, что позволяет считать предлагаемый способ отвечающим критерию «новизна».
Формула изобретения
Способ создания модели сегментарного остеонекроза мыщелков, составляющих коленный сустав у животных, включающий ежедневное параартикулярное введение адреналина, отличающийся тем, что крысе с возрастным остеопорозом и ренальной остеодистрофией в течение 6 недель вводят ежедневно в параартикулярные ткани 0,2 мл 0,1%-ного раствора адреналина и два раза в неделю внутрисуставно под надколенник 0,12 мг метилпреднизолона.
РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 12.02.2006
Извещение опубликовано: 27.04.2007 БИ: 12/2007
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 12.02.2006
Извещение опубликовано: 20.06.2007 БИ: 17/2007
|