|
|
(21), (22) Заявка: 2004122346/04, 20.07.2004
(24) Дата начала отсчета срока действия патента:
20.07.2004
(45) Опубликовано: 20.12.2005
(56) Список документов, цитированных в отчете о
поиске:
SU 509048 А, 15.12.1983. SU 630254 A, 30.10.1978.
Адрес для переписки:
150023, г.Ярославль, Московский пр., 88, ЯГТУ
|
(72) Автор(ы):
Каландадзе Л.С. (RU),
Абрамов И.Г. (RU),
Смирнов А.В. (RU),
Сахаров В.Н. (RU),
Сапегин А.В. (RU),
Красовская Г.Г. (RU)
(73) Патентообладатель(и):
Ярославский государственный технический университет (RU)
|
(54) ГЕТЕРОЦИКЛИЧЕСКИЕ О-ДИКАРБОНИТРИЛЫ
(57) Реферат:
Изобретение относится к области технологии органических соединений, а именно к гетероциклическим о-дикарбонитрилам, которые могут быть использованы для получения гексазоцикланов-флуорофоров, в качестве фрагмента-донора для получения гексазоцикланов-бифлуорофоров и гексазоцикланов-трифлуорофоров. Описываются гетероциклические о-дикарбонитрилы общей формулы:
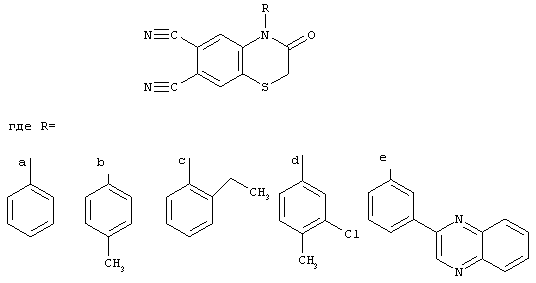
Технический результат – получены новые соединения, обладающие полезными свойствами. 2 табл.
Изобретение относится к области получения новых гетероциклических о-дикарбонитрилов. о-Дикарбонитрилы могут быть использованы для получения гексазоцикланов-флуорофоров, в качестве фрагмента-донора для получения гексазоцикланов-бифлуорофоров и гексазоцикланов-трифлуорофоров. Такие гексазоцикланы перспективны для использования в качестве активных сред жидких и твердых лазеров, сцинтилляторов, особенно для индикации жесткого излучения, для трансформации коротковолнового излучения в длинноволновое при передаче информации по волоконно-оптическим линиям связи, для увеличения мощности солнечных батарей, для защиты ценных бумаг, для изготовления рекламных щитов и т.д.
Данный гексазоциклан обладает следующими спектральными характеристиками: полоса излучения 540 нм при возбуждении в полосу 312 нм.
Задачей, решаемой настоящим изобретением, является получение новых гетероциклических о-дикарбонитрилов.
Заявляются гетероциклические о-дикарбонитрилы общей формулы:
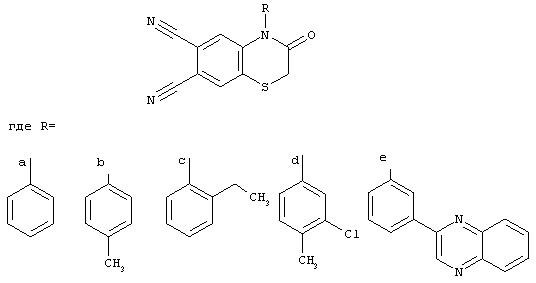
К заявляемым соединениям относятся:
3-оксо-4-фенил-3,4-дигидро-2Н-1,4-бензотиазин-6,7-дикарбонитрил (I):
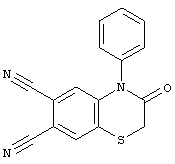
3-оксо-4-(4-метилфенил)-3,4-дигидро-2Н-1,4-бензотиазин-6,7-дикарбонитрил (II):
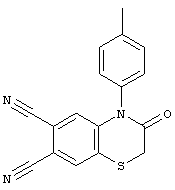
3-оксо-4-(2-этилфенил)-3,4-дигидро-2Н-1,4-бензотиазин-6,7-дикарбонитрил (III):
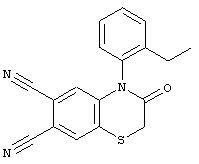
3-оксо-4-(4-метил-3-хлорфенил)-3,4-дигидро-2Н-1,4-бензотиазин-6,7-дикарбонитрил (IV):
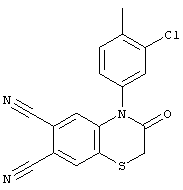
3-оксо-4-[3-(2-хиноксаленил)фенил]-3,4-дигидро-2Н-1,4-бензотиазин-6,7-дикарбонитрил (V):
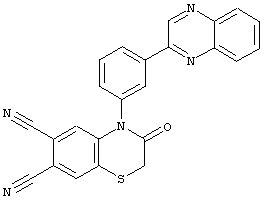
Данные соединения получают реакцией внутримолекулярной денитроциклизации в соответствующих 2-[(4,5-дициано-2-нитрофенил)сульфанил]-N1-фенилацетомидах в присутствии карбоната калия по схеме:
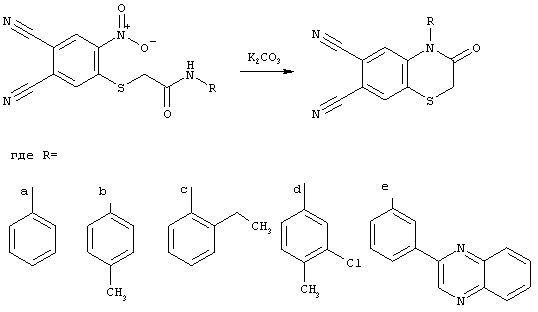
Данную реакцию проводят в среде диметилформамида в присутствии карбоната калия при температуре 90°С в течение 2 ч.
Изобретение иллюстрируется следующими примерами:
Пример 1. К 30 мл ДМФА при перемешивании добавляли 3.38 г (0.01 моль) 2-[(4,5-дициано-2-нитро-фенил)сульфанил]-N1-фенилацетомида и 1.38 г (0.01 моль) К2СО3. Полученную смесь перемешивали при температуре 90°С в течение 2 ч. Далее реакционную массу выливали в 50 мл воды. Выпадавший осадок отфильтровывали, промывали 50 мл воды и перекристаллизовывали из смеси 2-пропанола с ДМФА.
Получают 1,81 г (65% от теории) 3-оксо-4-фенил-3,4-дигидро-2Н-1,4-бензотиазин-6,7-дикарбонитрила (I). Это желтый кристаллический порошок, Тпл. 150-152°С.
Найдено, % С 65.81; Н 3.12; N 14.49; S 11.03
Вычислено, % С 65.97; Н 3.11; N 14.42; S 11.00 C16H9OS
1Н ЯМР ([2Н6] ДМСО):  , м.д.: 8.35 (s, 1H); 7.60 (t, 2H); 7.50 (t, 1H) 7.27 (d, 2H, J=8.0); 6.85 (s, 1H); 3.85 (s, 2H) , м.д.: 8.35 (s, 1H); 7.60 (t, 2H); 7.50 (t, 1H) 7.27 (d, 2H, J=8.0); 6.85 (s, 1H); 3.85 (s, 2H)
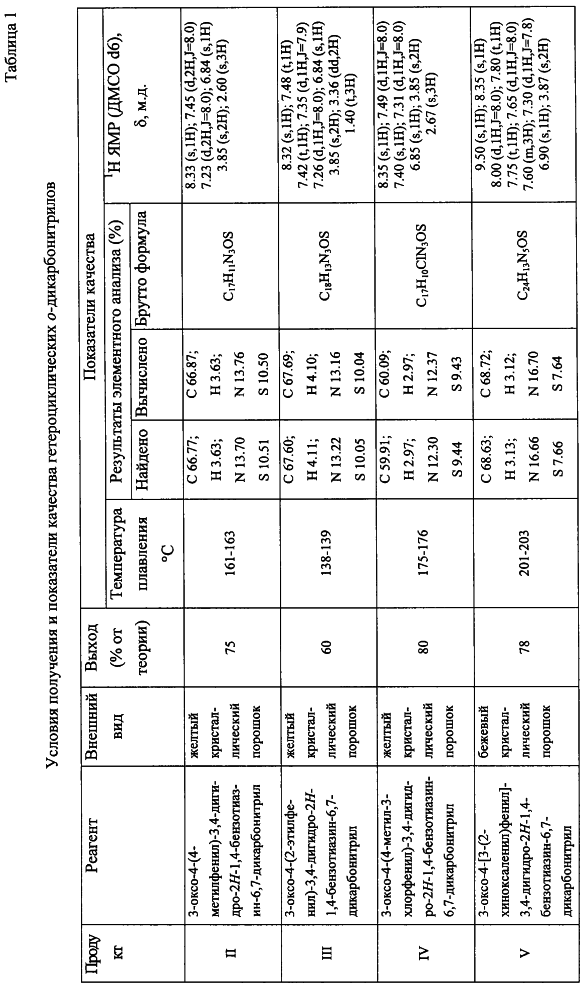
Пример 2-5. Реакцию проводят аналогично примеру 1, за исключением того, что в качестве исходных нитросоединений взяты замещенные 3-оксо-4-фенил-3,4-дигидро-2H-1,4-бензотиазин-6,7-дикарбонитрилы. Условия и результаты синтеза представлены в табл.1.
Пример 6. Конденсация I с родамином 123. В колбу, снабженной мешалкой, термометром, обратным холодильником и капилляром, для ввода аргона загружают 2.91 г (0.01 моль) I, 3.8 г (0.01 моль) родамина 123 и 10 г фенола. Полученную смесь медленно нагревают при перемешивании до 175…185°С. Образовавшийся расплав выдерживают при перемешивании в токе аргона до прекращения выделения аммиака. После окончания реакции реакционную смесь выливают в 20 мл этанола, выпавший осадок отфильтровывают, промывают 3 мл этанола и сушат при Т=60°С в течение 2 часов, затем в вакууме над P2O5. Получают 11.81 г (95% от теории) гексазоциклана.
Найдено, % С 71.42; Н 4.06; N 9.03; S 5.17
Вычислено, % С 71.48; Н 4.05; N 9.01; S 5.16: (C74Н50N8О8S2)
В ИК-спектре гексазоциклана отсутствует полоса 2220 см-1 – C N, присутствует полоса 680 см-1 – C=N-. N, присутствует полоса 680 см-1 – C=N-.
Структурная формула гексазоциклана, полученного на основе I и родамина 123:
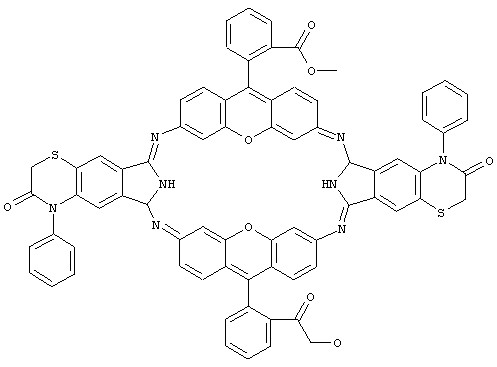
Макрогетероцикл, полученный на основе I и родамина 123, имеет следующие спектральные характеристики: максимумы спектра излучения – 540, 637, 720 нм при максимумах спектра поглощения – 240, 480, 577 нм.
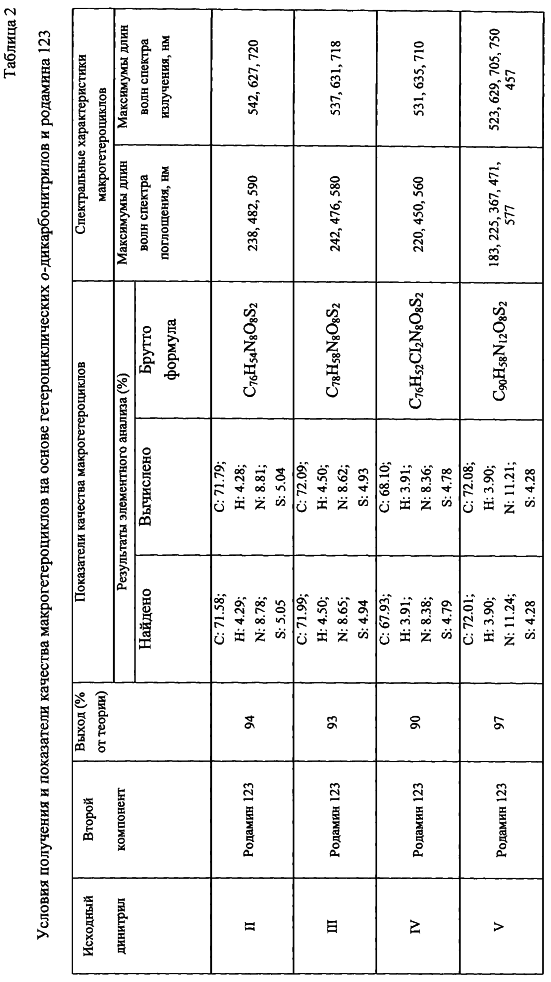
Пример 7-10. Реакцию проводят аналогично примеру 6, за исключением того, что вместо фталонитрила I используются эквимолярные количества фталонитрилов II-V.
Условия и результаты синтеза, а так же спектральные характеристики полученных макрогетероциклов приведены в табл.2.
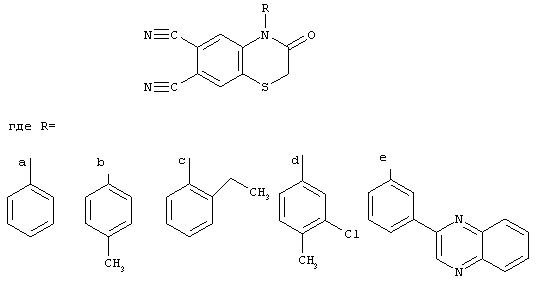
Формула изобретения
Гетероциклические о-дикарбонитрилы общей формулы:
РИСУНКИ
|
|