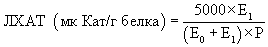Патент на изобретение №2265851
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ОПРЕДЕЛЕНИЯ ТОКСИЧНОСТИ ХИМИЧЕСКИХ ВЕЩЕСТВ
(57) Реферат:
Изобретение относится к области медицины, преимущественно к биохимии и токсикологии, а именно к способу определения токсичности лекарственных препаратов и химических веществ. Способ включает введение лабораторным животным токсического агента, забой животных, приготовление гомогената ткани печени с последующим определением активности фермента, отличающийся тем, что определяют активность фермента лецитин: холестеринацил-трансферазы и по снижению уровня активности фермента в течение 30-180 минут после введения вещества по сравнению с контролем судят о токсичности вещества. Технический результат: сокращение времени исследования токсичности химических веществ. 2 табл.
Изобретение относится к области медицины, преимущественное применение найдет в биохимии и токсикологии и может быть использовано для определения токсичности лекарственных препаратов и химических веществ. Известен способ определения токсичности биологически активных веществ путем введения испытуемых веществ группе подопытных животных и выявления среднесмертельной дозы препарата [1]. Однако известный способ не позволяет точно определить предельно допустимую концентрацию химических веществ. Известен способ определения токсичности химических веществ путем введения лабораторным животным (мышам) одновременно гидрокортизона и токсического агента с последующим определением активности тирозинаминотрансферазы печени черта 4-8 часов после введения [2]. Недостатком известного способа является его продолжительность, т.e. не менее 8 часов эксперимента, а также сочетанное введение химических веществ. Наиболее близким к заявляемому является способ определения токсичности химических веществ [3]. Сущность известного прототипа заключается в определении в гомогенате тканей печени лабораторных животных активности фермента ацилазы (N – ацил – DL – аминокислота – аминогидролазы К.Ф. 3.5.1.14.) через 2-4 часа после введения животным токсического вещества. О токсичности вещества судят по достоверному снижению уровня активности фермента по сравнению с контролем. Целью изобретения является сокращение времени исследования токсичности химических веществ. Для достижения поставленной цели проводится: 1. Введение токсического агента лабораторным животным. 2. Экспозиция, обеспечивающая развитие токсического действия (30-90 минут). 3. Забой животных, извлечение печени и приготовление гомогената ее тканей. 4. Определение активности фермента лецитин: холестерин ацилтрансферазы (ЛХАТ, К.Ф. 2.3.1.43) в тканях печени по следующей методике: через 30 минут после инкубации рабочей смеси с 0,1 мл исследуемой жидкости при 37°С из нее хлороформ – этанолом экстрагировали липиды, пробы наносили на пластинки Siluphol (Чехия) размером 8×100 мм и проводили одномерную восходящую хроматографию до фронта 80 мм. В качестве контроля использовали экстракт рабочего раствора, инкубированный в тех же условиях без добавления исследуемой жидкости. Для определения ферментативной активности пластинку разрезали пополам (0-50 мм, где остаются субстраты и 50-100 мм, куда продвигаются при хроматографировании эфиры холестерина), счищали носитель с липидами в 2 пробирки, содержащие по 5 мм 10% раствора фосфорномолибденовой кислоты, и нагревали до 80°С в водяной бане. Активность ЛХАТ рассчитывали по формуле: где Е0 и Е1 – экстинции, пропорциональные содержанию липидов в начальной и конечной половинках пластинки; 5000 – пересчетный коэффициент. Р – концентрация белка в гомогенате. Пример 1. Группе беспородных белых мышей самцов массой 18-20 г внутрибрюшинно вводился эндотоксин (фирма “Sigma”, США S.eridens) в дозе 10 мг/кг веса. Контрольной группе животных вводился физиологический раствор. Опытная группа состояла из 50 животных. Контрольная – 35. Затем животные забивались через 30, 60, 90, 120, 180 минут соответственно. У животных бралась печень, приготовлялся гомогенат тканей органа, в котором определялась активность фермента ацилазы [3] и ЛХАТ по описанной выше методике. Статистическая обработка проводилась по методам вариационной статистики с учетом коэффициента Стьюдента. Результаты эксперимента отражены в табл. №1, 2. Пример 2. Группе беспородных белых мышей самцов массой 21-23 г внутрибрюшинно вводился тетрахлорметан (ТХМ) в растворе в дозах 1 мл/кг, 4 мл/кг веса. Контрольной группе вводился физиологический раствор. Опытная группа состояла из 50 животных на каждую дозировку вводимого вещества. Затем животные забивались, из печени их готовился тканевой гомогенат, в котором определяли активность ферментов ЛХАТ и ацилазы. Статистическая обработка проводилась аналогичным образом. Данные эксперимента приведены в таблицах №1, 2. Сущность заключается в использовании другого информативного теста, что и позволяет сократить время исследования токсичности химических веществ, оценить опасность данного вещества на организм и определить степень влияния исследуемого агента на ткани печени и в целом на живой организм. Данный способ может быть использован в медицине (токсикологии, фармакологии). Литература: 1. Саноцкий И.В. “Методы определения токсичности и опасности химических веществ”, М., 1970. 2. Авторское свидетельство СССР №1163264, МКИ3 G 01 N 33/48; 23.06.85. 3. Авторское свидетельство СССР №1686376, МКИ3 G 01 N 33/68, 23.10.91.
Формула изобретения
Способ определения токсичности химических веществ, включающий введение лабораторным животным токсического агента, забой животных, приготовление гомогената ткани печени с последующим определением активности фермента, отличающийся тем, что определяют активность фермента лецитин: холестеринацил-трансферазы и по снижению уровня активности фермента в течение 30-180 мин после введения вещества по сравнению с контролем судят о токсичности вещества.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 23.01.2007
Извещение опубликовано: 20.02.2008 БИ: 05/2008
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||