Патент на изобретение №2265842
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ОПРЕДЕЛЕНИЯ АЛЮМИНИЯ В БИОЛОГИЧЕСКИХ ОБЪЕКТАХ
(57) Реферат:
Изобретение относится к химико-токсикологическому контролю при санитарно-гигиенической оценке продуктов животноводства, а также для прижизненной и посмертной диагностики случайных отравлений животных соединениями алюминия, а именно к способу определения алюминия в биологических объектах, заключающемуся в минерализации анализируемого образца азотной, серной и хлорной кислотами, выдерживании смеси при комнатной температуре, кипячении до полного ее обесцвечивания, охлаждении, нейтрализации, добавлении реакционной ацетатной буферной смеси, с последующим измерением оптической плотности и определением концентрации алюминия по калибровочному графику, отличающийся тем, что для минерализации образца азотную, серную и хлорную кислоту добавляют к образцу одновременно, смесь выдерживают при комнатной температуре 15-20 мин, затем нагревают в закрытой колбе при постепенном повышении температуры, смесь кипятят до полного обесцвечивания, используют ацетатную буферную смесь, содержащую 10% раствор гидроксиламина солянокислого, 0,3% эриохромцианина R, 10% растворы NaOH и СН3СООН при рН 5,4, а измерение оптической плотности проводят при длине волны
(56) (продолжение): CLASS=”b560m”scanning microscopy after staining with lumogallion, Uchimi A. et all, Analyst., 1998, 04.123(4); 759-62.
Изобретение относится к химико-токсикологическому контролю при санитарно-гигиенической оценке продуктов животноводства, а также прижизненной и посмертной диагностике случайных отравлений животных соединениями алюминия. В настоящее время соединения алюминия интенсивно используются в медицине, в пищевой промышленности, кормопроизводстве и ветеринарии (в качестве сорбентов, пищевых добавок, добавок в комбикорма, в качестве пестицидов). Соединения алюминия входят в состав лекарственных препаратов, применяемых в медицине и ветеринарии. Признаки отравления соединениями алюминия включают определенную форму энцефалопатии, нарушение обмена фосфора, кальция, магния, железа и, как следствие, развитие рахита, анемии. В экспериментах на животных было подтверждено нейротоксическое и мутагенное действие алюминия. Кроме того, растет число побочных токсических эффектов при использовании алюминия в составе лекарственных препаратов, что также ставит под сомнение безопасность этого металла. Для определения алюминия предложен ряд методов, из которых наиболее широко используются фотометрические, так как они легко осуществимы в условиях областных и районных ветеринарных лабораторий, а также в лабораториях санитарно-эпидемиологического надзора. Известен способ определения алюминия с алюминоном в консервах из рыбы и морепродуктов. Перед проведением анализа необходима минерализация образцов по ГОСТ 26929. В колбу с пробой вносят азотную кислоту из расчета 10 см3 на каждые 5 г пробы. Выдерживают не менее 15 мин, закрывают грушевидной пробкой и кипятят, упаривая до объема 3-5 см3. Колбу охлаждают, вносят 10 см3 азотной кислоты, содержимое упаривают до объема приблизительно 5 см3. Процедуру повторяют 2-4 раза. Затем в колбу вносят 10 см3 азотной кислоты, 5 см3 серной кислоты, 4 см3 хлорной кислоты на каждые 5 г пробы, нагревают и выпаривают до объема примерно 5 см3. Затем колбу охлаждают, добавляют 5 см3 азотной кислоты и 2 см3 хлорной кислоты и нагревают до появления паров серного ангидрида. Последнюю процедуру повторяют до обесцвечивания раствора. Затем раствор охлаждают, добавляют 10 см3 дистиллированной воды и кипятят 10 мин с момента выделения белых паров, затем раствор снова охлаждают. Добавление воды и нагревание повторяют еще два раза. После минерализации минерализат количественно переносят в мерную колбу вместимостью 50 см3. Затем в колбу добавляют 1 см3 раствора сульфата аммония, перемешивают и вносят 25-30 мг аскорбиновой кислоты. После перемешивания раствор оставляют стоять 10 мин. Затем в колбу приливают раствор уксуснокислого аммония для доведения рН среды приблизительно до 4,5, добавляют 10 см3 ацетатного буферного раствора, 1 см3 раствора алюминона и оставляют при комнатной температуре на 10 мин. Колбу опускают в кипящую водяную баню. Точно через 5 мин колбу быстро охлаждают до комнатной температуры и доводят содержимое колбы до метки дистиллированной водой. Через 30 мин интенсивность окраски определяют на фотоколориметре относительно раствора сравнения при длине волны 540±5 нм. Раствор сравнения готовят аналогично испытуемому, используя те же реактивы, в тех же объемах и последовательности, начиная с момента минерализации. Массу алюминия в аликвотном объеме минерализата находят с помощью калибровочного графика, который строится следующим образом. В мерные колбы вместимостью 50 см3 вносят 0,0; 1,0; 2,0; 4,0; 6,0; 8,0; 10,0; 14,0 мкг алюминия. В каждую колбу добавляют 20 см3 дистиллированной воды. Далее добавляются те же реактивы и проводятся те же операции, которые описаны в ходе проведения анализа. Минимальная масса алюминия, определяемая данным методом, 3 мкг в колориметрируемом объеме (ГОСТ 28914-91. Консервы и пресервы из рыбы и морепродуктов. Метод определения алюминия. – М. – 1991). Недостатками данного способа являются его длительность, трудоемкость, большой расход реактивов при минерализации. Реактивами, указанными в способе определения, не удается довести рН среды до 4,5 в указанном объеме. Кроме того, для построения калибровочного графика используют водные растворы, а определение алюминия проводится после предварительной минерализации в смеси кислот с последующей нейтрализацией щелочью. Из-за расхождений в условиях измерений результаты анализа оказываются заниженными. Известен также способ минерализации смесью азотной, серной и хлорной кислот. Измельченный биологический материал помещают в колбу Кьельдаля объемом 500 см3. К исследуемому материалу добавляют через воронку по 25 см3 концентрированных азотной, серной кислот и 35 см3 37% или 42% раствора хлорной кислоты на 100 г пробы. Колбу закрепляют в штативе вертикально. Над колбой укрепляют воронку и начинают постепенно нагревать, добавляя по каплям азотную кислоту, сначала концентрированную, затем 35-45% раствор. Минерализацию ведут до тех пор, пока раствор не станет прозрачным (Швайкова М.Д. Токсикологическая химия. – М. – Медицина. – 1975. – С.280-285). Недостатками данного способа являются его трудоемкость и необходимость постоянного контроля количества азотной кислоты. Из известных способов наиболее близким к заявляемому является способ определения алюминия в воде с применением эриохромцианина R, который является самым чувствительным реактивом на ион алюминия. В колбу вместимостью 50 см3 помещают аликвотную часть анализируемой воды, добавляют 0,5 см3 гидроксиламина солянокислого, 3 см3 0,1% эриохромцианина R, 10% раствор NaOH по каплям до фиолетовой окраски, затем по каплям 10% раствор уксусной кислоты до желтой окраски, 10 см3 ацетатной буферной смеси (рН 5,4), доливают дистиллированной воды до метки и перемешивают. Через 20 мин измеряют оптическую плотность раствора при длине волны ( Этот способ не применим к анализу биологических материалов без предварительной пробоподготовки. Целью изобретения является повышение точности, упрощение и ускорение процесса анализа. Поставленная цель достигается тем, что при минерализации образцов в колбу Кьельдаля добавляется сразу смесь концентрированных кислот (азотной, серной и хлорной). Колбу неплотно закрывают стеклянной пробкой и выдерживают при комнатной температуре 15-20 мин. Затем нагревают, не допуская бурного вспенивания. После прекращения выделения бурых паров температуру постепенно повышают и кипятят раствор до полного обесцвечивания. Нагревание в закрытой колбе используют для предотвращения испарения кислот. Этим достигается сокращение времени анализа и расхода реактивов. Затем минерализат количественно переносят в мерную колбу вместимостью 100 см3, добавляют 20 см3 10% раствора NaOH и перемешивают. В колбу вносят 0,5 см3 гидроксиламина солянокислого, 2 см3 0,3% эриохромцианина R, 10% раствор NaOH по каплям до фиолетовой окраски, 10% раствор СН3СООН до желтой окраски, ацетатную буферную смесь, доливают до метки дистиллированной водой и перемешивают. Через 15 мин измеряют оптическую плотность при Использование большего количества эриохромцианина R (ER) объясняется тем, что при избытке ER соотношение компонентов в образующемся комплексе Al:ER равно 1:3. При недостатке ER образуются комплексы с соотношением компонентов 1:1 и 1:2, имеющие такую же окраску, но менее интенсивную. Также при использовании большего количества ER наблюдается меньшее отклонение от закона Бугера. Все вышеперечисленное повышает точность и чувствительность определения. Построение калибровочного графика в условиях, сходных с условиями проведения анализа, дает возможность повысить точность анализа. Использование для минерализации смеси кислот позволяет сократить расход реактивов и время проведения анализа. Минерализация образца в закрытой колбе исключает необходимость постоянного добавления азотной кислоты, что упрощает проведение и сокращает время минерализации. Предлагаемый способ дает возможность осуществить контроль за качеством продуктов животного происхождения при использовании в рационе животных подкормок и ветеринарных препаратов на основе соединений алюминия, а также при случайных отравлениях осуществлять прижизненную и посмертную диагностику токсикоза. Способ обладает достаточно высокой чувствительностью, относительно прост в исполнении, значительно сокращает время минерализации образца за счет использования смеси кислот и кипячения пробы в закрытой колбе. Общие с прототипом признаки: 1. Предварительная минерализация образца. 2. Нейтрализация пробы. 3. Определение алюминия фотоколориметрическим методом с помощью калибровочного графика. Отличительные признаки предлагаемого способа: 1. Минерализацию образца проводят смесью кислот в закрытой колбе. 2. Для построения калибровочного графика используют те же реактивы, в тех же количествах и в той же последовательности, начиная с момента минерализации, которые применяются для проведения анализа; Способ осуществляют следующим образом. Пример. Навеску мышечной ткани, печени, почек или других органов берут на обеззоленный фильтр, заворачивают в него и помещают на дно колбы Кьельдаля. В колбу с пробой вносят 10 см3 концентрированной азотной кислоты, 3 см3 концентрированной серной кислоты и 3 см3 40% хлорной кислоты на каждые 5 г навески и выдерживают 15-20 мин при комнатной температуре. Затем колбу закрывают грушевидной стеклянной пробкой и начинают нагревать на электроплитке, покрытой асбестом, сначала слабо, не допуская вспенивания и выплескивания образца. После бурного выделения паров NO2 (через 10-15 мин) нагрев постепенно увеличивают и кипятят до полного обесцвечивания пробы. Минерализация считается законченной, когда раствор в колбе станет бесцветным и над поверхностью появятся пары серного ангидрида. Колбу с раствором охлаждают. Минерализат количественно переносят дистиллированной водой в мерную колбу вместимостью 100 см3 и добавляют 20 см3 10% раствора NaOH. В колбу вносят 0,5 см3 10% раствора гидроксиламина солянокислого, 2 см3 0,3% эриохромцианина R, 10% раствор NaOH по каплям до фиолетовой окраски, 10% раствор СН3СООН по каплям до желтой окраски, 10 см3 ацетатного буферного раствора (рН 5,4), доводят до метки дистиллированной водой и перемешивают. Через 15 мин измеряют оптическую плотность раствора на спектрофотометре или фотоколориметре при Содержание алюминия (X в мг/кг) вычисляют по формуле где А – количество алюминия, найденное по калибровочному графику, мкг; М – масса образца, взятого для исследования, г. Чувствительность метода составляет 5 мкг в 100 см3 пробы. Метрологическая характеристика способа представлена в таблице (С.6).
Формула изобретения
Способ определения алюминия в биологических объектах, заключающийся в минерализации анализируемого образца азотной, серной и хлорной кислотами, выдерживании смеси при комнатной температуре, кипячении до полного ее обесцвечивания, охлаждении, нейтрализации, добавлении реакционной ацетатной буферной смеси, с последующим измерением оптической плотности и определением концентрации алюминия по калибровочному графику, отличающийся тем, что для минерализации образца азотную, серную и хлорную кислоту добавляют к образцу одновременно, смесь выдерживают при комнатной температуре 15-20 мин, затем нагревают в закрытой колбе при постепенном повышении температуры, смесь кипятят до полного обесцвечивания, используют ацетатную буферную смесь, содержащую 10%-ный раствор гидроксиламина солянокнслого, 0,3% эриохромцианина R, 10%-ные растворы NaOH и СН3СООН при рН 5,4, а измерение оптической плотности проводят при длине волны
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 23.12.2005
Извещение опубликовано: 20.02.2007 БИ: 05/2007
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 =535 нм. Технический результат – повышение точности, упрощение и ускорение процесса анализа. 1 табл.
=535 нм. Технический результат – повышение точности, упрощение и ускорение процесса анализа. 1 табл. 12H2O с содержанием алюминия 1 мкг/см3. В колбы Кьельдаля вносят 10 см3 концентрированной азотной кислоты, 3 см3 концентрированной серной кислоты и 3 см3 40% хлорной кислоты. Колбы ставят на электрическую плитку, покрытую асбестом, и кипятят, упаривая содержимое до объема 3-5 см3. Остывшие растворы количественно переносят в мерные колбы вместимостью 100 см3 и добавляют 20 см3 10% раствора NaOH. В каждую колбу вносят 0,0; 1,0; 3,0; 5,0; 10,0; 15,0; 20,0; 25,0; 30,0 см3 рабочего раствора, 0,5 см3 10% гидроксиламина солянокислого, 2 см3 0,3% эриохромцианина R, 10% раствор NaOH по каплям до фиолетовой окраски, 10% раствор СН3СООН по каплям до желтой окраски, 10 см3 ацетатного буферного раствора (рН 4,5). Содержимое колб доводят до метки дистиллированной водой, перемешивают и через 15 мин измеряют оптическую плотность при
12H2O с содержанием алюминия 1 мкг/см3. В колбы Кьельдаля вносят 10 см3 концентрированной азотной кислоты, 3 см3 концентрированной серной кислоты и 3 см3 40% хлорной кислоты. Колбы ставят на электрическую плитку, покрытую асбестом, и кипятят, упаривая содержимое до объема 3-5 см3. Остывшие растворы количественно переносят в мерные колбы вместимостью 100 см3 и добавляют 20 см3 10% раствора NaOH. В каждую колбу вносят 0,0; 1,0; 3,0; 5,0; 10,0; 15,0; 20,0; 25,0; 30,0 см3 рабочего раствора, 0,5 см3 10% гидроксиламина солянокислого, 2 см3 0,3% эриохромцианина R, 10% раствор NaOH по каплям до фиолетовой окраски, 10% раствор СН3СООН по каплям до желтой окраски, 10 см3 ацетатного буферного раствора (рН 4,5). Содержимое колб доводят до метки дистиллированной водой, перемешивают и через 15 мин измеряют оптическую плотность при 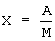
 =0,05, %
=0,05, %