|
|
(21), (22) Заявка: 2003134826/13, 02.12.2003
(24) Дата начала отсчета срока действия патента:
02.12.2003
(43) Дата публикации заявки: 10.05.2005
(45) Опубликовано: 20.10.2005
(56) Список документов, цитированных в отчете о
поиске:
US 6537797, 31.03.2000. US 4999300, 28.03.1988. RU 2155803, 10.09.2000. RU 2155804, 10.09.2000. WO 0136593, 25.05.2001.
Адрес для переписки:
614081, г.Пермь, ул. Голева, 13, Институт экологии и генетики микроорганизмов УрО РАН
|
(72) Автор(ы):
Плотникова Е.Г. (RU),
Рыбкина Д.О. (RU),
Демаков В.А. (RU)
(73) Патентообладатель(и):
Институт экологии и генетики микроорганизмов УрО РАН (RU)
|
(54) ШТАММ БАКТЕРИЙ RHODOCOCCUS RUBER – ДЕСТРУКТОР ПОЛИХЛОРИРОВАННЫХ БИФЕНИЛОВ
(57) Реферат:
Изобретение относится к биотехнологии, а именно к очистке окружающей среды. Предлагается штамм бактерий, относящийся к виду Rhodococcus ruber, обладающий высокой разрушающей активностью в отношении полихлорированных бифенилов. Штамм депонирован в Региональной профилированной коллекции алканотрофных микроорганизмов Института экологии и генетики микроорганизмов УрО РАН с коллекционным номером ИЭГМ 896. Штамм отличается способностью эффективно расти на 2-, 4-, и 2,4′-хлорбифенилах и продуктах метаболизма полихлорбифенилов – 2-, 4- и 2,4-хлорбензойных кислотах. В процессе роста разлагает 2,2′-, 4,4′-дихлорбифенилы, 2,4,2′-, 2,4,4′-трихлорбифенилы. Штамм может быть выращен промышленным способом с использованием стандартного оборудования с применением доступного сырья. Изобретение может служить основой для получения биопрепаратов для очистки почв, содержащих высокие концентрации полихлорированных бифенилов. 2 ил., 3 табл. 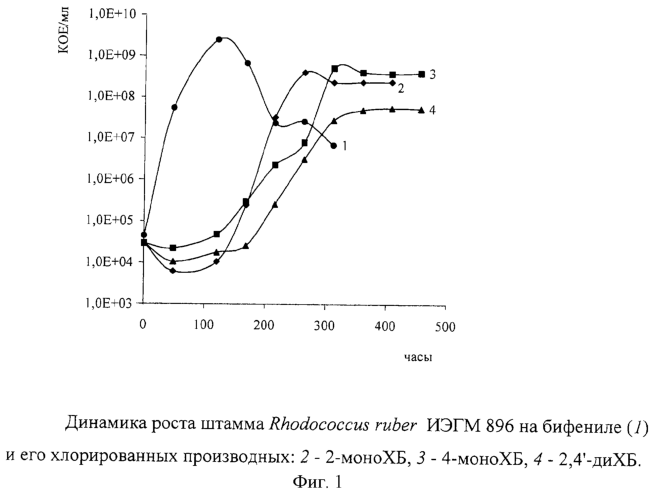
Изобретение относится к биотехнологии, а именно к очистке окружающей среды от загрязнения полихлорированными бифенилами (ПХБ) при помощи микроорганизмов, и касается получения нового штамма бактерий, способного эффективно разлагать ПХБ. Полихлорированные бифенилы относятся к ряду распространенных загрязнителей, являются токсичными и устойчивыми соединениями, которые аккумулируются в почве, донных отложениях. Эффективным способом очистки почв и водоемов от ПХБ является биоремедиация с помощью микроорганизмов. Однако большинство изученных и описанных в научной литературе микроорганизмов трансформируют ПХБ только до хлорбензойных кислот (ХБК), которые также являются токсичными и устойчивыми соединениями (Unterman R., в книге под ред. Crawford R.L., Crawford D.L.: Bioremediation. Principles and Applications, 1996, pp.209-253).
Известно лишь несколько природных бактериальных штаммов, способных расти на монохлорбифенилах (2-, 3- и 4-хлорбифенилах), использующих такие соединения в качестве единственного источника углерода и энергии:
– Pseudomonas sp. MB86 растет на 4-хлорбифениле, разлагая 4-хлорбифенил до 4-хлорацетофенона (патент US №4,999,300);
– Pseudomonas cepacia P166 утилизирует монохлорбифенилы через хлоркатехолы, которые оказывают токсический эффект на рост штамма (Arensdorf, Focht, 1995, Appl. Environ. MicrobioL, 61:443-447).
В качестве прототипа нами выбран штамм Burkcholderia sp. SK-3, способный использовать в качестве ростового субстрата 4-хлорбифенил и 2,4′-дихлорбифенил (патент US №6,537,797). При росте на 4-хлорбифениле штамм Burkcholderia sp. SK-3 осуществляет частичную трансформацию данного хлорбифенила в 4-хлорбензойную кислоту, которая полностью утилизируется штаммом. Также штамм Burkholderia sp. SK-3 способен к слабому росту на 2,4′-дихлорбифениле при концентрации 0.27 mM.
Цель изобретения – получение штамма бактерий, способного осуществлять эффективное разложение полихлорированных бифенилов до продуктов основного обмена микробной клетки.
Сущность изобретения: получение нового штамма бактерий, способного эффективно расти на 2-, 4- и 2,4′-хлорбифенилах и продуктах метаболизма полихлорбифенилов – 2-, 4- и 2,4-хлорбензойных кислотах, используя данные соединений в качестве единственного источника углерода и энергии.
Штамм выделен из почвы, загрязненной отходами химического производства, выпускающего широкий ассортимент галогенсодержащих органических соединений. Выделение штамма осуществлялось общепринятыми методами (методом накопительных культур и методом выделения чистых культур микроорганизмов) на минеральной среде К1 (Зайцев Г.М., Карасевич Ю.Н., 1981, Микробиология, 50:35-40) с использованием бифенила в качестве единственного источника углерода и энергии.
Штамм характеризуется следующими культурально-морфологическими, физиолого-биохимическими и хемотаксономическими признаками.
При росте на агаризованной среде штамм образует круглые колонии с блестящей поверхностью оранжево-красного цвета на полноценной среде и розово-оранжевого цвета на минеральных средах.
Клетки грамположительные, неподвижные, неспорообразующие, аэробные, имеют цикл развития: клетки культур 16-20 часового возраста длинные (0.8-1.2×16-19 мкм), обильно ветвящиеся, к 28-30 часам роста отмечено фрагментирование нитей, культуры 48-64 часового возраста представлены кокковидными овальными клетками (длиной 1-4 мкм).
Биохимические свойства штамма представлены в таблице 1.
Штамм растет на этаноле, моноэтаноламине, но не на L-аспарагине. Образует кислоту при росте на большинстве углеводов, многоатомных спиртов (таблица 2).
Штамм усваивает Na-соли уксусной, пропионовой, бутановой, пировиноградной, бензойной кислот, но не растет на Na-солях винной, муравьиной,  -кетоглутаровой кислот. -кетоглутаровой кислот.
Клеточная стенка содержит липид LCN-A типа Rhodococcus ruber. Основная аминокислота клеточной стенки – мезо-ДАПК (мезодиаминопимеленовая кислота), сахара клеточной стенки – арабиноза, галактоза.
Чувствительность к антибактериальным препаратам.
Штамм чувствителен к неомицину, стрептомицину, ристомицину, левомицетину.
Патогенность: штамм не патогенный.
На основании перечисленных характеристик штамм отнесен к виду Rhodococcus ruber. Штамм депонирован в Региональной профилированной коллекции алканотрофных микроорганизмов Института экологии и генетики микроорганизмов УрО РАН под названием Rhodococcus ruber с коллекционным номером ИЭГМ 896.
Изобретение может быть использовано в очистке объектов окружающей среды (почв, отвалов, донных отложений, захоронений отходов промышленных предприятий) от загрязнения полихлорированными бифенилами и хлорированными бензойными кислотами.
| Таблица 1 |
| Биохимические свойства штамма |
Активность |
| Каталаза |
++++ |
| Оксидаза |
++++ |
| Фосфатаза |
+ |
| Разжижение желатина |
– |
| Разложение тирозина |
++ |
| Амилаза (разложение крахмала) |
– |
| Липаза |
– |
| Ацетамидаза |
+++ |
| Никотинамидаза |
+++ |
| Денитрификация |
– |
| Восстановление NO3 – до NO2 – |
+++ |
| Образование H2S |
++ |
| Образование индола |
– |
| Целлюлолитическая активность |
– |
| O/F тест (глюкоза): аэробное окисление |
+++ |
| Брожение |
+ |
| (+ – ++++) – степень активности, (-) – отсутствие активности. |
| Таблица 2 |
| Углеводы и многоатомные спирты: |
Рост |
Образование кислот |
| Глюкоза |
+++ |
++++ |
| Арабиноза |
+++ |
++++ |
| Ксилоза |
+++ |
++++ |
| Лактоза |
+ |
– |
| Мальтоза |
+++ |
++++ |
| Рамноза |
+++ |
++ |
| Раффиноза |
+++ |
– |
| Сахароза |
+ |
– |
| Глицерин |
+++ |
++ |
| Дульцит |
– |
– |
| Манит |
+++ |
++++ |
| Сорбит |
+++ |
+ |
| (+ – ++++) – степень активности, (-) – отсутствие активности. |
Культура используемого в данном изобретении штамма бактерий Rhodococcus ruber ИЭГМ 896 может быть выращена на простых микробиологических средах, включающих различные источники углерода, азота, органические и неорганические соли, которые обычно используются для получения биомассы бактерий.
Деградативные активности в отношении полихлорированных бифенилов штамма проверяли путем анализа ростовых характеристик при выращивании штамма на индивидуальных хлорбифенилах и хлорбензоатах, а также в опытах с «отмытыми» клетками путем обнаружения продуктов метаболизма ПХБ (методом спектрофотометрии и методом высокоэффективной жидкостной хроматографии).
Пример 1. Кинетику роста штамма изучали в периодической культуре при выращивании в жидкой минеральной среде следующего состава: К2HPO4×3Н2О – 4 г/л, NaH2PO4×2Н2О – 0.4 г/л, (NH4)2SO4 – 0.5 г/л, Са(NO3)2 – 0.01 г/л, MgSO4×7Н2О – 0.15 г/л, NaMoO4×2Н2О – 4.0 г/л (рН среды – 7.3), на бифениле, хлорбифенилах и 2-, 4-, 2,4-хлорбензоатах, которые использовались в качестве единственного источника углерода и энергии. Культивирование проводили в колбах на 250 мл (объем среды – 100 мл) при 28°С, аэрация на шейкере при 100 об/мин. Бифенил вносили в виде порошка (1 г/л), а хлорбифенилы и хлорбензоаты – в виде растворов до конечной концентрации 0.5 г/л и 1 г/л, соответственно. В качестве инокулята использовали культуру, выращенную на минеральной среде (состав среды смотри выше) с бифенилом или с соответствующей хлорбензойной кислотой. Начальная концентрация бактерий в колбах составляла 4-5×104 кл/мл. Оптическую плотность (ОД) определяли фотометрически при длине волны 540 нм. Количество колониеобразующих единиц (КОЕ) определяли методом стандартных серийных разведений с последующим высевом и подсчетом колоний микроорганизмов на чашках с агаризованной средой LB (5 г/л дрожжевого экстракта, 10 г/л триптона, 10 г/л хлорида натрия, 15 г/л агара Difco).
Штамм Rhodococcus ruber ИЭГМ 896 способен использовать в качестве единственного источника углерода и энергии 2-, 4- и 2,4′-хлорбифенилы, а также продукты метаболизма данных хлорбифенилов -2- и 4-хлорбензоаты. В процессе роста на 2- и 4-хлорбензоатах в среде отмечено накопление эквимолярного количества свободных ионов хлора и снижение концентрации субстрата, что свидетельствует об отсутствии токсичных метаболитов. Рост штамма на данных соединениях представлен на фиг. 1 и 2.
Таким образом, штамм Rhodococcus ruber ИЭГМ 896 способен полностью утилизировать 2-, 4- и 2,4′-хлорбифенилы в концентрации 0.5 г/л (0.5 г/л 2,4′-диХБ соответствует 2.25 mM данного хлорбифенила) и является более активным деструктором, чем штамм Burkholderia sp. SK-3.
Пример 2. Продукты деградации хлорбифенилов определяли спектрофотометрически и методом высокоэффективной жидкостной хроматографии (ВЭЖХ). Штаммы выращивали в жидкой минеральной среде (состав среды: К2HPO4×3Н2O – 4 г/л, NaH2PO4×2H2O – 0.4 г/л, (NH4)2SO4 – 0.5 г/л, Ca(NO3)2 – 0.01 г/л, MgSO4×7Н2O – 0.15 г/л, NaMoO4×2H2O – 4.0 г/л, рН среды – 7.3) с бифенилом (1 г/л) при 28°С до ОД600=1.0. Отмытые клетки (1 мл, ОД600=2.0) переносили во флаконы с тефлоновыми крышками. Монохлорбифенилы добавляли до конечной концентрации 500 мкМ (94.25 мг/л), дихлорбифенилы – 100 мкМ (22.3 мг/л), трихлорбифенилы – 50 мкМ (12.8 мг/л). Флаконы встряхивали на шейкере при температуре 28°С и 100 об/мин. Образование продукта мета-расщепления хлорбифенилов (2-гидрокси-6-оксо-6-фенилгексадиеновой кислоты) определяли спектрофотометрически при  max от 390 нм до 450 нм. Содержание хлорбензоатов в среде культивирования регистрировали методом высокоэффективной жидкостной хроматографии. Идентификацию продуктов метаболизма проводили при сравнении «времени выхода» пиков образовавшихся соединений со стандартами. В качестве стандартов использовались растворы 2ХБК, 4ХБК, 2,4ДХБК в концентрациях 1 г/л, 100 мкМ, 20 мкМ. max от 390 нм до 450 нм. Содержание хлорбензоатов в среде культивирования регистрировали методом высокоэффективной жидкостной хроматографии. Идентификацию продуктов метаболизма проводили при сравнении «времени выхода» пиков образовавшихся соединений со стандартами. В качестве стандартов использовались растворы 2ХБК, 4ХБК, 2,4ДХБК в концентрациях 1 г/л, 100 мкМ, 20 мкМ.
Динамику дегалогенирования хлорбифенилов определяли измерением оптической плотности раствора хлорида серебра, образующегося после реакции ионов хлора с азотнокислым серебром, при 460 нм и 540 нм в культуральной жидкости, освобожденной от клеток.
Штамм Rhodococcus ruber ИЭГМ 896 осуществляет деструкцию различных орто- и пара-хлорированных бифенилов, в том числе 2,2′-, 4,4′-дихлорбифенилов, 2,4,2′- и 2,4,4′-трихлорбифенилов. Данные по деструкции ПХБ приведены в таблице 3.
Таблица 3
Деструкция хлорбифенилов штаммом Rhodococcus ruber ИЭГМ 896 |
| ПХБ |
Концентрация ПХБ (мг/л) |
Время инкубации (час) |
Концентрация ионов хлора (мг/л) |
Хлорбензойная кислота |
ГОФДК |
| Положение хлора |
Концентрация |
 max max |
ОД |
| мг/л |
%* |
| 2-моно-ХБ |
94.25 |
0 |
н.о. |
2 |
– |
– |
395 |
0.13±0.02 |
| |
5 |
|
|
26.61±0.2 |
34.0 |
|
0.69±0.03 |
| |
24 |
|
|
60.25±0.4 |
77.0 |
|
0.25±0.01 |
| 4-моно ХБ |
94.25 |
0 |
н.о. |
4 |
1.09±0.02 |
1.4 |
434 |
0.05±0.01 |
| |
5 |
|
|
51.65±0.1 |
66.0 |
|
0.52±0.02 |
| |
24 |
|
|
32.08±0.08 |
41.0 |
|
0.57±0.04 |
| 2,2′-диХБ |
22.3 |
0 |
– |
2 |
– |
– |
– |
– |
| |
24 |
4.3±0.2 |
|
2.22±0.07 |
14.2 |
|
– |
| |
48 |
7.8±0.2 |
|
н.о. |
н.о. |
|
– |
| 2,4′-диХБ |
22.3 |
0 |
– |
4 |
– |
– |
397 |
<0.1 |
| |
24 |
4.6±0.5 |
|
5.77±0.03 |
36.9 |
|
0.52±0.07 |
| |
48 |
6.8±0.3 |
|
1.05±0.02 |
6.77 |
|
0.39±0.03 |
| 4,4′-диХБ |
22.3 |
0 |
– |
4 |
– |
– |
434 |
0.06±0.01 |
| |
24 |
2.8±0.3 |
|
10.64±0.04 |
68.0 |
|
0.38±0.02 |
| |
48 |
7.010.2 |
|
1.88±0.02 |
12.0 |
|
0.411±0.07 |
| 2,4,2′-три-ХБ |
12.8 |
0 |
0 |
2 |
– |
– |
– |
– |
| |
5 |
<2.0 |
|
0.79±0.01 |
10.2 |
|
– |
| |
24 |
2.2±0.3 |
|
2.91±0.02 |
37.4 |
|
– |
| 2,4,4′-триХБ |
12.8 |
0 |
0 |
2,4 |
– |
– |
396 |
0.1 |
| |
5 |
<2.0 |
|
4.75±0.04 |
49.9 |
|
0.82±0.03 |
| |
24 |
<2.0 |
|
5.55±0.03 |
58.5 |
|
0.71±0.02 |
| Примечание: н.о. – не определяли, “-” – не зафиксировано, *% от теоретически возможного. |
Таким образом, штамм Rhodococcus ruber ИЭГМ 896 может служить основой для получения биопрепаратов для очистки почв и водоемов, содержащих высокие концентрации полихлорированных бифенилов и хлорбензойных кислот.
Формула изобретения
Штамм бактерий Rhodococcus ruber ИЭГМ 896 – деструктор полихлорированных бифенилов.
РИСУНКИ
|
|