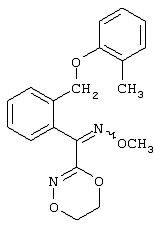
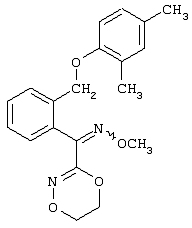
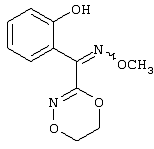
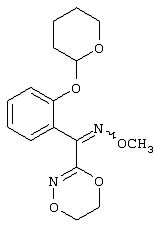
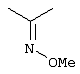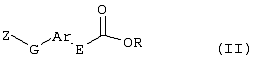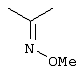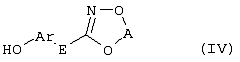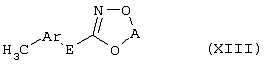Патент на изобретение №2258066
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ЗАМЕЩЕННЫЕ АЗАДИОКСОЦИКЛОАЛКЕНЫ, СПОСОБЫ ИХ ПОЛУЧЕНИЯ, ПРОМЕЖУТОЧНЫЕ ПРОДУКТЫ, ФУНГИЦИДНЫЕ СРЕДСТВА И СПОСОБ ИХ ПОЛУЧЕНИЯ, СПОСОБ БОРЬБЫ С НЕЖЕЛАТЕЛЬНЫМИ ГРИБАМИ
(57) Реферат:
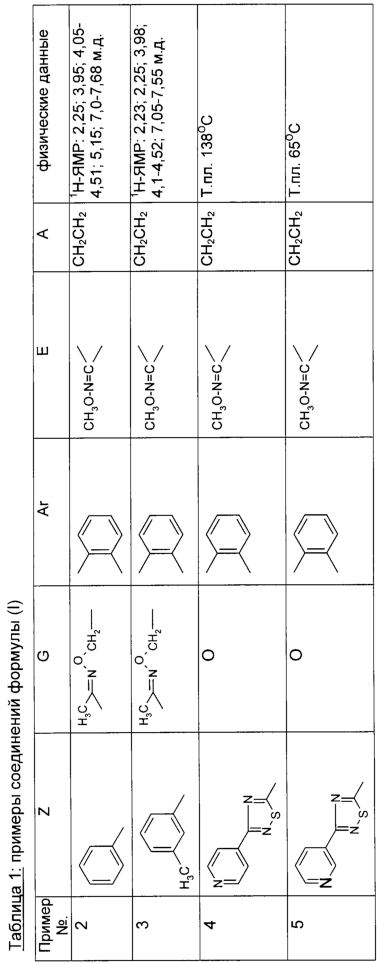
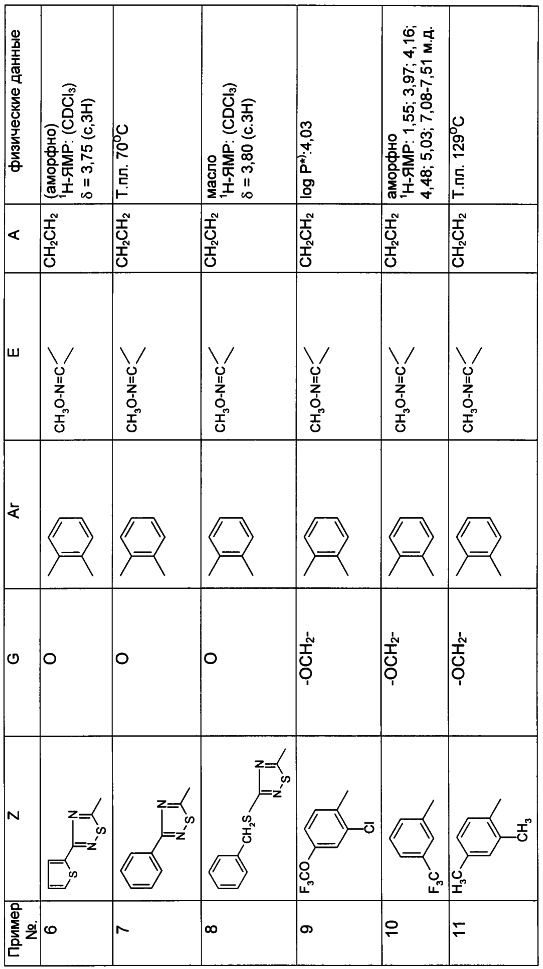
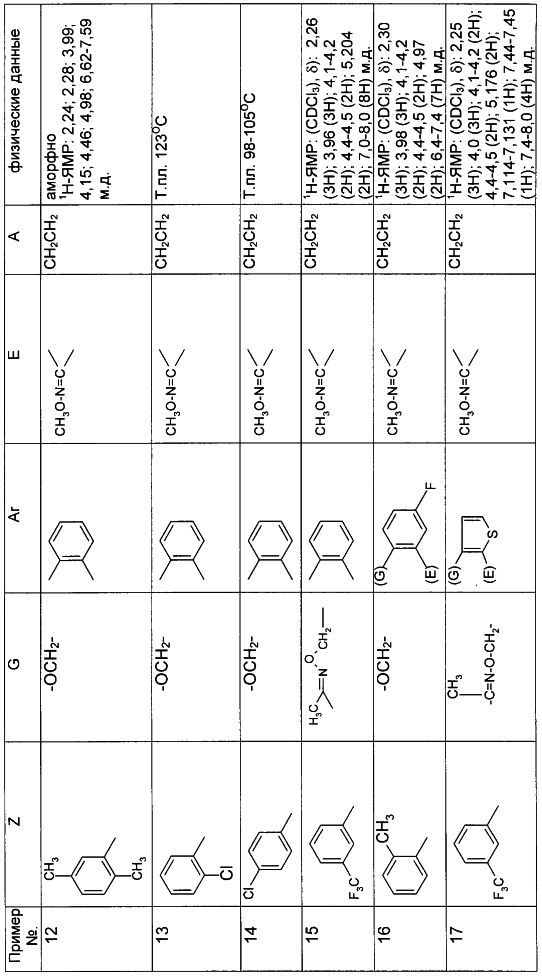
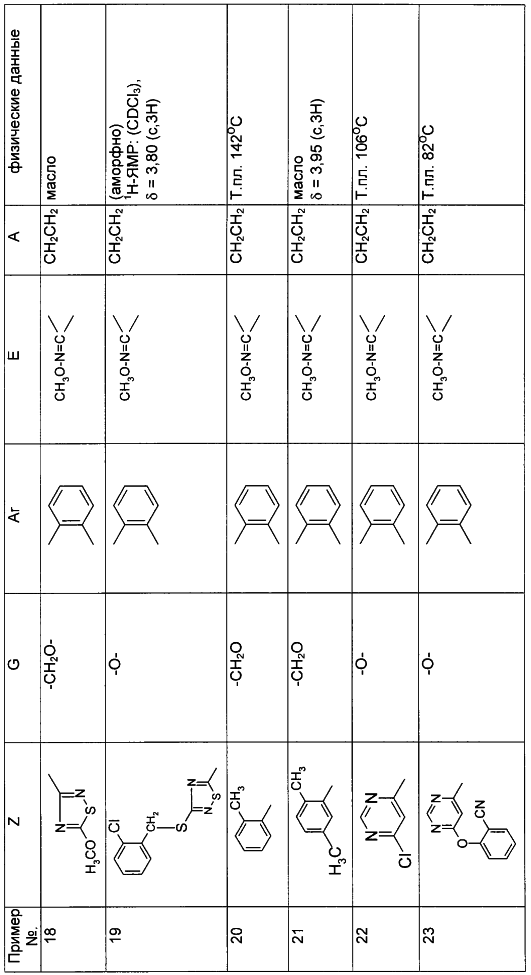
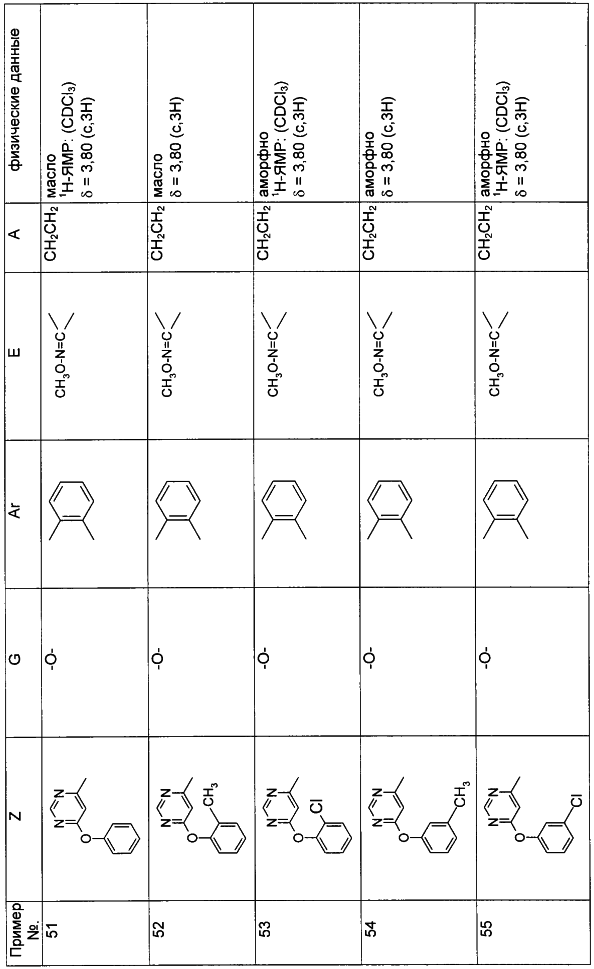
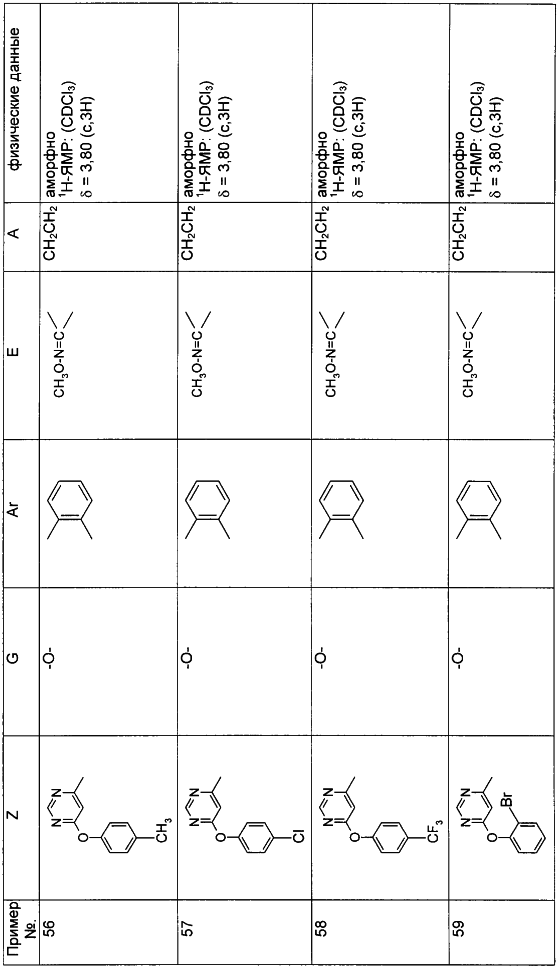
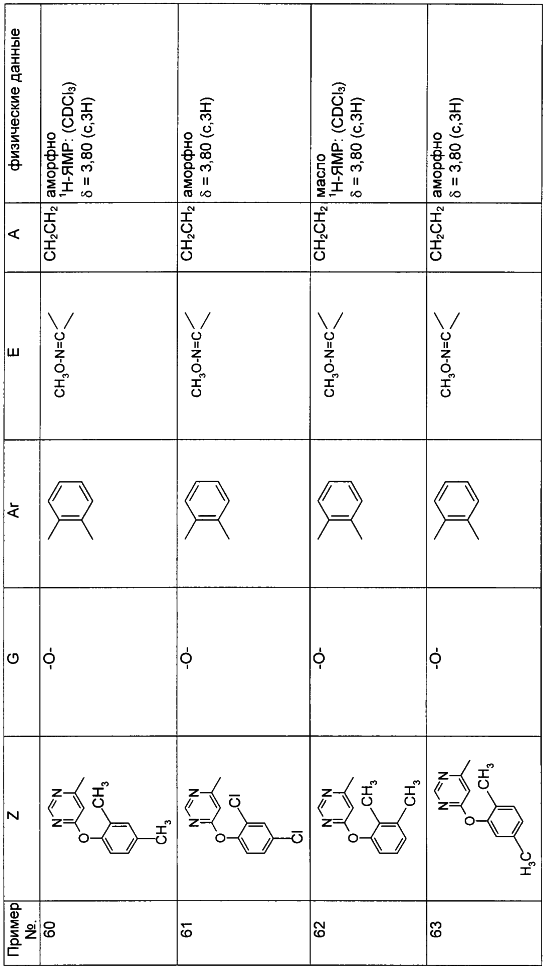
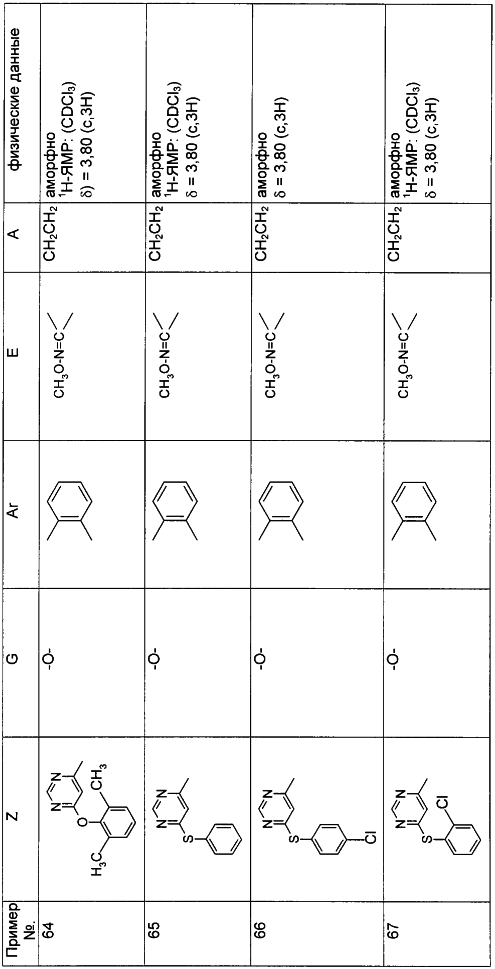
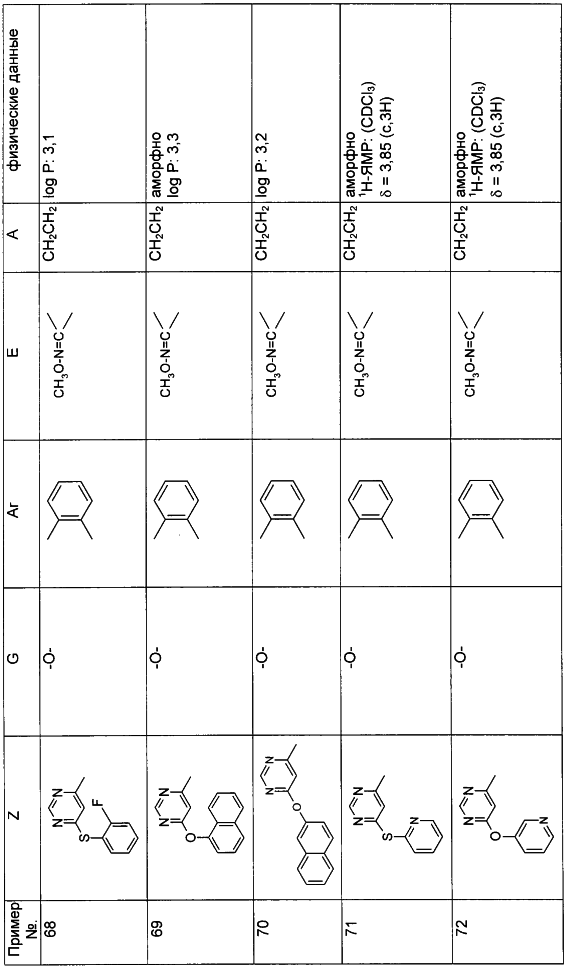
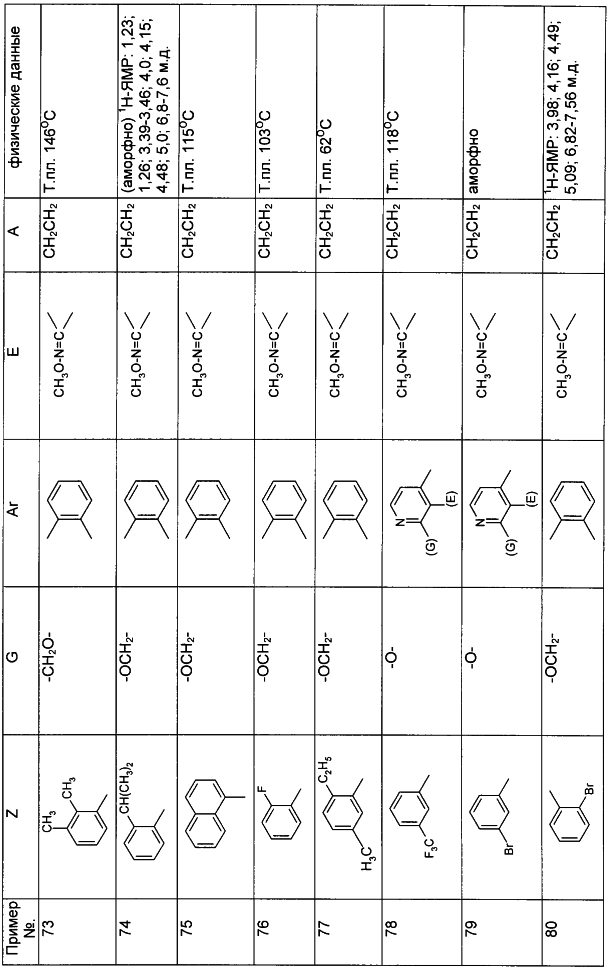
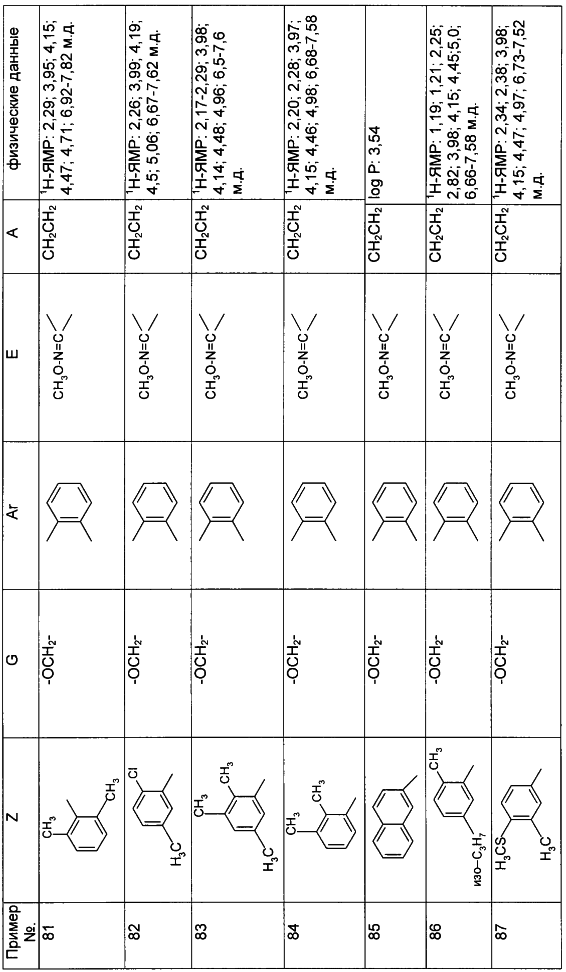
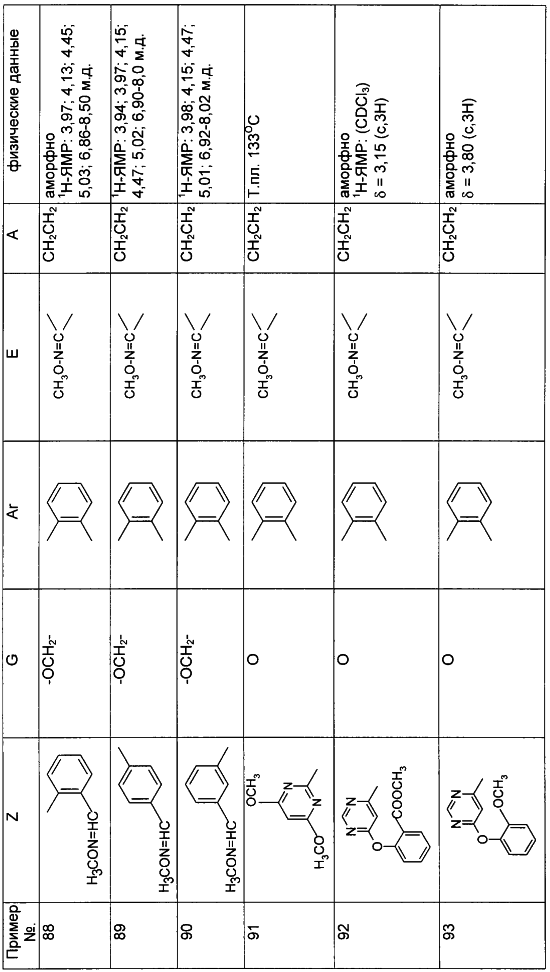
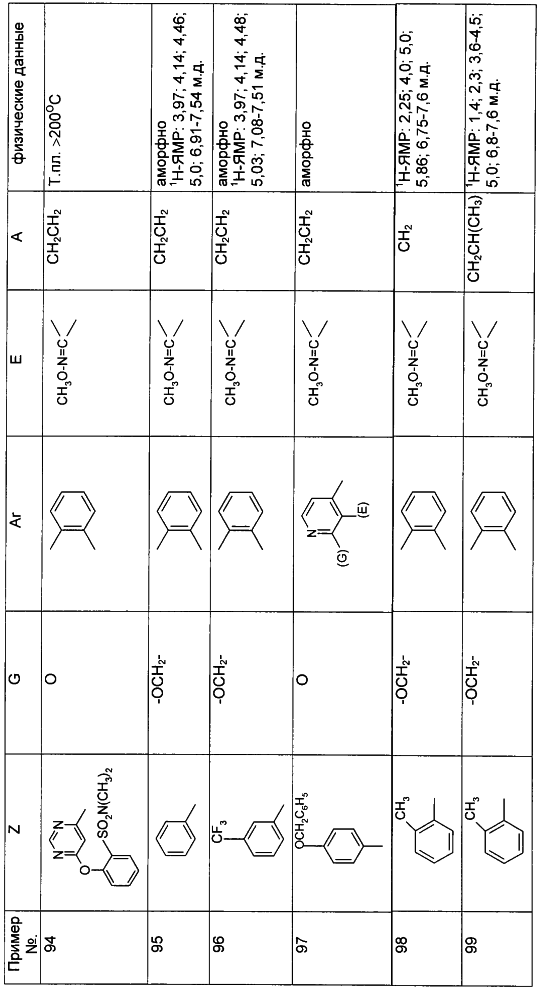
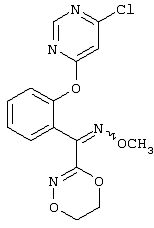
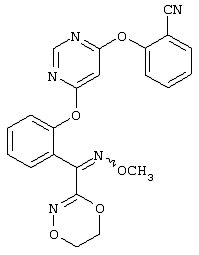
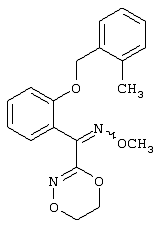
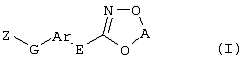
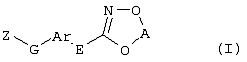
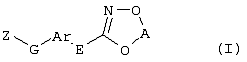
Описываются замещенные азадиоксоциклоалкены общей формулы (I) где А – диметилен, незамещенный или замещенный метилом, Ar – орто-фенилен, незамещенный или замещенный фтором, тиофендиил или пиридиндиил, Е – группа формулы G – кислород, группы -О-СН2-, -СН2-О- или -С(СН3)=N-O-СН2-, Z – фенил, пиримидинил или тиадиазолил, незамещенные или замещенные, или нафтил. Описываются 4 способа получения соединений формулы (I), 5 видов промежуточных продуктов для получения соединений формулы (I), фунгицидные средства, содержащие в качестве активного вещества соединение формулы (I), способ получения фунгицидных средств, способ борьбы с нежелательными грибами, использующий соединение формулы (I). Технический результат – соединения формулы (I) проявляют фунгицидные свойства, что позволяет использовать их в сельском хозяйстве. 13 н.п. ф-лы, 5 табл.
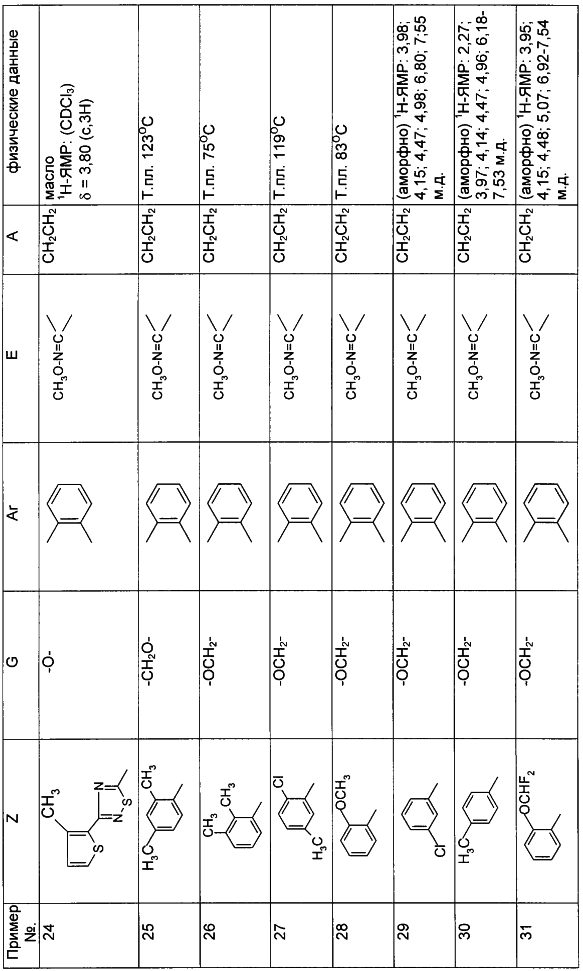
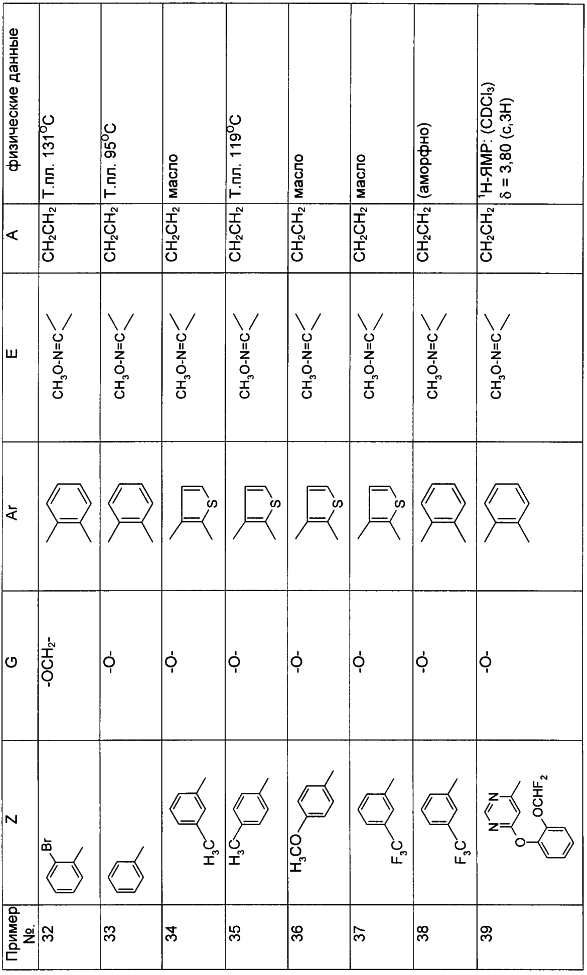
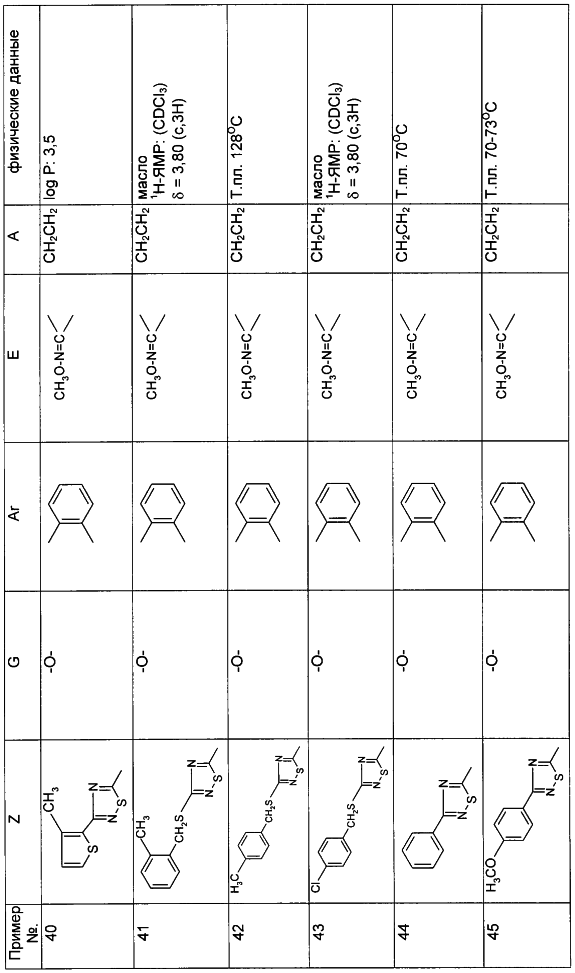
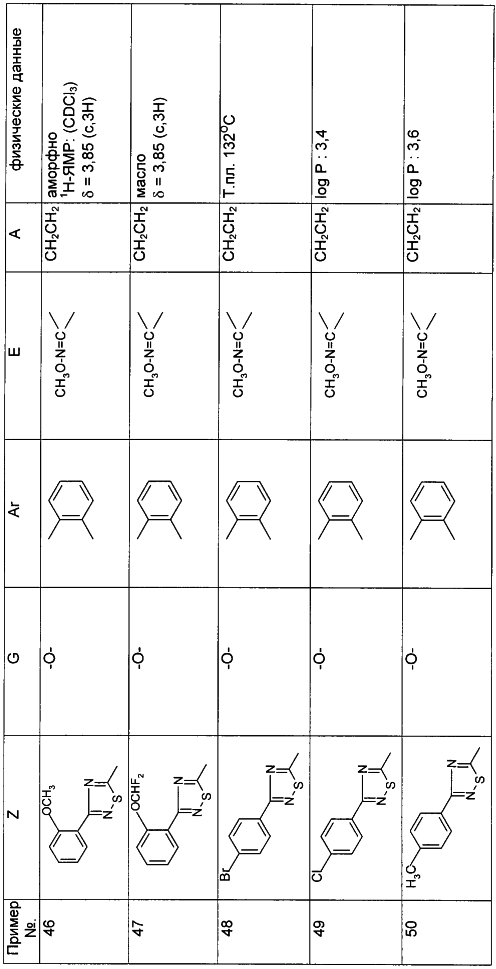
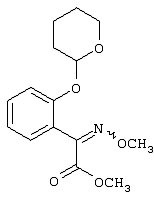
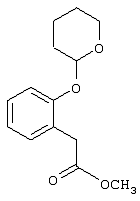
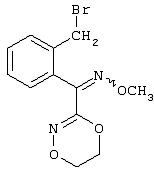
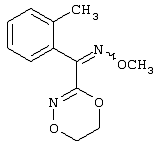
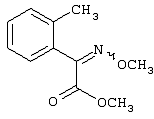
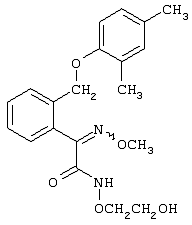
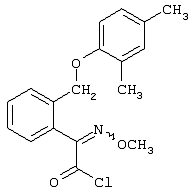
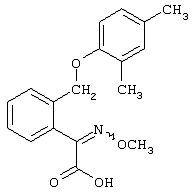
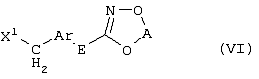
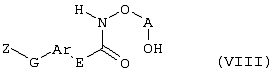
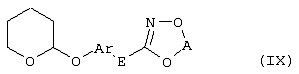
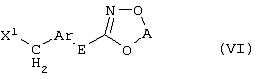
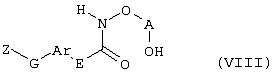
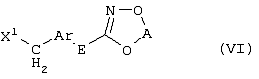
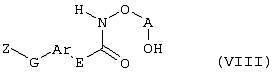
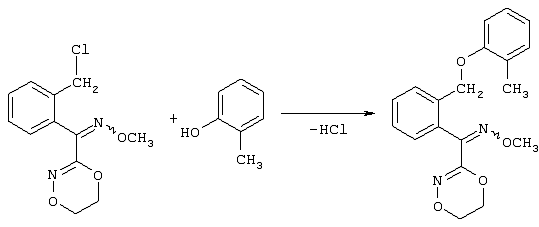
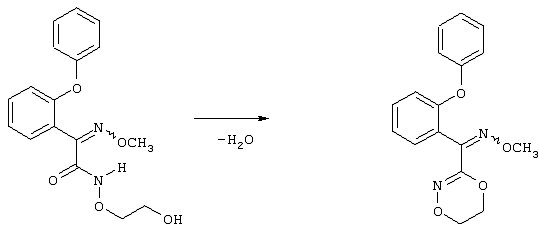
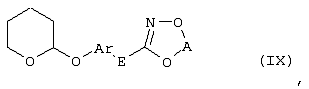
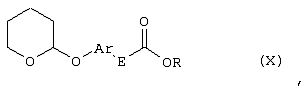
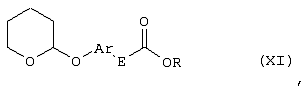
Настоящее изобретение относится к новым замещенным диоксазинам, обладающим фунгицидной активностью, более конкретно к замещенным азадиоксоциклоалкенам, способам их получения, промежуточным продуктам, фунгицидным средствам и способу их получения. Известны замещенные 5,6-дигидро-1,4,2-диоксазины, обладающие фунгицидной активностью (см. JP-A-02001484 или Chemical Abstracts, vol.113, №.1, 02.07.1990, abstract №.6381 у). Задачей изобретения является расширение ассортимента замещенных диоксазинов, проявляющих фунгицидную активность. Поставленная задача решается предлагаемыми замещенными азадиоксоциклоалкенами общей формулы (I) где А – диметилен (этан-1,2-диил), незамещенный или замещенный метилом, Ar – орто-фенилен, незамещенный или замещенный фтором, тиофендиил или пиридиндиил, Е – группа формулы G – кислород, группы -O-СН2-, -CH2-O- или -С(СН3)=N-O-СН2-, Z – фенил, пиримидинил или тиадиазолил, незамещенные или одно- или двукратно замещенные заместителями из группы, включающей метил, этил, н- или изопропил, н-, изо-, втор- или трет.бутил, метокси, этокси, трифторметил, трифторметокси, дифторметокси, фтор, хлор, бром, метилтио, этилтио, Н3С-O-N=СН-, бензилокси, нафтилокси, пиридинил, пиридинилтио, пиридинилокси, бензилтио, незамещенный или замещенный хлором или метилом, тиенил, незамещенный или замещенный метилом, фенил, незмещенный или замещенный 1 или 2 одинаковыми или различными заместителями из группы, включающей метил, этил, метокси, этокси, дифторметилокси, трифторметил, фтор, хлор и бром, фенокси-группу, незамещенную или замещенную 1 или 2 одинаковыми или различными заместителями из группы, включающей фтор, хлор, бром, циано, метил, метокси, этил, дифторметилокси, трифторметил, метокси-карбонил и диметиламиносульфонил, и фенилтио-группу, незамещенную или замещенную однократно фтором, хлором или бромом, или Z означает нафтил. Замещенные азадиоксациклоалкены вышеприведенной общей формулы (I), где А, Ar, Е, G и Z имеют вышеуказанные значения, можно получать за счет того, что производные карбоновой кислоты общей формулы (II) где Ar, Е, G и Z имеют вышеуказанные значения, a R представляет собой C1-C4-алкил, подвергают взаимодействию с гидроксиламином или его галоидводородной солью, при необходимости, в присутствии акцептора кислоты и, при необходимости, в присутствии разбавителя, полученный продукт подвергают взаимодействию с двузамещенными алканами общей формулы (III) где А имеет вышеуказанное значение, Х – галоген, алкилсульфонилокси или фенилсульфонилокси; при необходимости, в присутствии акцептора кислоты и, при необходимости, в присутствии разбавителя, с последующим выделением целевого продукта. В нижеследующем данный способ обозначается как способ а). Замещенные азадиоксоциклоалкены вышеприведенной общей формулы (I), где А означает диметилен (этан-1,2-диил), Ar означает орто-фенилен, Е означает группу формулы G означает кислород или группу -CH2-O- и Z означает фенил, пиримидинил, замещенные метилом, этилом, фтором, хлором, бромом, феноксигруппу, замещенную циано, можно получать за счет того, что что гидроксиариловые соединения общей формулы (IV) где А, Ar и Е имеют вышеуказанные значения, подвергают взаимодействию с соединениями общей формулы (V) где Z имеет вышеуказанные значения, m означает 0 или 1, а Х означает галоген, при необходимости, в присутствии акцептора кислоты и, при необходимости, в присутствии разбавителя, с последующим, в случае необходимости, переведением группы Z в желаемое значение и выделением целевого продукта. В нижеследующем данный способ обозначается как способ б). Замещенные азадиоксоциклоалкены вышеприведенной общей формулы (I), где А означает диметилен (этан-1,2-диил), Ar означает орто-фенилен, Е означает группу формулы G – группа -СН2-O-, Z – фенил, замещенный метилом или этилом, можно получать за счет того, что галогенметиловые соединения общей формулы (VI) где А, Ar и Е имеют вышеуказанные значения, а X1 означает галоген, подвергают взаимодействию с соединениями общей формулы (VII) где Z имеет вышеуказанное значение, при необходимости, в присутствии акцептора кислоты и, при необходимости, в присутствии разбавителя, с последующим выделением целевого продукта. В нижеследующем данный способ обозначается как способ в). Замещенные азадиоксоциклоалкены вышеприведенной общей формулы (I), где А означает диметилен (этан-1,2-диил), Ar означает орто-фенилен, Е означает группу формулы G – группа -СН2-O-, Z – фенил, замещенный метилом или этилом, можно получать за счет того, что гидроксиалкиламиды общей формулы (VIII) где А, Ar, Е, G и Z имеют вышеуказанные значения, подвергают циклизации водоудаляющим средством, при необходимости, в присутствии разбавителя, с последующим выделением целевого продукта. В нижеследующем данный способ обозначается как способ г). Проведение способов а)-г), представляющих собой дополнительный объект данного изобретения, поясняются следующими данными. В случае, если в качестве исходных веществ используют, например, сложный метиловый эфир В случае, если в качестве исходных веществ используют, например, 3-метоксимино-(2-гидрокси-фенил)-метил]-5,6-дигидро-1,4,2-диоксазин и бензилхлорид, то реакция по предлагаемому способу (б) протекает по следующей реакционной схеме: В случае, если в качестве исходных веществ используют, например, 3-метоксимино-(2-хлорметил-фенил)-метил]-5,6-дигидро-1,4,2-диоксазин и 2-метилфенол, то реакция по предлагаемому способу (в) протекает по следующей реакционной схеме: В случае, если в качестве исходного соединения используют, например, н-(2-гидрокси-этокси)-метоксимино-(2-фенокси-фенил)-ацетамид, то реакция по предлагаемому способу (г) протекает по следующей реакционной схеме: Исходные вещества формулы (II) известны или их можно получать известными способами (см. заявки 178826, 242081, 382375, 493711). Исходные вещества формулы (III) представляют собой известные химикаты органических синтезов. Исходные вещества формулы (IV) из литературы не известны. Поэтому дальнейшим объектом изобретения являются соединения формулы (II), где А означает диметилен, Ar – орто-фенилен и Е – группу формулы в качестве промежуточных продуктов для соединений формулы (II). Новые гидроксиариловые соединения формулы (IV) получают за счет того, что тетрагидропиранилокси-соединения общей формулы (IX) где А, Ar и Е имеют вышеуказанные значения, подвергают взаимодействию с кислотой, такой, как, например, соляная кислота, метансульфоновая кислота, бензолсульфоновая кислота, п-толуолсульфоновая кислота, или с кислым ионообменником, при необходимости в присутствии разбавителя, такого, как, например, вода, метанол, этанол или сложный этиловый эфир уксусной кислоты, при температуре 0-100°С (см. нижепредставленные примеры). Тетрагидропиранилокси-соединения формулы (IX) из литературы не известны. Поэтому дальнейшим объектом изобретения являются соединения формулы (IX), где А означает диметилен (этан-1,2-диил), Ar – орто-фенилен, Е – группу формулы в качестве промежуточных продуктов для соединений формулы (I). Новые тетрагидропиранилокси-соединения формулы (IX) получают за счет того, что сложные эфиры общей формулы (X) где Ar, Е и R имеют вышеуказанные значения, подвергают взаимодействию с гидроксиламином или его гидрохлоридом, при необходимости в присутствии акцептора кислоты, такого, как, например, гидроокись калия, и, при необходимости, в присутствии разбавителей, таких, как, например, метанол и вода, и образовавшийся при этом промежуточный продукт ин ситу подвергают взаимодействию с дигалогеналканами вышеприведенной общей формулы (III), при необходимости в присутствии акцептора кислоты, такого, как, например, карбонат калия, при температуре 0-100°С (см. описание предлагаемого способа (а) и нижепредставленные примеры). Новые сложные эфиры формулы (X) из литературы не известны. Их можно получать за счет того, что сложные эфиры тетрагидропиранилокси-фенил-уксусной кислоты общей формулы (XI) где Ar и R имеют вышеуказанные значения, подвергают дериватизации обычными методами (см. нижепредставленные примеры). Новые сложные эфиры тетрагидропиранилокси-фенил-уксусной кислоты общей формулы (XI) из литературы не известны. Их можно получать за счет того, что сложные эфиры гидроксифенилуксусной кислоты общей формулы (XII) где Ar и R имеют вышеуказанные значения, подвергают взаимодействию с дигидропираном, при необходимости в присутствии катализатора, такого, как, например, п-толуолсульфоновая кислота, и, при необходимости, в присутствии разбавителя, такого, как, например, тетра-гидрофуран, при температуре 0-100°С (см. нижепредставленные примеры). Исходные вещества формулы (XII) представляют собой известные химикаты органических синтезов. Используемые в предлагаемом способе (б) в качестве дальнейшего реагента соединения формулы (V) представляют собой известные химикаты органических синтезов. Используемые в предлагаемом способе (в) в качестве исходного вещества галогенметиловые соединения формулы (VI) из литературы не известны. Поэтому дальнейшим объектом изобретения являются соединения формулы (VI), где А – диметилен (этан-1,2-диил), Ar – орто-фенилен, Е – группа формулы X1 – галоген, в качестве промежуточных продуктов для соединений формулы (I). Новые галогенметиловые соединения формулы (VI) получают за счет того, что метиловые соединения общей формулы (XIII) где А, Ar и Е имеют вышеуказанные значения, подвергают взаимодействию с агентом галогенирования, таким, как, например, N-бром- или N-хлор-сукцинимид, при необходимости в присутствии катализатора, такого, как, например, азоизобутиронитрил, и, при необходимости, в присутствии разбавителя, такого, как, например, тетрахлорметан, при температуре 0-150°С (см. нижепредставленные примеры). Метиловые соединения формулы (XIII) из литературы не известны. Поэтому дополнительным объектом изобретения являются соединения формулы (XIII), где А – диметилен (этан-1,2-диил), Ar – орто-фенилен, Е – группа формулы в качестве промежуточных продуктов для соединений формулы (I). Новые метиленовые соединения формулы (XIII) получают за счет того, что сложные эфиры общей формулы (XIV) где где Ar, Е и R имеют вышеуказанные значения, подвергают последовательному взаимодействию с гидроксиламином или его гидрохлоридом, при необходимости, в присутствии акцептора кислоты, такого, как, например, гидрооксись калия, и, при необходимости, в присутствии разбавителя, такого, как, например, метанол, и с дизамещенным алканом вышеприведенной общей формулы (III), при необходимости, в присутствии акцептора кислоты, такого, как, например, карбоната калия, при температуре 0-150°С (см. нижепредставленные примеры). Соединения формулы (XIV) известны или их можно получать известными способами (см. заявки ЕР 386561, 498188, нижепредставленные примеры). Используемые в предлагаемом способе (в) в качестве исходного вещества соединения формулы (VII) представляют собой известные химикаты органических синтезов. Используемые в предлагаемом способе (г) в качестве исходного вещества гидроксиалкоксиамиды формулы (VIII) из литературы не известны. Поэтому еще одним объектом изобретения являются соединения формулы (VIII), где А означает диметилен (этан-1,2-диил), Ar – орто-фенилен, Е – группу формулы G – группу -CH2-O-, Z – фенил, замещенный метилом, в качестве промежуточных продуктов для соединений формулы (I). Новые гидроксиалкоксиамиды формулы (VIII) получают за счет того, что производные общей формулы (XV) где Ar, Е, G и Z имеют вышеуказанные значения, и Y означает галоген, гидрокси или алкокси, подвергают взаимодействию с гидроксиламинами общей формулы (XVI) где А имеет вышеуказанное значение, при необходимости, в присутствии акцептора кислоты, такого, как, например, три-этиламин, пиридин или 4-диметиламино-пиридин, и, при необходимости, в присутствии разбавителя, такого, как, например, метиленхлорид, толуол или тетрагидрофуран, при температуре 0-150°С (см. заявки ЕР 178826, 242081, 493711). Производные формулы (XV) известны или их можно получать известными способами (см. J. Chem. Soc. Perkin Trans. I 1987, 2829-2823). Предлагаемые способы (а), (б) и (в) проводят предпочтительно в присутствии акцептора кислоты. В качестве акцепторов кислоты пригодны все органические или неорганические основания. К ним принадлежат, например, гидриды щелочноземельных металлов или щелочных металлов, гидроокиси щелочноземельных металлов или щелочных металлов, амиды щелочноземельных металлов или щелочных металлов, алкоголяты щелочноземельных металлов или щелочных металлов, ацетаты щелочноземельных металлов или щелочных металлов, карбонаты щелочноземельных металлов или щелочных металлов или гидрокарбонаты щелочноземельных металлов или щелочных металлов, такие, как, например, гидрид натрия, амид натрия, метилат натрия, этилат натрия, трет. бутилат калия, гидроокись натрия, гидроокись калия, гидроокись аммония, ацетат натрия, ацетат калия, ацетат кальция, ацетат аммония, карбонат натрия, карбонат калия, гидрокарбонат калия, гидрокарбонат натрия или карбонат аммония, а также трет. амины, такие, как, например, триметиламин, триэтиламин, трибутиламин, N,N-диметиланилин, N,N-диметил-бензиламин, пиридин, N-метилпиперидин, N,N-диметиламинопиридин, диазабициклооктан, диазабициклононен или диазабициклоундецен. В качестве разбавителя для проведения предлагаемых способов (а), (б) и (в) используют воду и органические растворители. К ним принадлежат, в частности, алифатические, алициклические или ароматические, при необходимости галогенированные углеводороды, такие, как, например, бензин, бензол, толуол, ксилол, хлорбензол, дихлорбензол, простой петролейный эфир, гексан, циклогексан, дихлорметан, хлороформ или четыреххлористый углерод, простые эфиры, такие, как, например, диэтиловый эфир, диизопропиловый эфир, диоксан, тетрагидрофуран или этиленгликоль-диметиловый или этиленгликольдиэтиловый эфиры; кетоны, такие, как, например, ацетон, бутанон или метил-изобутил-кетон; нитрилы, такие, как, например, ацетонитрил, пропионитрил или бензонитрил; амиды, такие, как, например, N,N-диметилформамид, N,N-диметилацетамид, N-метилформанилид, N-метилпирролидон или триамид гексаметилфосфорной кислоты; сложные эфиры, такие, как, например, сложный метиловый эфир уксусной кислоты или сложный этиловый эфир уксусной кислоты; сульфоксиды, как, например, диметилсульфоксид, спирты, такие, как, например, метанол, этанол, н.- или изопропанол, простой этиленгликольмонометиловый эфир, простой этиленгликольмоноэтиловый эфир, простой диэтиленгликоль-монометиловый эфир, простой диэтиленгликоль-моноэтиловый эфир, их смеси с водой или чистая вода. Предлагаемый способ (г) проводят предпочтительно в присутствии средства дегидратации. При этом в качестве средства дегидратации в частности пригодны обычные водоудаляющие химикаты, в частности ангидриды кислоты, такие, как, например, фосфорный ангидрид. В качестве разбавителя для проведения предлагаемого способа (г) используют общепринятые инертные органические растворители. К ним принадлежат, в частности, алифатические, алициклические или ароматические, при необходимости галогенированные углеводороды, такие, как, например, бензин, бензол, толуол, ксилол, хлорбензол, дихлорбензол, простой петролейный эфир, гексан, циклогексан, дихлорметан, хлороформ или четыреххлористый углерод, простые эфиры, такие, как, например, диэтиловый эфир, диизопропиловый эфир, диоксан, тетрагидрофуран или этиленгликоль-диметиловый или этиленгликольдиэтиловый эфиры; кетоны, такие, как, например, ацетон, бутанон или метилизобутилкетон; нитрилы, такие, как, например, ацетонитрил, пропионитрил или бензонитрил; амиды, такие, как, например, N,N-диметилформамид, N,N-диметилацетамид, N-метилформанилид, N-метилпирролидон или триамид гексаметилфосфорной кислоты; сложные эфиры, такие, как, например, сложный метиловый эфир уксусной кислоты или сложный этиловый эфир уксусной кислоты; сульфоксиды, как, например, диметилсульфоксид. Температура реакции при проведении предлагаемых способов (а) – (г) может колебаться в широких пределах. Обычно работают при температуре -20-+200°С, предпочтительно при температуре 0-150°С. Для проведения предлагаемого способа (а) на 1 моль производного карбоновой кислоты формулы (II) обычно используют 1-5 моль, предпочтительно 1,0-2,5 моль, гидроксиламина или его галоидводородной соли и обычно 1-1 моль, предпочтительно 1,0-5,0 моль, дизамещенного алкана формулы (III). Для проведения предлагаемого способа (б) на 1 моль гидроксиларилового соединения формулы (IV) обычно используют 0,5-2,0 моль, предпочтительно 0,9-1,2 моль, соединения формулы (V). Для проведения предлагаемого способа (в) на 1 моль галогенированного соединения формулы (VI) обычно используют 1-5 моль, предпочтительно 1,5-3 моль, соединения формулы (VII). Для проведения предлагаемого способа (г) на 1 моль гидроксиалкоксиамида формулы (VIII) обычно используют 1-5 моль, предпочтительно 1,5-4 моль, средства дегидратации. Реакции, переработку реакционных смесей и выделение целевых продуктов осуществляют известными приемами (см. нижепредставленные примеры). Предлагаемые соединения вышеприведенной формулы (I) могут иметься в качестве смесей различных изомерных форм, в частности, Е- и Z-изомеров. Используют как Е-, так и Z-изомеры, а также смеси этих изомеров в любой форме. Предлагаемые соединения проявляют фунгицидную активность. Фунгицидные средства, которые являются дальнейшим объектом изобретения, используют для борьбы с плазмо-диофоромицетами, оомицетами, хитридиомицетами, цигомицетами, аскомицетами, базидомицетами и дейтеромицетами. В нижеследующем в качестве примера приводятся несколько возбудителей грибковых заболеваний, принадлежащих к вышеназванным семействам. Виды Pythium, такие, как, например, Pythium ultimum, Виды Phytophthora, такие, как, например, Phytophthora infestans. Виды Pseudoperonospora, такие, как, например, Pseudoperonospora humuli или Pseudoperonospora cubense. Виды Plasmopara, такие, как, например, Plasmopara viticola. Виды Peronospora, такие, как, например, Peronospora pisi или Peronospora brassicae. Виды Erysiphe, такие, как, например, Erysiphe graminis. Виды Sphaerotheca, такие, как, например, Sphaerotheca fuliginea. Виды Podosphaera, такие, как, например, Podosphaera leucotricha. Виды Venturia, такие, как, например, Venturia inaequalis. Виды Pyrenophora, такие, как, например, Pyrenophora teres или Pyrenophora graminea (конидиальная форма: Drechslera, синоним: Helminthosporium). Виды Cochliobolus, такие, как, например, Cochliobolus sativus (конидиальная форма: Drechslera, синоним: Helminthosporium). Виды Uromyces, такие, как, например, Uromyces appendiculatus. Виды Puccinia, такие, как, например, Puccinia recondita. Виды Tilletia, такие, как, например, Tilletia caries. Виды Ustilago, такие, как, например, Ustilago nuda или Ustilago avenae. Виды Pellicularia, такие, как, например, Pellicularia sasakii. Виды Pyricularia, такие, как, например, Pyricularia oryzae. Виды Fusarium, такие, как, например, Fusarium culmorum. Виды Botrytis, такие, как, например, Botrytis cinerea. Виды Septoria, такие, как, например, Septoria nodorum. Виды Leptosphaeria, такие, как, например, Leptosphaeria nodorum. Виды Cercospora, такие, как, например, Cercospora canescens. Виды Alternaria, такие, как, например, Alternaria brassicae. Виды Pseudocercosporella, такие, как, например, Pseudocercosporella herpotrichoides. Хорошая переносимость растениями активных веществ в необходимых для борьбы с болезнями растений концентрациях позволяет производить обработку надземных частей растений, посадочного и посевного материалов и почвы. При этом предлагаемые активные вещества можно использовать особенно успешно для борьбы с болезнями в области плодоводства и овощеводства, как, например, с возбудителями Phytophtora, или для борьбы с болезнями хлебных злаков, например, для борьбы с возбудителями Pyrenophora. Кроме того, предлагаемые активные вещества обладают хорошим действием, например, в борьбе с возбудителями Erisyphe graminis, Cochliobolus sativus, Leptosphaeria nodorum, Pseudocercosporella herpotrichoides и с видами Fusarium на хлебных злаках, с возбудителями Pyricularia oryzae и Pellicularia sasakii на рисе. Они обладают также широким действием ин-витро. Активные вещества можно переводить в стандартные препараты в зависимости от их физических и/или химических свойств, например, растворы, эмульсии, суспензии, порошки, пены, пасты, гранулы, аэрозоли, полимерные микрокапсулы и оболочки для посевного материала. Кроме того, они могут представлять собой препараты для чрезвычайно тонкого распределения в виде холодного и теплого тумана. Эти препараты получают известными приемами, например, смешиванием активного вещества с наполнителями, например, с жидкими растворителями, находящимися под давлением сжиженными газами и/или твердыми носителями, при необходимости с применением поверхностно-активных веществ, например, эмульгаторов и/или диспергаторов и/или пенообразователей. В случае использования воды в качестве наполнителя можно также применять органический растворитель в качестве вспомогательного средства. В качестве органического растворителя применяют в основном: ароматические углеводороды, такие, как, например, ксилол, толуол, или алкилнафталины, хлорированные ароматические и алифатические углеводороды, например, хлорбензолы, хлорэтилены или метиленхлорид, алифатические углеводороды, как циклогексан или парафины, например, нефтяные фракции, спирты, как бутанол или гликоль, а также их простые и сложные эфиры, кетоны, такие, как ацетон, метилэтилкетон, метилизобутилкетон или циклогексанон, сильно полярные растворители, как диметилформамид или диметилсульфоксид, а также вода. Под сжиженными газообразными наполнителями или носителями следует понимать такие жидкости, которые при температуре окружающей среды и атмосферном давлении являются газообразными, например, рабочие газы для аэрозолей, такие, как, например, галогенированные углеводороды, а также бутан, пропан, азот и двуокись углерода. В качестве твердых носителей применяют, например, натуральную породную муку, такую, как каолин, глинозем, тальк, мел, кварц, аттапульгит, монтпориллонит или диатомная земля, и синтетическую породную муку, такую, как высокодисперсная кремневая кислота, окись алюминия и силикаты. В качестве твердых носителей для гранулятов применяют, например, измельченные и фракционированные природные каменные породы, такие, как кальцит, мрамор, пемза, сепиолит, доломит, синтетические неорганические и органические муки, а также органические материалы, такие, как опилки, кожура кокосового ореха, початки кукурузы и стебли табака. В качестве эмульгатора и/или пенообразователя применяют, например, неионогенные и анионные эмульгаторы, как сложные полиоксиэтиленовые эфиры жирных кислот, простые полиоксиэтиленовые эфиры жирных спиртов, например, аклил-арил-полигликолевый эфир, алкилсульфонаты, алкилсульфаты, арилсульфонаты, а также белковые гидролизаты. В качестве диспергатора применяют, например, отработанный лигнинсульфитный щелок и метилцеллюлозу. Препараты могут также содержать связующее, такое, как, например, карбокси-метилцеллюлоза, природные и синтетические порошкообразные, зернистые или латексные полимеры, как, например, гуммиарабик, поливиниловый спирт, поливинилацетат, а также натуральные фосфолипиды, как кефалин и лецитин и синтетические фосфолипиды. Другими добавками могут быть минеральные и растительные масла. Кроме того, препараты могут содержать еще красители, как, например, неорганические пигменты, например, окись железа, окись титана, ферроцианистый синий, и органические красители, как ализарин, азо- и метилфталоцианиновые красители и питательные микроэлементы, такие, как соли железа, марганца, бора, меди, кобальта и олова. Препараты содержат обычно 0,1-95 вес.% активного вещества, предпочтительно 0,5-90 вес.%. Предлагаемые активные вещества можно применять как таковые или в виде их препаратов, а также в виде смеси с известными фунгицидами, бактерицидами, акарицидами, нематоцидами или инсектицидами, например, в целях расширения спектра действия активных веществ или предотвращения устойчивости. Во многих случаях получается синергетический эффект, т.е. активность смеси превышает активность отдельных компонентов. Особенно выгодными для сочетания с предлагаемыми активными веществами являются следующие соединения: Фунгициды: 2-аминобутан; 2-анилино-4-метил-6-циклопропил-пиримидин; 2′,6′-дибромо-2-метил-4′-трифторметокси-4′-трифтор-метил-1,3-тиазолы-5-карбоксанилид; 2,6-ди-хлор-М-(4-трифторметилбензил)бензамид; (Е)-2-метоксиимино-М-метил-2-(2-феноксифенил)ацетамид; 8-гидроксихинолинсульфат; метил-(Е)-2-{2-[6-(2-цианофен-окси)пиримидин-4-илокси]фенил}-3-метоксиакрилат; метил-(Е)-метоксимино[альфа-(о-толилокси)-о-толил]ацетат; 2-фенилфенол (ОРР), альдиморф, ампропил-фос, анилазин, азацоназол, беналаксил, беноданил, беномил, бинапакрил, бифенил, битертанол, бластицидин-S, бромуцоназолы, бупириматы, бутиобаты, полисульфид кальция, каптафол, каптан, карбендазим, карбоксин, хинометионат, хлоронеб, хлоропикрин, хлороталинил, хлозолинат, цуфранеб, цимоксанил, ципроцоназолы, ципрофурам, дихлорофен, диклобутразол, диклофлуанид, дикломезин, диклоран, диэтофенкарб, дифеноцоназол, диметиримол, диметоморф, диницоназол, динокап, дифениламин, дипиритион, диталимфос, дитианон, додин, дразоксолон, эдифенфос, эпоксицоназолы, этиримол, этридиазол, фенаримол, фенбуцоназолы, фенфурам, фенитропан, фенпиклонил, фенпропидин, фенпропиморф, фентинацетаты, фентингидроксид, фербам, феримзоны, флюазинам, флюдиоксонил, фторомиды, флюхинцоназолы, флюсилазолы, флюсульф-амиды, флютоланил, флютриафол, фолпет, фосетил-алюминий, фталиды, фубери-дазол, фуралаксил, фурмециклокс, гуазатины, гексахлорбензол, гексацоназол, гимексазол, имизалил, имибенцоназол, иминоктадин, ипробенфос (IBR), ипродион, изопротиолан, казугамицин, приготовления меди, такие, как гидроокись меди, нафтенат меди, хлорокись меди, сернокислая медь, окись меди, медный оксин и бордосская смесь, мэн-коппер, манцозеб, манеб, мепанипирим, мепронил, металаксил, метцоназол, метасульфокарб, метфуроксам, метирам, метсульфовакс, миклобутанил, диметилдитиокарбамат никеля, нитротал-изопропил, нуаримол, офурацы, оксадиксил, оксамокарб, оксикарбоксин, пефуразоат, пенцоназол, пенцицурон, фосдифен, пимарицин, пипералин, полиоксин, пробеназол, прохлорац, процимидон, пропамокарб, пропицоназолы, пропинеб, пиразофос, пирифенокс, пириметанил, пирохилон, хинтозен (PCNB), сера и приготовления серы, тебуцоназол, теклофталам, тецназен, тетрацоназол, тиабендазол, тициофен, тиофанат-метил, тирам, толхлофос-метил, толилфлюанид, триадимефон, триадименол, триазоксид, трихламид, трициклазол, тридеморф, трифлюмизол, трифорин, тритицоназол, валидамицин А, винхлозолин, зинеб, зирам. Бактерициды: бронопол, дифхлорофен, нитрапирин, диметилдитиокарабамат никеля, касугамицин, октилинон, фуранкарбоновая кислота, окситетрациклин, пробеназол, стрептомицин, теклофталам, сернокислая медь и другие приготовления меди. Инсектициды, акарициды, нематициды: абамектин, ацефат, акринатрин, аланикарб, альдикарб, алфаметрин, амитраз, авермектин, AZ 60541, азадирахтин, азинфос А, азинфос М, азоциклотин, Bacillus thuringiensis, 4-бромо-2-(4-хлорфенил)-1-(этоксиметил)-5-(трифторметил)-1Н-пирролы-3-карбонитрилы, бендиокарб, бенфуракарб, бенсультап, бетацил-утрин, бифентрин, ВРМС, брофенпрокс, бромофос А, буфенкарб, бупрофезин, бутокарбоксин, бутилпиридабен, кадусафос, карбарил, карбофуран, карбофенотион, карбосульфан, картап, хлорэтокарб, хлорэтоксуфос, хлорэтоксифос, хлорфенвинфос, хлорфлюазурон, хлормефос, N-[(6-хлоро-3-пиридинил)-метил]-N хлорпирифос, хлорпирифос М, цис-ресметрин, клоцитрин, клофентезин, цианофос, циклопротрин, цифлутрин, цигалотрин, цигексатин, циперметрин, циромазин, дельтаметрин, деметон М, деметон S, деметон-S-метил, диафентиурон, диазинон, дихлофентион, дихлорфос, диклифос, дикротофос, диэтион, дифлубензурон, диметоат, диметилвинфос, диоксатион, дисульфотон, эдифенфос, эмамектин, эсфенвалерат, этиофенкарб, этион, этофенпрокс, этопрофос, этофенпрокс, этримфос, фенаминфос, феназахин, фенбутатиноксид, фенитротион, фенобукарб, фенотиокарб, феноксикарб, фенпропатрин, фенпирад, фенпироксимад, фентион, фенвалераты, фипронил, флуазинам, флуазурон, флуциклоксурон, флуцитринат, флуфеноксурон, флуфенпрокс, флувалинаты, фонофос, формотион, фостиазат, фубфенпрокс, фуратиокарб, НСН, гептенофос, гексафлумурон, гекситиазокс, имидаклоприд, ипробенфос, изазофос, изофенфос, изопрокарб, изоксатион, ивемектин, ламда-цигалотрин, луфенурон, малатион, мекарбам, мервинфос, месульфенфос, метальдегид, метакрифос, метамидофос, метидатион, метиокарб, метомил, метолкарб, милбемектин, монокротофос, моксидектин, налед, NC 184,нитенпирам, ометоат, оксамил, оксидеметон М, оксидепрофос, паратион А, паратион М, перметрин, пентоат, форат, фосалон, фосмет, фосфамдон, фоксим, пиримикарб, пиримифос М, пиримифос А, профенофос, профенофос, промекарб, пропафос, пропоксур, протиофос, протоат, пиметрозин, пирахлофос, пираклофос, пираклофос, пирадафентион, пиресметрин, пиретрум, пиридабен, пиримидифен, пирипроксифен, хиналфос, салитион, себуфос, силафтофен, сульфотеп, сульпрофос, тебуфенозиды, тебуфенпирад, тебупиримфос, тефлубензурон, тефлутрин, темефос, тербам, тербуфос, тетрахлорвинфос, тиафенокс, тиодикарб, тиофанокс, тиометон, тионазин, турингиенсин, тралометрин, триаратен, триазофос, триазурон, трихлорфон, трифлумурон, триметакарб, вамидотион, ХМС, ксилилкарб, YI 5301 /5302, зетаметрин. Предлагаемые активные вещества могут иметься в препаратах также в смеси с другими известными активными веществами, такими, как гербициды, а также с удобрениями и регуляторами роста растений. Активные вещества можно применять как таковые, в виде их препаратов или получаемых из них рабочих форм, таких, как, например, готовые к использованию растворы, суспензии, смачивающиеся порошки, пасты, растворимые порошки, средства для опыливания и грануляты. Их используют известными приемами, например, путем поливания, разбрызгивания, распыления, рассыпания, вспенивания, нанесения кистью и т.д. Кроме того, возможно применять активные вещества по методу обеспечения чрезвычайно тонкого распределения или же впрыскивания средства или же самого активного вещества в почву. Возможна и обработка посевного материала полезных растений. При обработке частей полезных растений концентрация активного вещества в используемых препаратах может колебаться в широких пределах. Она обычно составляет 1-0,0001 вес.%, предпочтительно 0,5-0,001 вес.%. При обработке посевного материала обычно применяют 0,001-50 г активного вещества на кг посевного материала, предпочтительно 0,01-10 г. При обработке почвы в месте применения активного вещества требуются концентрации от 0,00001 до 0,1 вес.%, предпочтительно 0,0001 до 0,02 вес.%. Изобретение иллюстрируется следующими примерами. Пример 1 К 1,8 г (25 ммоль) гидрохлорида гидроксиламина в 20 мл метанола при 20°С медленно добавляют раствор 3,3 г 86%-ной гидроокиси калия в 20 мл метанола. Затем порциями добавляют 4,0 г (12,8 ммоль) сложного метилового эфира Получают 1,4 г (33% теории) 3-{ Целевой продукт данного примера также получают при замене 1,2-дибром-этана на 1,2-диметилсульфонилоксиэтан и 1,2-дифенилсульфонилокси-этан. Аналогично примеру 1, а также в соответствии с общим описанием предлагаемого способа можно также получать приведенные в следующей таблице 1 соединения формулы (I). 1H-ЯМР-спектры поглощены в CDCl3 с тетраметилсиланом в качестве внутреннего стандарта. Химические смещения, как правило, приводятся значениями *3начние log Р определено согласно EEC-Directive 79/831 Annex V.A8 путем высокопроизводительной жидкостной хроматографии на обратнофазной колонке (С 18) при температуре 43°С с применением в качестве элюента 0,1%-ной водной фосфорной кислоты и линейного градиента ацетонитрила (от 10% до 90%). Калибровка осуществлялась линейными алкан-2-онами, значение log P которых известны (определение значений log P на основе времени удерживания путем линейной интерполяции между двумя последующими алканонами). Приведенное в таблице 1 в качестве примера 22 соединение можно получать, например, следующим образом: К смеси 1,5 г (6 ммоль) 3-[ Получают 1,9 г (86% теории) 3-{ Целевой продукт данного примера можно также получать при замене 4,6-дихлор-пиримидина на 4-хлор-6-метилсульфонилокси-пиримидин или 4-хлор-6-фенилсульфонилокси-пиримидин. Приведенное в таблице 1 в качестве примера 23 соединение можно получать, например, следующим образом: Смесь 0,3 г (0,9 ммоль) 3-[ Получают 0,3 г (81% теории) 3-{ Приведенное в таблице 1 в качестве примера 20 соединение можно получать, например, следующим образом: Смесь 0,5 г (2 ммоль) 3-[( Получают 0,4 г (59% теории) 3-{ Получаемое согласно примеру 1 соединение можно также получать, например, следующим образом: 0,75 г (2,4 ммоль) 3-[ Получают 0,40 г (49% теории) 3-{ Приведенное в таблице 1 в качестве примера 11 соединение можно получать, например, следующим образом: 0,20 г (0,56 ммоль) N-(2-гидрокси-этокси)- Получают 84 мг (42% теории) 3-{ 1H-ЯМР (D6-ДМСО, Получение исходных веществ формулы (IV): Пример (IV-1) 9,0 г (28 ммоль) 3-[( В качестве 1-й фракции получают 0,6 г (9% теории) 7-{3-[ Получение исходных веществ формулы (IX): Пример (IX-1) К 6,8 г (98 ммоль) гидрохлорида гидроксиламина в 290 мл метанола добавляют 13,9 г (211 ммоль) 85%-ного водного раствора гидроокиси калия и 17 г (58 ммоль) сложного метилового эфира Получают 9,0 г (49% теории) 3-[ Получение исходных веществ Формулы (X): Пример (Х-1) К раствору 203 г (1,81 моль) трет. бутилата калия в 2 л трет. бутанола добавляют каплями 564 г (4,93 моль) трет. бутилнитрита и 411 г (1,64 моль) сложного метилового эфира 2-тетрагидропиранилокси-фенилуксусной кислоты, растворенных в 500 мл трет. бутанола. По истечении 90 минут добавляют каплями 350 г (2,47 моль) метилйодида, после чего смесь перемешивают в течение 15 часов при 20°С. Затем в вакууме, получаемом с помощью водоструйного насоса, остаток подают в простой метил-трет.-бутиловый эфир, сушат над сульфатом натрия и фильтруют. Остаток кристаллизуют путем дигерирования с помощью диэтилового эфира, и продукт выделяют путем отсасывания. Получают 69,3 г (15% теории) сложного метилового эфира Получение исходных веществ формулы (XI): Пример (XI-1) Смесь 500 г (3,0 моль) сложного метилового эфира 2-гидрокси-фенил-уксусной кислоты, 506 г (6,0 моль) 3,4-дигидро-пирана, п-толуолсульфокислоту с конца шпателя и 2,5 л тетрагидрофурана перемешивают в течение 15 часов при 20°С, затем ее при перемешивании смешивают с 10%-ным ледяным водным раствором гидроокиси калия, после чего добавляют сульфат натрия и фильтруют. Из фильтрата растворитель тщательно отгоняют в вакууме, получаемом с помощью водоструйного насоса. Получают 698 г (99% теории) сложного метилового эфира 2-тетрагидропиранил-окси-фенилуксусной кислоты в качестве маслянистого остатка. Получение исходных веществ формулы (VI): Пример (VI-1) 0,50 г (2,13 ммоль) 3-[ Получают 20 мг (30% теории) 3-[ Получение исходных веществ формулы (XIII): Пример (XIII-1) К 19,6 г (0,283 моль) гидрохлорида гидроксиламина в 150 мл метанола добавляют медленно раствор 36,9 г (0,565 моль) 86%-ного гидроокиси калия в 150 мл метанола. Затем добавляют порциями 30 г (0,145 моль) сложного метилового эфира Получают 15,2 г (45% теории) 3-[ Получение исходных веществ формулы (XIV): Пример (XIV-1) 187,5 г (1,673 моль) трет. бутилата калия растворяют в 1875 мл трет. бутанола. К этому раствору добавляют раствор 471,5 г (4,57 моль) трет. бутилнитрита и 250 г (1,525 моль) сложного метилового эфира 2-метил-фенилуксусной кислоты в 500 мл трет. бутанола таким образом, что внутренняя температура не превышает 50°С. Смесь перемешивают в течение 90 минут при 20 – 30°С. После этого добавляют каплями 326,5 г (2,3 моль) метилйодида. Реакционную смесь перемешивают в течение 14 часов при 20°С. Затем растворитель отгоняют в вакууме, получаемом с помощью водоструйного насоса, остаток подают в 2 л воды и три раза экстрагируют сложным этиловым эфиром уксусной кислоты. Объединенные органические фазы сушат над сульфатом натрия и фильтруют. Фильтрат сгущают, осадок подают в 250 мл изопропанола и при кипячении смешивают с водой до помутнения. После охлаждения до 0°С и перемешивания в течение 60 минут, выкристаллизовавшийся продукт выделяют путем отсасывания. Получают 84,5 г (27% теории) сложного метилового эфира 1H-ЯМР (CDCl3, Получение исходных веществ формулы (VIII): Пример (VIII-1) 0,8 г (2,36 ммоль) хлорангидрида Получают 0,4 г (50% теории) N-(2-гидрокси-этокси)- 1H-ЯМР (CDCl3, Получение исходных веществ формулы (XV): Пример (XV-1) 0,93 г (2,95 ммоль) Получают 0,95 г хлорангидрида Пример (XV-2) 2,0 г (6,1 ммоль) сложного метилового эфира Получают 1,5 г (78% теории) 1H-ЯМР (CDCl3, Фунгицидная активность замещенных азадиоксоциклоалкенов формулы (I) подтверждается следующими примерами. Пример А Опыт с Pyrenophora teres (ячмень)/защитное действие 1 вес. часть активного вещества смешивают с 10 вес. частями N-метилпирролидона в качестве растворителя и 0,6 вес. части простого алкиларилполигликолевого эфира в качестве эмульгатора и полученный концентрат разбавляют водой до желаемой концентрации. Для исследования защитного действия молодые растения опрыскивают препаратом активного вещества до образования капель. После присыхания препарата растения опрыскивают конидиальной суспензией Pyrenophora teres. Затем растения в течение 48 часов хранят в инкубационной камере при температуре 20°С и относительной влажности воздуха 100%. После этого растения хранят в теплице при температуре около 20°С и относительной влажности воздуха около 80%. Через 7 дней после инокуляции проводят оценку. При этом устанавливают, что степень активности соединения примера 1 составляет 100% при норме расхода 400 г/га. Такую же активность проявляют соединения примеров 6, 8, 19, 23, 24, 39, 44, 46, 47, 52, 53, 65, 69, 72, 78, 79. Если применять соединения примеров 2, 15, 16, 26 и 29 при норме расхода 250 г/га, то степень активности составляет соответственно 83, 67, 67, 72 и 68% от необработанных контрольных растений. Пример Б Опыт с Phytophthora (помидоры)/системное действие 1 вес. часть соединения примера 1 в качестве активного вещества смешивают с 4,7 вес. части ацетона в качестве растворителя и 0,6 вес. части простого алкиларилполигликолевого эфира в качестве эмульгатора и полученный концентрат разбавляют водой до желаемой концентрации. Для исследования системных свойств препарат активного вещества наливают на почву, в которой находятся готовые к проведению опыта молодые растения. Через 3 дня после обработки растения инокулируют водной суспензией спор Phytophthora infestans. Затем растения хранят в инкубационной камере при температуре около 20°С и относительной влажности воздуха 100%. Через 3 дня после инокуляции проводят оценку. При этом устанавливают, что степень активности соединения примера 1 составляет 58% при концентрации 100 ч/млн. Пример В Опыт с Pyricularia (рис) / системное действие. 1 вес. часть соединения примера 1 в качестве активного вещества смешивают с 12,5 вес. части ацетона в качестве растворителя и 0,3 вес. части простого алкиларилполигликолевого эфира в качестве эмульгатора и полученный концентрат разбавляют водой до желаемой концентрации. Для исследования системных свойств 40 мл препарата активного вещества наливают на почву, в которой выросли молодые рисовые растения. Через 7 дней после обработки растения инокулируют водной суспензией спор Pyricularia oryzae. После этого растения до проведения оценки хранят в теплице при температуре 25°С и относительной влажности воздуха 100%. Через 4 дня после инокуляции проводят оценку поражения. При этом устанавливают, что степень активности соединения примера 1 составляет 80% при расходе 100 мг/100 мл. Пример Г Опыт с Venturia (яблоня)/защитный 1 вес. часть активного вещества смешивают с 4,7 вес. части ацетона в качестве растворителя и 0,3 вес. части алкиларилполигликолевого простого эфира в качестве эмульгатора и полученный концентрат разбавляют водой до концентрации, равной 2,5 ч/млн. Для проверки на защитную активность молодые растения обрызгивают композицией биологически активного вещества. После высыхания нанесенного состава растения инокулируют водной суспензией конидий возбудителя яблочной парши Venturia inaequalis и затем оставляют на один день в инкубационной камере при температуре 20°С и 100%-ной относительной влажности воздуха. Затем растения помещают в теплицу при температуре 20°С и относительной влажности воздуха около 70%. Через двенадцать дней после инокуляции определяют процентную степень активности по сравнению с необработанными контрольными растениями. Результаты опыта сведены в таблице 2.
Пример Д Опыт с Sphaerotheca (огурцы) / защитный 1 вес. часть активного вещества смешивают с 4,7 вес. частей ацетона в качестве растворителя и 0,3 вес. части алкиларилполигликолевого простого эфира в качестве эмульгатора и полученный концентрат разбавляют водой до концентрации, равной 10 ч/млн. Для проверки на защитную активность молодые растения обрызгивают композицией биологически активного вещества. После высыхания нанесенного состава растения опыляют конидиями гриба Sphaerotheca fuliginea. Затем растения помещают в теплицу при температуре 23-24°С и относительной влажности воздуха около 75%. Через десять дней после инокуляции определяют процентную степень активности по сравнению с необработанными контрольными растениями. Результаты опыта сведены в таблице 3.
Пример Е Опыт с Pseudocercosporella herpotrichoides (пшеница) / защитный 1 вес. часть активного вещества смешивают с 10 вес. частями М-метилпирролидона в качестве растворителя и 0,6 вес. части алкиларилполигликолевого простого эфира в качестве эмульгатора и полученный концентрат разбавляют водой. Для проверки на защитную активность молодые растения обрызгивают композицией биологически активного вещества, при этом биологически активное вещество применяют в количестве, равном 250 г/га. После высыхания нанесенного состава растения инокулируют у основания стебля спорами Pseudoercosporella herpotrichoides. Затем растения помещают в теплицу при температуре приблизительно 10°С и относительной влажности воздуха около 80%. Через двадцать один день после инокуляции определяют процентную степень активности по сравнению с необработанными контрольными растениями. Результаты опыта сведены в таблице 4.
Пример Ж Опыт с Cochliobolus sativus (ячмень) / защитный 1 вес. часть активного вещества смешивают с 10 вес. частями N-метилпирролидона в качестве растворителя и 0,6 вес. части алкиларилполигликолевого простого эфира в качестве эмульгатора и полученный концентрат разбавляют водой. Для проверки на защитную активность молодые растения обрызгивают композицией биологически активного вещества, при этом биологически активное вещество применяют в количестве, равном 250 г/га. После высыхания нанесенного состава растения обрызгивают водной суспензией конидий Cochliobolus sativus. Растения помещают в теплицу при температуре приблизительно 20°С и относительной влажности воздуха около 80%. Через двадцать один день после инокуляции определяют процентную степень активности по сравнению с необработанными контрольными растениями при норме расхода, равной 250 г/га. Результаты опыта сведены в таблице 5.
Формула изобретения
1. Замещенные азадиоксоциклоалкены общей формулы (I) где А – диметилен (этан-1,2-диил), незамещенный или замещенный метилом; Ar – орто-фенилен, незамещенный или замещенный фтором, тиофендиил или пиридиндиил; Е – группа формулы G – кислород, группы -O-СН2-, -СН2-O- или -С(СН3)=N-O-СН2-; Z – фенил, пиримидинил или тиадиазолил, незамещенные или одно- или двукратно замещенные заместителями из группы, включающей метил, этил, н- или изопропил, н-, изо-, втор- или трет-бутил, метокси, этокси, трифторметил, трифторметокси, дифторметокси, фтор, хлор, бром, метилтио, этилтио, H3C-O-N=CH-, бензилокси, нафтилокси, пиридинил, пиридинилтио, пиридинилокси, бензилтио, незамещенный или замещенный хлором или метилом, тиенил, незамещенный или замещенный метилом, фенил, незамещенный или замещенный 1 или 2 одинаковыми или различными заместителями из группы, включающей метил, этил, метокси, этокси, дифторметилокси, трифторметил, фтор, хлор и бром, феноксигруппу, незамещенную или замещенную 1 или 2 одинаковыми или различными заместителями из группы, включающей фтор, хлор, бром, циано, метил, метокси, этил, дифторметилокси, трифторметил, метоксикарбонил и диметиламиносульфонил, и фенилтиогруппу, незамещенную или замещенную однократно фтором, хлором или бромом, или Z означает нафтил. 2. Способ получения замещенных азадиоксоциклоалкенов общей формулы (I) где А – диметилен (этан-1,2-диил), незамещенный или замещенный метилом; Ar – ортофенилен, незамещенный или замещенный фтором, тиофендиил или пиридиндиил; Е – группа формулы G – кислород, группы -О-СН2-, -СН2-O- или -С(СН3)=N-O-СН2-, Z – фенил, пиримидинил или тиадиазолил, незамещенные или одно- или двукратно замещенные заместителями из группы, включающей метил, этил, н- или изопропил, н-, изо-, втор- или трет-бутил, метокси, этокси, трифторметил, трифторметокси, дифторметокси, фтор, хлор, бром, метилтио, этилтио, H3C-O-N=CH-, бензилокси, нафтилокси, пиридинил, пиридинилтио, пиридинилокси, бензилтио, незамещенный или замещенный хлором или метилом, тиенил, незамещенный или замещенный метилом, фенил, незамещенный или замещенный 1 или 2 одинаковыми или различными заместителями из группы, включающей метил, этил, метокси, этокси, дифторметилокси, трифторметил, фтор, хлор и бром, феноксигруппу, незамещенную или замещенную 1 или 2 одинаковыми или различными заместителями из группы, включающей фтор, хлор, бром, циано, метил, метокси, этил, дифторметилокси, трифторметил, метоксикарбонил и диметиламиносульфонил, и фенилтиогруппу, незамещенную или замещенную однократно фтором, хлором или бромом, или Z означает нафтил, отличающийся тем, что производные карбоновой кислоты общей формулы (II) где Ar, Е, G и Z имеют вышеуказанные значения; R представляет собой С1-С4-алкил, подвергают взаимодействию с гидроксиламином или его галоидводородной солью при необходимости в присутствии акцептора кислоты и при необходимости в присутствии разбавителя, полученный продукт подвергают взаимодействию с двузамещенными алканами общей формулы (III) где А имеет вышеуказанное значение; Х – галоген, алкилсульфонилокси или фенилсульфонилокси, при необходимости в присутствии акцептора кислоты и при необходимости в присутствии разбавителя с последующим выделением целевого продукта. 3. Способ получения замещенных азадиоксоциклоалкенов общей формулы (I) где А – диметилен (этан-1,2-диил); Ar – орто-фенилен; Е – группа формулы G – кислород или группа -CH2-O-; Z – фенил, пиримидинил, замещенные метилом, этилом, фтором, хлором, бромом, феноксигруппа, замещенная циано, отличающийся тем, что гидроксиариловые соединения общей формулы (IV) где А, Ar и Е имеют вышеуказанные значения, подвергают взаимодействию с соединениями общей формулы (V) где Z имеет вышеуказанные значения; m означает 0 или 1; Х означает галоген, при необходимости в присутствии акцептора кислоты и при необходимости в присутствии разбавителя с последующим в случае необходимости переведением группы Z в желаемое значение и выделением целевого продукта. 4. Способ получения замещенных азадиоксоциклоалкенов общей формулы (1) где А – диметилен (этан-1,2-диил); Ar – ортофенилен; Е – группа формулы G – группа -O-СН2-; Z – фенил, замещенный метилом или этилом, отличающийся тем, что галогенметиловые соединения общей формулы (VI) где А, Ar и Е имеют вышеуказанные значения; X1 означает галоген, подвергают взаимодействию с соединениями общей формулы (VII) где Z имеет вышеуказанное значение, при необходимости в присутствии акцептора кислоты и при необходимости в присутствии разбавителя с последующим выделением целевого продукта. 5. Способ получения замещенных азадиоксоциклоалкенов общей формулы (I) где А – диметилен (этан-1,2-диил); Ar – ортофенилен; Е – группа формулы G – группа -СН2-O-; Z – фенил, замещенный метилом или этилом, отличающийся тем, что гидроксиалкиламиды общей формулы (VIII) где А, Ar, Е, G и Z имеют вышеуказанные значения, подвергают циклизации водоудаляющим средством при необходимости в присутствии разбавителя. 6. Соединения формулы (IV) где А – диметилен (этан-1,2-диил); Ar – ортофенилен; Е – группа формулы в качестве промежуточных продуктов для соединений формулы (I). 7. Соединения формулы (IX) где А – диметилен (этан-1,2-диил); Ar – ортофенилен; Е – группа формулы в качестве промежуточных продуктов для соединений формулы (I). 8. Соединения формулы (VI) где А – диметилен (этан-1,2-диил); Ar – ортофенилен; Е – группа формулы X1 – галоген, в качестве промежуточных продуктов для соединений формулы (I). 9. Соединения формулы (XIII) где А – диметилен (этан-1,2-диил); Ar – ортофенилен; Е – группа формулы в качестве промежуточных продуктов для соединений формулы (I). 10. Соединения формулы (VIII) где А – диметилен (этан-1,2-диил); Ar – ортофенилен; Е – группа формулы G – группа -СН2-О-; Z – фенил, замещенный метилом, в качестве промежуточных продуктов для соединений формулы (I). 11. Фунгицидные средства, отличающиеся тем, что они содержат соединение формулы (I) по п.1 в качестве активного вещества. 12. Способ получения фунгицидных средств по п.11, отличающийся тем, что соединения формулы (I) по п.1 смешивают с наполнителями и/или поверхностно-активными веществами. 13. Способ борьбы с нежелательными грибами, отличающийся тем, что соединениями формулы (I) по п.1 обрабатывают грибы и/или их биотоп.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

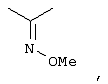
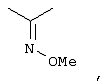
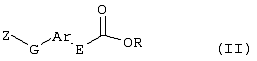

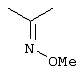
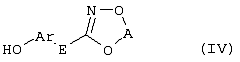


 -метоксимино-
-метоксимино-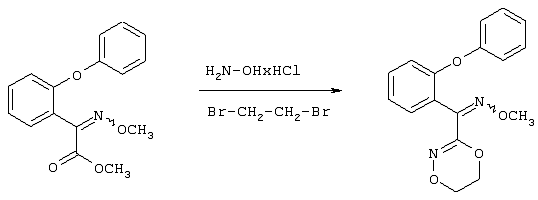
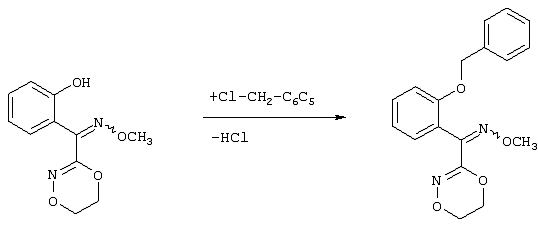
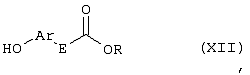
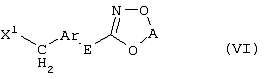
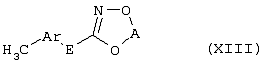
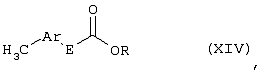
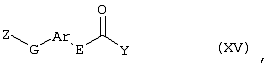
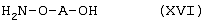
 -циано-N-метилэтанимидамиды,
-циано-N-метилэтанимидамиды,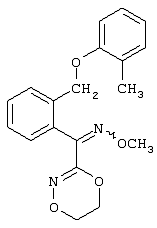
 (см. табл.1).
(см. табл.1).