|
(21), (22) Заявка: 2003135172/13, 04.12.2003
(24) Дата начала отсчета срока действия патента:
04.12.2003
(45) Опубликовано: 27.07.2005
(56) Список документов, цитированных в отчете о
поиске:
US 4,895,795, 23.01.1990. US 5,496,700, 05.03.1996. RU 2008684 С1, 28.02.1994. RU 2160583 С1, 20.12.2000.
Адрес для переписки:
141306, Московская обл., г. Сергиев Посад, Вирусологический центр НИИ Микробиологии Министерства обороны Российской Федерации, Начальнику центра
|
(72) Автор(ы):
Ручко С.В. (RU),
Чуркин И.А. (RU),
Лебедев В.Н. (RU),
Паныгина С.А. (RU),
Хамитова М.Ф. (RU),
Плеханова Т.М. (RU),
Ярош А.Г. (RU),
Харченко В.А. (RU),
Ионов С.Н. (RU),
Максимов В.А. (RU)
(73) Патентообладатель(и):
Вирусологический центр НИИ Микробиологии Министерства обороны Российской Федерации (RU)
|
(54) ШТАММ ГИБРИДНЫХ КЛЕТОК С3/S-3E5 ЖИВОТНЫХ MUS MUSCULUS L., ПРОДУЦИРУЮЩИХ МОНОКЛОНАЛЬНЫЕ АНТИТЕЛА К КОКСИЕЛЛАМ БЕРНЕТА
(57) Реферат:
Изобретение относится к гибридомной технологии и представляет собой новый штамм гибридных клеток C3/S-3E5 животных Mus musculus L., продуцирующих в клеточных культурах и брюшной полости сингенных животных моноклональные антитела (далее МКАт) к коксиеллам Бернета (штамм “Грита”). В результате слияния миеломы мыши линии Sp-2/0 и спленоцитов мышей BALB/c, иммунизированных инактивированным формалином концентрированным очищенным препаратом коксиелл Бернета (штамм “Грита”), при использовании в качестве сливающего агента полиэтиленгликоля с молекулярной массой 1000 и последующего клонирования методом предельных разведений получена гибридома C3/S-3E5, продуцирующая МКАт к данному возбудителю. Специфичность полученных МКАт: отсутствие перекрестных реакций в ИФА с антигеном риккетсий Провачека, а также с неинфицированным субстратом накопления. С помощью полученных МКАт можно проводить специфическое выявление коксиелл Бернета методом ИФА (прямой и непрямой варианты). Чувствительность ИФА на основе данных МКАт составляет 2,0· 103 ИД50· см-3 для белых крыс. Использование изобретения позволяет выявить и идентифицировать возбудителей риккетсиозной этиологии. 1 ил., 3 табл.
Изобретение относится к области микробиологии и биотехнологии, а именно к гибридомной технологии, и представляет собой новый штамм гибридных клеток C3/S-3E5 животных Mus musculus L., продуцирующих в клеточных культурах и брюшной полости сингенных животных моноклональные антитела (далее МКАт) к коксиеллам Бернета (штамм “Грита”), который может быть использован в научных исследованиях и при изготовлении медицинских иммунобиологических препаратов.
Изобретение может быть использовано в микробиологических и иммунологических исследованиях при создании диагностикумов для выявления в пробах от людей и переносчиков коксиелл Бернета – возбудителей лихорадки Ку.
Лихорадка Ку относится к зооантропонозам с природной очаговостью и распространена во многих странах мира [1-7]. Особенности патогенеза инфекции у человека и своеобразие клинических проявлений коксиеллеза создает большие трудности в распознавании заболевания [1,8-10].
Для обнаружения специфических антигенов возбудителей различных инфекционных заболеваний вирусной и риккетсиозной этиологии в последнее время широкое применение получили иммунохимические методы, в частности иммуноферментный анализ (далее ИФА). Одним из наиболее перспективных направлений повышения эффективности ИФА является использование МКАт как антителсодержащего субстрата, применяемого в качестве диагностикума. Однако вопрос о возможности использования МКАт для выявления и идентификации возбудителей риккетсиозной этиологии остается до настоящего времени нерешенным.
Применение МКАт к коксиеллам Бернета для диагностики лихорадки Ку на ранней стадии заболевания может исключить ложноположительные реакции, нередко возникающие при использовании тест-систем на основе поликлональных иммунных сывороток. Необходимо также отметить, что использование МКАт позволит создавать стандартизованные тест-системы за счет возможности применения антител постоянной авидности и специфичности.
При разработке на основе МКАт диагностикумов, предназначенных для выявления возбудителей опасных и особо опасных инфекционных заболеваний вирусной и риккетсиозной этиологии, актуальным является вопрос получения достаточной биомассы последних. С этой целью проводят культивирование клеток гибридом различными методами in vitro или in vivo.
Перспективным направлением исследований является выбор и обоснование условий метода культивирования гибридом in vitro, позволяющих получать биомассу МКАт, количественно сопоставимую с таковой при выращивании клеток гибридом in vivo.
Целью настоящего изобретения является получение гибридомы, продуцирующей МКАт к коксиеллам Бернета, которые используют в качестве антителсодержащего субстрата в серологических тестах при выявлении и идентификации данного возбудителя.
Сущность изобретения состоит в том, что в результате слияния миеломы мыши линии Sp-2/О и спленоцитов мышей BALB/c, иммунизированных инактивированным очищенным концентрированным антигеном коксиелл Бернета, при использовании в качестве сливающего агента полиэтиленгликоля (далее ПЭГ) с молекулярной массой 1000 и последующего клонирования методом предельных разведений получена гибридома C3/S-3E5, продуцирующая МКАт к коксиеллам Бернета. Данные МКАт позволяют проводить специфическое выявление коксиелл Бернета методом ИФА (прямой и непрямой варианты). Чувствительность ИФА на основе МКАт составляет 2,0· 103 ИД50· cм-3.
Пример выполнения
Полученный штамм гибридных клеток C3/S-3E5 животных Mus musculus L., продуцирующих моноклональные антитела к коксиеллам Бернета, обладает следующими характеристиками:
1. Родословная гибридомы представлена на чертеже.
2. Число пассажей к моменту паспортизации составляет 14 раз.
3. Стандартные условия выращивания in vitro:
– посевная концентрация при выращивании in vitro 2,0· 105 кл· см-3;
– среда культивирования – среда Игла в модификации Дюльбекко (DMEM) с добавлением 10% фетальной телячьей сыворотки (далее ФТС);
– температура культивирования (37±0,5)° С;
– содержание СО2 в атмосфере культивирования 5%.
4. Культуральные свойства штамма
Штамм является монослойно-суспензионным: около 30% клеток находятся в суспензии, не прикрепляясь к поверхности культурального сосуда. Частота пассирования при посевной дозе 2,0· 105 кл· см-3 составляет от 3 до 4 суток. Индекс пролиферации при выращивании in vitro равен 7,2.
5. Ростовые (кинетические) характеристики гибридомы представлены таблице 1. 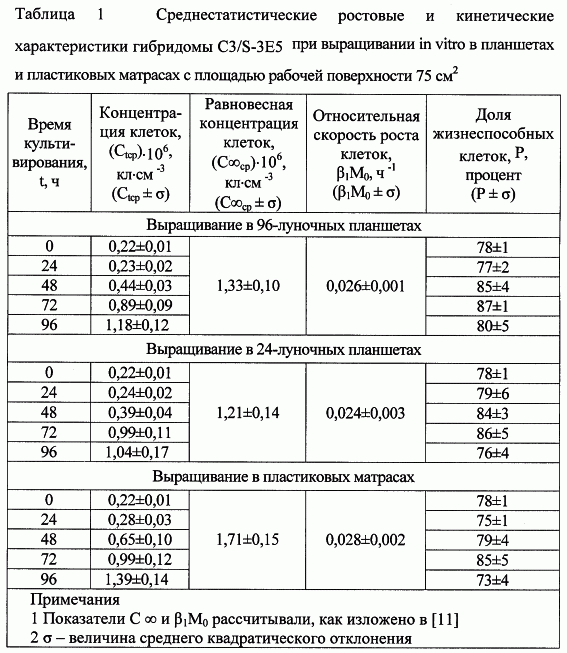
6. Характеристика культивирования в организме животного
При внутрибрюшинном введении мышам BALB/c от 2,0· 106 до 5,0· 106 клеток гибридомы на 9-21 сутки формируются серозные опухоли. От одной мыши получают от 2,0 до 3,0 см3 иммунной асцитической жидкости (далее ИАЖ). Концентрация клеток гибридомы в ИАЖ составляет от 30· 106 до 50· 106 кл· см-3.
7. Цитогенетическая (кариологическая) характеристика:
– модальный класс от 88 до 96 хромосом;
– доля клеток в модальном классе – 54%;
– модальный класс для родительской миеломной линии Sp-2/O – от 57 до 59 хромосом.
8. Цитоморфологическая характеристика
Клон гибридомы представлен крупными округлыми клетками с размерами от 20 до 25 мкм, близкими по морфологии клеткам исходной миеломы линии Sp-2/O.
9. Видовая принадлежность Mus musculus.
10. Онкогенность
Гибридома при внутрибрюшинном введении вызывает серозные (в 70% случаев) и солидные опухоли.
11. Маркерные характеристики
Клон продуцирует МКАт к коксиеллам Бернета.
12. Контроль контаминации
Грибковая и бактериальная микрофлора в культуре штамма гибридомы отсутствует.
13. Биотехнологическая характеристика
Штамм продуцирует МКАт к коксиеллам Бернета:
– титр МКАт при выращивании in vitro – 1:2560 (в ИФА);
– титр МКАт при выращивании in vivo – 1:163840 (в ИФА).
Характеристика продуцируемых МКАт к коксиеллам Бернета:
– белок-мишень – антиген I фазы коксиелл Бернета, структурный белок с молекулярной массой (ММ) 62 кДа;
– изотип продуцируемых иммуноглобулинов – IgG;
– количество изученных пассажей: in vitro – 14; in vivo – 5.
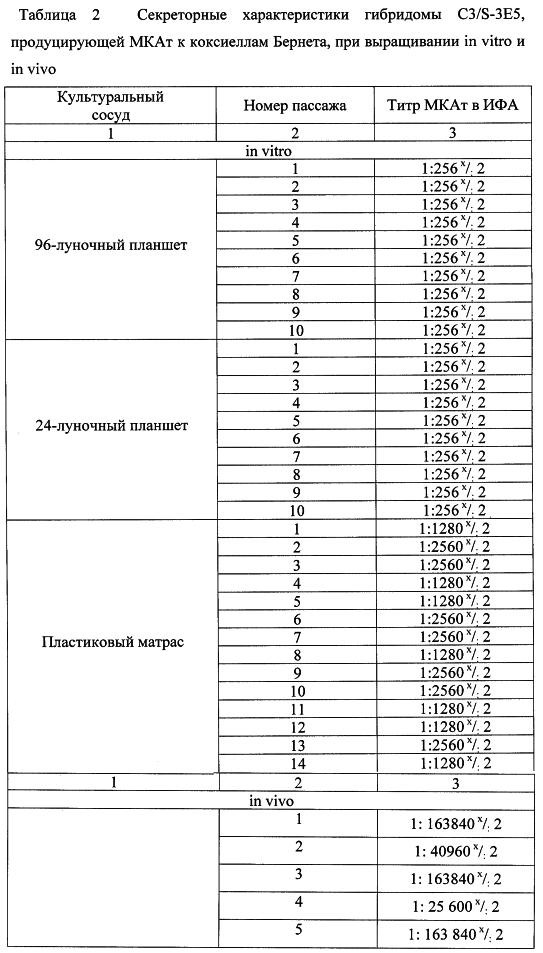
Секреторные характеристики гибридомы C3/S-3E5 представлены в таблице 2.
14. Способ криоконсервации
Осадок клеток, полученный после низкоскоростного центрифугирования, ресуспендируют в среде, содержащей 90% ФТС и 10% диметилсульфоксида (DMSO), доводят до конечной концентрации 3,0· 106 кл· см-3 и разливают в пластиковые ампулы по 0,5 см3. Ампулы охлаждают до температуры минус 70° С в установке для программного замораживания при скорости замораживания от 1 до 2° С в минуту и затем помещают в сосуд Дьюара с жидким азотом.
Клетки гибридомы C3/S-3E5, выращенные in vitro в 24-луночных планшетах до конечной концентрации от 1,0· 106 до 1,5· 106 кл· см-3, осаждают с помощью низкоскоростного центрифугирования и вводят внутрибрюшинно мышам линии BALB/c, предварительно (за 7 суток) обработанным адъювантом Пристана, в количестве от 2,0· 106 до 5,0· 10 клеток в объеме 0,5 см3. На 9-21 сутки после введения гибридомы примерно у 70% животных формируются асцитные опухоли. Клетки гибридомы осаждают из ИАЖ с помощью низкоскоростного центрифугирования (1500 об· мин -1 в течение 10 минут) и используют для последующего пассажа in vivo. Супернатант, содержащий МКАт в высоких титрах, используют в качестве полуфабриката для выделения иммуноглобулина, который используют для получения диагностикума. Данные по чувствительности и специфичности ИФА на основе МКАт C3/S-3E5 представлены в таблице 3.
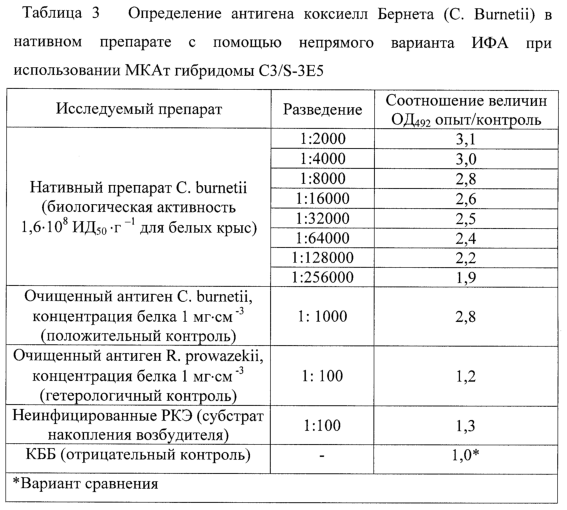
Как показывает анализ данных, представленных в таблице 3, чувствительность непрямого варианта ИФА на основе МКАт при определении коксиелл Бернета (С. Bumetii) в составе нативного препарата составляет 1,2· 103 ИД50· г-1. Специфичность непрямого варианта ИФА на основе МКАт подтверждена отсутствием положительной реакции с антигеном риккетсий Провачека (R. Prowazekii) [12].
Источники информации
11. Васильев Н.Н., Амбросов В.А., Складнев А.А. Моделирование процессов микробиологического синтеза. – М.: Лесная промышленность, 1975.
Формула изобретения
Штамм гибридных клеток C3/S-3E5 животных Mus musculus L., продуцирующих в течение 14 изученных пассажей in vitro моноклональные антитела к коксиеллам Бернета (штамм “Грита”), относящиеся к изотипу IgG, пригодные для приготовления на их основе диагностикумов для специфического выявления коксиелл Бернета (1-й фазы) с помощью иммуноферментного анализа.
РИСУНКИ
|