|
|
(21), (22) Заявка: 2000129927/15, 01.12.2000
(24) Дата начала отсчета срока действия патента:
01.12.2000
(43) Дата публикации заявки: 20.10.2002
(45) Опубликовано: 27.07.2005
(56) Список документов, цитированных в отчете о
поиске:
RU 2105000 С1 20.02.1998. RU 2124888 С1 20.01.1999. RU 2032661 С1 10.04.1995. RU 2098085 С1 10.12.1997. SI 9011538 A 31.08.1998. US 5371088 A1 06.12.1994. WO 9730703 A1 28.08.1997.
Адрес для переписки:
191186, Санкт-Петербург, а/я 230, “АРС-Патент”, пат.пов. С.В. Новоселовой, рег.№ 622
|
(72) Автор(ы):
Медведев Ю.В. (RU),
Соболев Д.В. (RU),
Александрова А.Е. (RU)
(73) Патентообладатель(и):
Соболев Дмитрий Владимирович (RU)
|
(54) НАТРИЕВАЯ СОЛЬ ПОЛИ(ПАРАДИГИДРОКСИ- ПАРАФЕНИЛЕН)ТИОСУЛЬФОКИСЛОТЫ В КАЧЕСТВЕ РЕГУЛЯТОРА МЕТАБОЛИЗМА КЛЕТОК И АНТИГИПОКСАНТА, ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ НА ЕЕ ОСНОВЕ
(57) Реферат:
Изобретение относится к фармакологии и медицине, а также может быть использовано в косметологии и пищевой промышленности, и касается препаратов, регулирующих метаболизм отдельно взятых клеток и их сообщества в биологических тканях.Предложена натриевая соль поли (пара-дигидрокси-пара-фенилен) тиосульфокислоты общей формулы
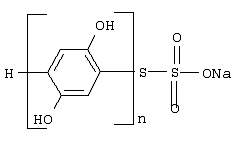
где n = 2-6,
в качестве регулятора метаболизма клеток и антигипоксанта. Также предложена фармацевтическая композиция на основе указанного соединения. Использование соединения обеспечивает выраженный антигипоксический эффект. 2 н. и 2 з.п. ф-лы, 10 табл., 4 ил.
ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к фармакологии и медицине, а также может быть использовано в косметологии и пищевой промышленности, и касается препаратов, регулирующих метаболизм отдельно взятых клеток и их сообщества в биологических тканях.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Для защиты тканей от повреждающего воздействия гипоксии или реоксигенации предложено использовать антигипоксанты. В настоящее время выделяют 5 типов подобных препаратов (Смирнов А.В., Криворучко Б.И. Сб.: Применение инфузионных антигипоскантов и искусственных переносчиков кислорода в хирургии, – СПб.: 1999, с.53-62, [2]).
К первой группе относят препараты типа гутимина и амтизола, которые усиливают гликолиз и повышают синтез аденозинтрифосфата (АТФ) в результате процесса анаэробного окисления субстрата.
Вторую группу антигипоксантов составляют вещества макроэргической природы (креатинфосфат, АТФ).
Остальные три группы антигипоксантов составляют препараты, регулирующие активность главной энергопродуцирующей системы клеток – митохондриальной дыхательной цепи. В частности, в третью группу включены препараты, поддерживающие высокую активность одного из двух субстратных участков дыхательной цепи – сукцинатоксидазного. К этой группе относится янтарная кислота, оксибутират натрия, препараты мексидол и муфасол.
К четвертой группе антигипоксантов относят синтетические препараты с электроноакцепторными свойствами, представляющие собой производные хинонов.
В пятую группу антигипоксантов включены цитохром С и убихинон Q10 (коэнзим Q10), являющиеся естественными компонентами митохондриальной дыхательной цепи.
Среди перечисленных антигипоксантов особый интерес представляет убихинон Q10, поскольку в митохондриальной цепи он играет ключевую роль в переносе электронов от субстратных участков (никотинамидадениндинуклеотид оксидазы (НАДН-оксидазы) или сукцинатоксидазы) на цитохромную цепь.
Дефицит убихинона Q10 блокирует перенос электронов по дыхательной цепи и ведет к прекращению синтеза АТФ.
При изучении соотношения между убихиноном и остальными партнерами по дыхательной цепи было обнаружено преобладание на порядок первого над остальными компонентами. Кажущаяся “расточительность” природы, использовавшей при конструировании дыхательной цепи большой избыток одного из элементов конструкции по сравнению с остальными, удалось понять, изучив более детально механизм функционирования коэнзима Q10. Оказалось, что реальным партнером, непосредственно участвующим во взаимодействии с субстратными участками дыхательной цепи, является не убихинон Q10, а его полувосстановленная свободнорадикальная форма – убисемихинон (Nohl H. Free Rad. Res. Communs, 1990, Vol.8, No.4-6, р.307-315, [3]). Поскольку пордолжительность жизни убисемихинона крайне мала, и он диспропорционирует на убихинон Q10 и убихинол Q10 (восстановленную форму убихинона), избыток коэнзима необходим для поддержания оптимальной концентрации убисемихинона.
Учитывая важную роль молекул, содержащих неспаренный электрон, в работе митохондриальной дыхательной цепи, одной из задач исследования было получение продукта, способного более продолжительное время по сравнению с убисемихиноном находиться в свободнорадикальном состоянии, и оценка эффективности его антигипоксической активности.
Наиболее близким структурным аналогом предложенного соединения является натриевая соль [поли-(2,5-дигидрокси-фенилен)]-4-тиосульфокислоты (мета НПФ), состоящей из последовательно соединенных между собой в мета-положении гидрохиноидных звеньев, имеющих в крайнем звене заместитель в виде натриевой соли тиосульфокислоты. Продукт получают взаимодействием пара-бензохинона с тиосульфатом натрия в водно-спиртовой среде при температуре выше 65°С. Показано, что продукт влияет на метаболизм клеток (Патент РФ №2105000, МПК6: С 07 С 381/02, C 08 G 61/10, А 61 К 31/05, [4]).
В современной фармакологии известны почти две тысячи различных регуляторов клеточного метаболизма, из которых только около ста являются препаратами фенольного типа (Машковский М.Д. Лекарственные средства. Изд. 13-е в двух томах. – Харьков: Торсинг, 1997, [5]).
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Задачей настоящего изобретения является расширение спектра препаратов, регулирующих метаболическую активность клеток, в том числе проявляющих антигипоксическую активность.
В результате проведенных исследований было показано, что желаемой активностью – способностью регулировать метаболизм клеток, в том числе регулировать их энергетический обмен – обладает натриевая соль поли(пара-дигидроски-пара-фенилен)тиосульфокислоты (далее также для краткости называемая “пара-НПФ”), имеющая следующую структурную формулу:
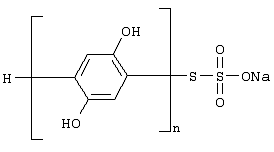
где n=2-6.
Брутто-формула продукта: C6nH4n+1O2n+3S2Na.
Продукт был получен в результате реакции пара-бензохинона с тиосульфатом натрия в водной среде при нагревании от 50 до 100°С. Образующийся в результате реакции продукт отделяют от растворителя, очищают от низкомолекулярных примесей с помощью диэтилового эфира и сушат от экстрагента под вакуумом при температуре 50°С. Более подробно условия синтеза продукта и его свойства описаны в нижеследующих примерах.
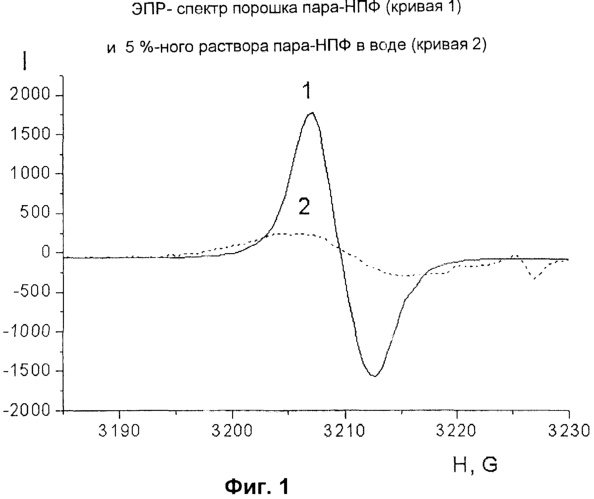
Принципиальное отличие предложенного соединения от его аналога заключается в том, что известное соединение состоит из звеньев гидрохинона, соединенных между собой в мета-положении, тогда как в предложенном соединении эти звенья расположены в пара-положении. Как известно, изменение химической структуры вещества неизбежно связано с изменением его свойств. Из химии ароматических соединений известно, что заместители, расположенные в мета-положении ароматического ядра, оказывают слабое взаимное влияние друг на друга, тогда как заместители, расположенные в пара-положении, сильно влияют друг на друга и на молекулу в целом. Наиболее ярким проявлением особых свойств продукта, предложенного в соответствии с настоящим изобретением, по сравнению с аналогом является проявление характерного сигнала, регистрируемого с помощью метода спектроскопии электронного парамагнитного резонанса (ЭПР-спектроскопии), свидетельствующего о наличии в образцах пара-НПФ неспаренных электронов, которые не были зафиксированы в образцах аналога (Фиг.1). Важно отметить также, что в отличие от малостабильного убисемихинона, для регистрации спектра которого применяют замораживание, ЭПР-спектры образцов пара-НПФ сохраняют устойчивость месяцами в условиях комнатной температуры. Наличие стабильного сигнала ЭПР в образцах пара-НПФ связано с проявлением сильного взаимодействия между всеми фенильными ядрами, соединенными друг с другом в пара-положении, при этом образуется достаточно протяженная система сопряжения, обеспечивающая эффективную стабилизацию неспаренного электрона в пределах молекулы. Спектр ЭПР наблюдается как для твердого пара-НПФ (кривая 1 на Фиг.1), так и для его водного раствора (кривая 2 на Фиг.1).
Проверка возможного влияния пара-НПФ на аэробный энергетический метаболизм проводилась на изолированных митохондриях скелетных мышц. Оценивалось влияние препарата на скорости эндогенного дыхания митохондрий (V0), дыхания митохондрий в метаболических состояниях 3 (V3) и 4 (V4) по Чансу, а также скорость разобщенного дыхания в присутствии разобщителя – 2,4-динитрофенола (VДНФ). Рассчитывался коэффициент дыхательного контроля по Чансу-Вильямсу (ДКч-в) и коэффициент фосфорилирования (АДФ/О) (Краковский М.Э., Аширметов А.X., Иноятова Ф.X. Вопр. мед. химии, 1986, т.32, №6, с.66-70, [6]). Результаты представлены в Таблице 1.
Таблица 1
Влияние препарата пара-НПФ на дыхание и фосфорилирование изолированных митохондрий скелетных мышц крыс |
| Показатели |
Контроль |
Конц пара-НПФ (мкМ/л) |
| 1,2 |
2,4 |
6,0 |
| V0 |
15,0 |
16,1 |
17,9 |
22,6 |
| V3 |
113,0 |
85,7 |
83,9 |
60,4 |
| V4 |
46,3 |
26,0 |
22,3 |
21,7 |
| VДНФ |
82,4 |
62,5 |
54,5 |
52,8 |
| ДКЧ-В |
2,4 |
3,3 |
3,8 |
2,8 |
| АДФ/О |
1,75 |
1,94 |
2,63 |
1,85 |
Из Таблицы 1 следует, что пара-НПФ активно влияет на аэробный энергетический метаболизм, при этом достигаемый эффект зависит от дозы препарата. Значения дыхательного контроля (ДКЧ-В) и коэффициента сопряженности окислительного фосфорилирования и дыхания (АДФ/О) по мере увеличения концентрации пара-НПФ вначале растут, что соответствует более эффективной энергопродуцирующей функции митохондрий, а затем падают (разобщающий эффект).
При внесении пара-НПФ в состав глюкозо-минеральной питательной среды, содержащей (г/л) глюкозу – 4, Na2HPО4 – 7, КН2РО4 – 3, NH4Cl – 1, NaCl – 0,5, MgSO4 – 0,2, СаСl2 – 0,02, никотиновую кислоту – 0,005, пара-НПФ – 0,02, при культивировании факультативных аэробов Escherichia coli штамм М-17 время генерации микробной популяции на стадии логарифмического роста культуры сокращалось на 24±12% по сравнению с контролем (эффект стимуляции роста). Внесение 50 мг/л пара-НПФ в культуральную жидкость замедляет развитие микробных клеток (эффект ингибирования роста).
Представленные результаты показывают, что пара-НПФ участвует в регуляции метаболических процессов как в случае прокариотических, так и эукариотических клеток. Возможность повышения сопряженности процессов фосфорилирования и дыхания, подтвержденная на модели изолированных митохондрий скелетных мышц, позволяет рассматривать пара-НПФ в качестве активного антигипоксанта прямого действия.
Предложенная в соответствии с настоящим изобретением натриевая соль поли(пара-дигидрокси-пара-фенилен)тиосульфокислоты может быть применена в качестве антигипоксического препарата в составе фармацевтической композиции в любой подходящей фармацевтической форме, известной специалистам в данной области, например в форме таблетки, капсулы или раствора. Фармацевтическая композиция также может включать известные фармацевтически приемлемые наполнители, разбавители, связующие вещества и носители. Доза фармацевтической композиции должна содержать, в зависимости от назначения, по меньшей мере, терапевтически или профилактически эффективное количество активного соединения – натриевой соли поли(пара-дигидрокси-пара-фенилен)тиосульфокислоты.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фиг.1 изображен спектр электронного парамагнитного резонанса (ЭПР-спектр) молекулы натриевой соли поли(пара-дигидроски-пара-фенилен)тиосульфокислоты (пара-НПФ). Кривая 1 представляет собой ЭПР-спектр порошка пара-НПФ, а кривая 2 – ЭПР-спектр, полученный при 20-кратном разбавлении пара-НПФ водой (ЭПР-спектр 5%-ного водного раствора пара-НПФ).
На Фиг.2 представлен ИК-спектр пара-НПФ в таблетке КВг.
На Фиг.3 изображены УФ-спектры поглощения водного раствора пара-НПФ (кривая 3) и водного раствора гидрохинона (кривая 4).
На Фиг.4 изображен 13С-ЯМР спектр пара-НПФ в твердой фазе.
ОПИСАНИЕ ПРИМЕРОВ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Для лучшего понимания сути изобретения приведены следующие примеры.
Пример 1.
В аппарат емкостью 2 л, снабженный мешалкой и рубашкой, помещают 76,6 г (0,31 М) тиосульфата натрия в 1 л дистиллированной воды. Раствор нагревают до температуры 50°С и при интенсивном перемешивании вводят 100 г (0,93 М) пара-бензохинона. Через 2,5 часа процесс прекращают и образовавшийся продукт сушат на распылительной сушилке. Сухой порошкообразный продукт помещают в аппарат Сокслетта и удаляют примеси с помощью диэтилового эфира в качестве экстрагента. Время экстракции – 24 часа. Затем продукт сушат под вакуумом при температуре 50°С. Выход целевого продукта 102,7 г. Молекулярная масса, определенная криоскопическим методом, равна 440. Содержание серы по данным элементного анализа составляет 16,2%.
На Фиг.2 представлен ИК-спектр образца в таблетке КВг. На нем видна широкая полоса поглощения в области 3600-2000 см-1, относящаяся к валентным колебаниям НО-групп; полосы при 1200 и 1040 см-1 относятся к валентным колебаниям SО3-групп. Набор полос в области 1600-1500 см-1 относится к валентным колебаниям связей С=С в ароматическом кольце, а полоса при 830 см-1 связана с неплоскими деформационными колебаниями связи С-Н в тетразамещенном бензольном кольце.
На Фиг.3 представлены УФ-спектры растворов пара-НПФ (кривая 3) и гидрохинона (кривая 4) в воде. Гидрохинон можно рассматривать в качестве модельного соединения для элементарного звена пара-НПФ. Два слабо выраженных пика в области 45000 и 33000 см-1, наблюдаемые в спектре пара-НПФ, смещены в более низкочастотную область по сравнению с характерными полосами поглощения гидрохинона 45200 и 32780 см-1. Подобное смещение, а также непрерывное поглощение образца от ультрафиолетовой (УФ-) до видимой области спектра свидетельствует об эффективном сопряжении в синтезированном продукте.
Пример 2.
В аппарат, описанный в примере 1, помещают 23 г (0,093 М) тиосульфата натрия в 1 л дистиллированной воды, раствор нагревают до 90°С и вводят при интенсивном перемешивании 100 г (0,93 М) пара-бензохинона. Через 1,5 часа реакцию прекращают и содержимое сушат на распылительной сушилке. Выделенный сухой продукт экстрагируют диэтиловым эфиром в течение 24 часов, затем сушат под вакуумом при температуре 50°С. Выход целевого продукта 80,2 г. По данным элементного анализа содержание серы составляет 10,8%, молекулярная масса полученного продукта равна 750.
Присоединение гидрохиноидных звеньев в синтезированном образце в пара-положении друг относительно друга подтверждается данными спектроскопии ядерного магнитного резонанса 13С-ЯМР по наличию полосы поглощения при 147,87 м.д., характерной для Саром.-Саром. связи между бензольными кольцами (Фиг.4).
Пример 3. Оценка влияния пара-НПФ на метаболизм клеток
Для оценки влияния пара-НПФ, полученного в примере 1, на метаболическую активность клеток была использована культура гриба Aspergillus oryzae, являющегося продуцентом амилолитических ферментов. Данный гриб относится к строгим аэробам и выращивается на плотных питательных средах. Из-за ограничений с диффузией кислорода воздуха внутрь “коржа” эффективность продуцирования амилолитических ферментов прогрессивно снижается по мере увеличения толщины слоя плотной питательной среды. В таблице 2 приведены данные по амилолитической активности гриба из проб, взятых из образцов с толщиной “коржа” 1, 3 и 4 см.
Таблица 2
Влияние пара-НПФ на амилолитическую активность гриба Aspergillus oryzae |
| Толщина “коржа”, см |
Концентрация пара-НПФ, мг/л |
| 25 |
50 |
100 |
| Контроль |
Опыт |
Эффект, % |
Контроль |
Опыт |
Эффект, % |
Контроль |
Опыт |
Эффект, % |
| 1 |
394 |
362 |
-8 |
394 |
397 |
-1 |
327 |
370 |
15 |
| 3 |
233 |
299 |
28 |
233 |
286 |
23 |
210 |
226 |
8 |
| 4 |
168 |
156 |
-7 |
168 |
246 |
46 |
141 |
172 |
22 |
Из таблицы 2 видно, что вблизи поверхности плотной питательной среды, где условия аэрации максимально благоприятны для развития культуры, добавка пара-НПФ мало сказывается на амилолитической активности гриба. Однако по мере увеличения толщины “коржа” с ростом ограничений по диффузии кислорода амилолитическая активность гриба снижается. В этих условиях добавление пара-НПФ в питательную среду заметно повышает амилолитическую активность гриба Aspergillus oryzae.
Пример 4. Оценка антигипоксической активности пара-НПФ
В аппарат, описанный в примере 1, помещают 38,3 г (0,15 М) тиосульфата натрия в 1 л дистиллированной воды, раствор нагревают до 70°С и при интенсивном перемешивании вводят 100 г (0,93 М) пара-бензохинона. Через 2 часа реакцию прекращают и содержимое сушат на распылительной сушилке. Полученный продукт экстрагируют в течение суток диэтиловым эфиром и сушат от экстрагента под вакуумом при 50°С. Выход целевого продукта – 95,7 г. По данным элементного анализа содержание серы составляет 11,7%. Молекулярная масса полученного образца равна 650.
Оценку антигипоксического действия пара-НПФ проводили на модели гипоксической гипоксии при моделировании в барокамере подъема на высоту 12000 м над уровнем моря. В качестве подопытных животных использовались крысы. Использовалась барокамера с приточно-вытяжной вентиляцией, исключающей накопление углекислого газа. Был использован следующий режим “подъема” животных: первые 5000 м – за 3 минуты, каждые последующие 1000 м – за 1 минуту. На высоте 12000 м производили экспозицию крыс в течение 45 минут. Эффективность препарата оценивалась по следующим показателям: выживаемость животных (в %), продолжительность жизни на высоте (мин), коэффициент эффективности антигипоксического воздействия препарата ( ), определяемый по отношению продолжительности жизни на высоте животных, получивших препарат, к продолжительности жизни животных в контрольной группе контролю. В качестве эталонного препарата был использован убихинон Qio. Результаты опыта представлены в Таблице 3. ), определяемый по отношению продолжительности жизни на высоте животных, получивших препарат, к продолжительности жизни животных в контрольной группе контролю. В качестве эталонного препарата был использован убихинон Qio. Результаты опыта представлены в Таблице 3.
Таблица 3
Сравнительная антигипоксическая активность пара-НПФ и убихинона Q10 в оптимальных дозах на модели гипоксической гипоксии (крысы) |
| Условия опыта |
Число крыс |
Доза препарата, мг/кг |
Время введения препарата до подъема |
Выживаемость, % |
Продолжительность жизни крыс, мин |
 |
| Контроль |
20 |
0 |
45 |
0 |
12±1,7 |
3,5±0,3 |
| Пара-НПФ |
20 |
10 |
45 |
80 |
41,5±2,2 |
| Контроль |
20 |
о |
80 |
0 |
9,6±1,7 |
2,3±0,4 |
| Убихинон Q10 |
20 |
200 |
80 |
0 |
22,8±0,6 |
На модели гипоксической гипоксии преимущество пара-НПФ по сравнению с убихиноном Q10 проявилось как в увеличении продолжительности жизни животных при экспозиции “на высоте” 12000 м, так и в выживаемости 80% крыс, тогда как все контрольные животные и животные, получившие убихинон Q10, погибли.
В таблице 4 представлены результаты сравнительной эффективности пара-НПФ и убихинона Q10 на модели гистотоксической гипоксии. В эксперименте использовали мышей, которым вначале вводили внутрибрюшинно антигипоксанты, а через 45 минут – летальную дозу цианида калия, составляющую 15 мг/кг массы.
Таблица 4
Сравнительная антигипоксическая активность пара-НПФ и убихинона Q10 на модели гистотоксической гипоксии (доза цианида калия 15 мг/кг, внутрибрюшинно) |
| Условия опыта |
Число животных |
Доза препарата, мг/кг |
Число выживших животных |
Продолжительность жизни животных, мин |
 |
| Контроль |
68 |
0 |
0 |
2,53±0,18 |
– |
| Пара-НПФ |
14 |
15 |
0 |
3,81±0,26 |
1,5 |
| 10 |
35 |
1 |
5,08±0,51 |
2,0 |
| 45 |
70 |
18 |
5,38±0,48 |
2,1 |
| Убихинон Q10 |
12 |
100 |
0 |
2,55±0,14 |
1,0 |
| 16 |
200 |
0 |
3,43±0,20 |
1,4 |
Таким образом, защитный эффект пара-НПФ при введении летальной дозы цианистого калия оказался более высоким по сравнению с убихиноном Q10.
В Таблице 5 представлены результаты сравнительной эффективности пара-НПФ и убихинона Q10 на модели циркуляционной гипоксии, вызванной кровопотерей. Опыты поставлены на крысах, у которых из общей сонной артерии отбирали кровь в объеме 3 мл крови на 100 г массы животного. Препараты вводили внутрибрюшинно за 45 мин до кровопотери. Отслеживали количество выживших животных через 6, 12 и 24 часа после кровопотери.
Таблица 5
Сравнительная антигипоксическая активность пара-НПФ и убихинона Q10 на модели циркуляционной гипоксии, вызванной кровопотерей |
| Условия опыта |
Число крыс |
Выживаемость крыс после кровопотери, % |
| 6 час |
12 час |
24 час |
| Контроль |
30 |
0 |
0 |
0 |
| пара-НПФ |
30 |
70 |
60 |
60 |
| Убихинон Q10 |
30 |
20 |
0 |
0 |
Нетрудно видеть, что на модели циркуляционной гипоксии, вызванной кровопотерей, антигипоксический эффект пара-НПФ существенно превосходит аналогичный эффект убихинона Q10.
Пример 5. Оценка острой и хронической токсичности пара-НПФ
Острую токсичность препарата определяли на мышах-самцах массой 20-25 г при внутрибрюшинном введении 7%-ного водного раствора пара-НПФ. Летальную дозу ЛД50 рассчитывали по методу Беренса. Оказалось, что летальная доза зависит от молекулярной массы препарата. Для образца пара-НПФ, описанного в примере 1 (молекулярная масса М=440), летальная доза ЛД50 составляет 520 мг/кг, для образца пара-НПФ, описанного в примере 2 (М=750), летальная доза ЛД50 составляет 920 мг/кг, а для образца пара-НПФ, описанного в примере 4 (М=650), летальная доза ЛД50 составляет 810 мг/кг.
Хроническую токсичность препарата определяли на крысах-самцах. При введении образца пара-НПФ, описанного в примере 4 (М=650), в дозе 20 мг/кг ежедневно в течение 1 года видимых изменений в поведении животных не выявлено. Проведенные гистологический исследования образцов легких, сердца, печени, почек, селезенки, щитовидной железы, скелетной мышцы не выявили патологических изменений по сравнению с контролем.
Пример 6. Сравнение биологической активности пара-НПФ и мета-НПФ
Задачей исследования было сравнение биологической активности соединения согласно изобретению (пара-НПФ) и его ближайшего структурного аналога – мета-НПФ, описанного в упомянутом выше патенте РФ №2105000. Биологическая активность мета-НПФ описана также в патенте РФ № 2124888. В качестве экстремального фактора была выбрана острая гипоксическая гипоксия.
Методика
Исследование выполнено на беспородных белых крысах-самцах массой 180-200 г в условиях хронического эксперимента. Предварительно у крыс исследовали индивидуальную устойчивость к острой гипоксической гипоксии. Для этого изучали время выживания их “на высоте” 12000 м, скорость “подъема” на высоту составляла 75 м/с. Согласно методике В.А.Березовского, определяли время устойчивости от момента достижения высоты 12000 м и до появления атонального дыхания или приступа судорог. Животные, имеющие низкую устойчивость к гипоксии, из эксперимента исключались. За неделю до основного эксперимента ежедневно внутрибрюшинно крысам I (контрольной) группы вводили 1 мл 0,9% раствора хлорида натрия (15 животных), II группы – мета-НПФ 1 мл 4% раствора (14 животных), III группы – пара-НПФ 1 мл 4% раствора (16 животных). Для всех трех препаратов доза составила 40 мг/кг. Доза мета-НПФ и пара-НПФ была предварительно подобрана в тесте физической работоспособности. Через три дня после теста с гипоксической гипоксией у животных изучали в крови маркеры неспецифической резистентности.
В нижеследующих таблицах количество животных в группе обозначено “п”.
Результаты
Приведенные в Таблице 6 результаты исследования показали, что пара-НПФ проявляет большую эффективность в отношении устойчивости к гипоксической гипоксии.
| Таблица 6 |
| Группы |
Количество животных |
Время устойчивости к гипоксии (с) |
| Минимальное |
Максимальное |
Среднее |
Ошибка среднего |
Процент от контроля |
| I (контроль) |
15 |
31 |
144 |
77,3 |
19,05 |
100 |
| II (мета-НПФ) |
14 |
44 |
217 |
114,2 |
23,44 |
147 |
| III (пара-НПФ) |
16 |
48 |
219 |
128 |
23,7 |
166 |
Результаты исследования показателей нейроэндокринной регуляции представлены в Таблице 7, белков сыворотки крови – в Таблице 8, углеводного обмена – в Таблице 9, процессов пероксидации и состояния антиоксидантной системы – в Таблице 10.
Таблица 7
Показатели нейроэндокринной регуляции (X±х) |
| Показатели |
Группы животных |
I (контроль)
п=15 |
II (мета-НПФ)
п=14 |
III (пара-НПФ)
п=16 |
| Катехоламины (мкг/л) |
2,13±0,14 |
2,67±0,06 |
1,72±0,13 |
| Адреналин (мкг/л) |
1,1+0,08 |
0,92±0,05 |
1,06±0,13 |
| Норадреналин (мкг/л) |
1,83±0,07 |
1,05±0,05 |
1,56±0,07 |
| Норадреналин (усл. ед.) Адреналин |
1,86±0,08 |
2,0±0,16 |
1,59±0,2 |
| Ацетилхолин (мкг/л) |
2,14±0,06 |
2,11±0,04 |
1,90±0,05 |
| Катехоламины (усл. ед.) Ацетилхолин |
1,67±0,08 |
0,80±0,03 |
1,47±0,06 |
| Ацетилхолин (усл. ед.) Норадреналин |
1,43±0,05 |
2,01±0,08 |
1,14±0,09 |
Примечание:  – различия достоверны – различия достоверны |
Таблица 8
Содержание белков в сыворотке крови (Х±х) |
| Показатели |
Группы животных |
I (контроль)
п=15 |
II (мета-НПФ)
п=14 |
III (пара-НПФ)
п=16 |
| Общий белок (г/л) |
68,7±1,4 |
73,2±1,8* |
79,8±1,5* |
| Альбумин (г/л) |
32,8±1,0 |
40,8±1,8* |
36,3±1,7* |
 1 – глобулины (%) 1 – глобулины (%) |
4,3±0,4 |
4,5±0,5 |
5,3±0,2 |
 2 – глобулины (%) 2 – глобулины (%) |
12,2±0,8 |
12,1±0,9 |
11,6±0,3 |
 – глобулины (%) – глобулины (%) |
12,3±0,6 |
12,5±0,7 |
12,1±0,4 |
 – глобулины (%) – глобулины (%) |
20,3±0,5 |
19,5±0,6 |
22,8±0,6 |
 1 – глобулины (%) 1 – глобулины (%) |
4,3±0,4 |
4,5±0,5 |
5,3±0,2 |
 2 – глобулины (%) 2 – глобулины (%) |
12,2±0,8 |
12,1±0,9 |
11,6±0,3 |
 – глобулины (%) – глобулины (%) |
12,3±0,6 |
12,5±0,7 |
12,1±0,4 |
 – глобулины (%) – глобулины (%) |
20,3±0,5 |
19,5±0,6 |
22,8±0,6 |
Примечание:  – различия достоверны – различия достоверны |
Таблица 9
Показатели углеводного обмена (Х±х) |
| Показатели |
Группы животных |
I (контроль)
п=15 |
II (мета-НПФ)
п=14 |
III (пара-НПФ)
п=16 |
| Глюкоза (ммоль/л) |
2,7±0,07 |
4,51±0,09 |
4,28±0,08 |
| Лакт (ммоль/л) |
183±18,5 |
185,0±20,0 |
151,0±17,0 |
| Пируват (ммоль/л) |
9,7±1,89 |
10,31±0,81 |
13,3±1,6 |
| Гликоген (отн. ед.) |
0,28±0,09 |
0,15±0,01 |
0,19±0,01 |
Г-6 ФДГ(отн. ед.) ФДГ(отн. ед.) |
53,2±3,9 |
54,0±6,0 |
43,5±3,8 |
| ЩФ (отн. ед.) |
121±6,5 |
121,0±2,0 |
105,0±6,08 |
Примечание:  – различия достоверны – различия достоверны |
Таблица 10
Показатели процессов пероксидации и состояния антиоксидантной системы(Х±х) |
| Показатели |
Группы животных |
I (контроль)
п=15 |
II (мета-НПФ)
п=14 |
III (пара-НПФ)
п=16 |
| Малоновый диальдегид (мкмол/л) |
3,3±0,13 |
3,6±0,15 |
6,1±0,36 |
| Супероксиддисмутаза (уел. ед.) |
1,83±0,06 |
2,09±0,24 |
2,1±0,19 |
| Витамин “Е” (мкмоль/л) |
3,7±0,16 |
5,31±0,51 |
7,6±0,35 |
| Дегидроаскорбиновая кислота (мкмоль/л) |
4,2±0,17 |
7,6±0,62 |
6,8±0,34 |
| Аскорбиновая кислота (мкмоль/л) |
3,9±0,14 |
17,7±1,31 |
17,66±0,78 |
| Общая аскорбиновая кислота (мкмоль/л) |
18,6±1,2 |
29,3±1,25 |
24,6±1,62 |
| Аскорбиновая / Дегидроаскорбиновая кислота (усл.ед.) |
2,1±0,12 |
3,12±0,38 |
3,21±0,24 |
| Бета-каротин (мкг/дл) |
12,3±0,9 |
17,9±4,15 |
21,3±0,59 |
| Ретинол (мкг/дл) |
8,7±0,7 |
7,7±1,29 |
12,5±3,1 |
| Восстановленный глутатион (мкмоль/л) |
1,0±0,06 |
1,1±0,03 |
1,39±0,07 |
| Окисленный глутатион (мкмоль/л) |
3,1±0,5 |
2,6±0,02 |
1,7±0,06 |
| Общий глутатион (мкмоль/л) |
12,5±0,5 |
13,4±0,04 |
18,6±0,07 |
Примечание:  – различия достоверны – различия достоверны |
ВЫВОДЫ
1. Пара-НПФ обеспечивает более выраженный антигипоксический эффект, чем мета-НПФ.
2. Действие экстремального фактора после введения в организм мета-НПФ или пара-НПФ приводит к увеличению неспецифической резистентности, при этом повышение неспецифической резистентности более выражено при использовании пара-НПФ, что свидетельствует о том, что пара-НПФ обладает более выраженным стресспротективным действием.
3. Механизм действия пара-НПФ при действии экстремальных факторов заключается в оптимизации нейроэндокринной регуляции, усилении белкового синтеза, анаэробного окисления.
4. Пара-НПФ обладает более выраженным защитным противоокислительным действием, чем мета-НПФ.
Формула изобретения
1. Натриевая соль поли(парадигидрокси-парафенилен)тиосульфокислоты общей формулы
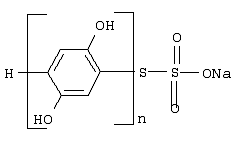
где n = 2 ÷ 6,
в качестве регулятора метаболизма клеток.
2. Натриевая соль поли(парадигидрокси-парафенилен)тиосульфокислоты по п. 1 в качестве антигипоксанта.
3. Фармацевтическая композиция, содержащая в качестве активного начала терапевтически или профилактически эффективное количество антигипоксанта, отличающаяся тем, что в качестве антигипоксанта используют натриевую соль поли(пара-дигидрокси-парафенилен)тиосульфокислоты, как она определена в п.1 или 2.
4. Фармацевтическая композиция по п. 3, отличающаяся тем, что дополнительно содержит фармацевтически приемлемый носитель, разбавитель, связующее вещество или инертный наполнитель.
РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 02.12.2005
Извещение опубликовано: 27.01.2007 БИ: 03/2007
NF4A Восстановление действия патента СССР или патента Российской Федерации на изобретение
Извещение опубликовано: 10.02.2007 БИ: 04/2007
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 02.12.2007
Извещение опубликовано: 27.07.2009 БИ: 21/2009
|
|