Патент на изобретение №2256642
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ВИНИЛХЛОРИДА
(57) Реферат:
Использование: химия хлорорганических соединений. Сущность: проводят газофазное термическое дегидрохлорирование (пиролиз) 1,2-дихлорэтана в присутствии промотора – хлористого водорода, который растворен в питающем сырье. Концентрация хлористого водорода находится в диапазоне 50-10000 ppm массовых. Технический результат: повышение конверсии сырья и снижение выхода побочных продуктов. 2 з.п. ф-лы, 1 табл.
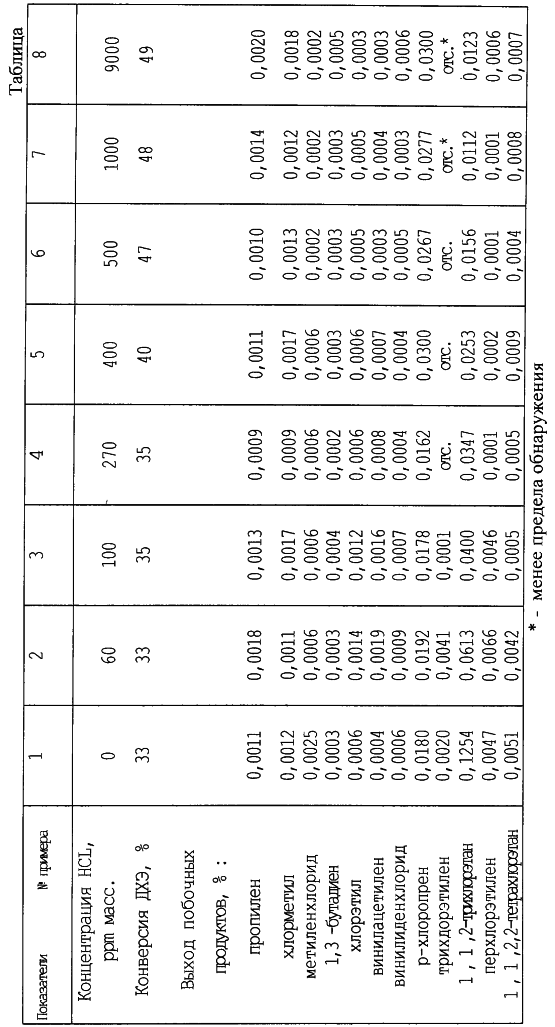
Винилхлорид (ВХ) является одним из важнейших мономеров. На его основе получают большое количество полимеров, имеющих широкий спектр различных свойств (механических, электрических, оптических и др.). В мировой промышленной практике ВХ получают в основном сбалансированным методом из этилена через стадию газофазного, термического дегидрохлорирования (пиролиза) 1,2-дихлорэтана (ДХЭ) (Bunten M.J. et. al. Encyclopedia of Polymer Science and Engineering. Volumes 17 and Supplement. – Jhon Wiley & Sons Inc.,1989, p.247 [1]). Этот метод имеет ряд недостатков, а именно: низкую конверсию ДХЭ за один проход, образование большого количества побочных продуктов, кокса и смол. Для улучшения технико-экономических показателей процесса пиролиза ДХЭ предлагается проводить его в присутствии различных веществ, которые называются промоторами или инициаторами. Их использование позволяет повысить конверсию ДХЭ, снизить образование кокса и некоторых побочных веществ. Известны способы пиролиза ДХЭ в присутствии молекулярного хлора (Авторское свидетельство СССР №218680, 1966; Патент Великобритании №1225210, 1969 [2, 3]), кислорода (Авторское свидетельство СССР №1066979 [4]), неорганических и органических производных галогенов (Патент США №4851597, 1989 [5]). Хлорированные и бромированные производные ацетона, в частности гексахлор- или гексабромацетон, инициируют пиролиз ДХЭ в массовом соотношении 0.01-0.00001:1 (Патент США №4584420, 1986). При этом выход ВХ возрастает вместе с увеличением количества вредных побочных продуктов – хлоропрена и ацетилена. Значительно повышается конверсия ДХЭ при пиролизе в присутствии 250-1000 ppm масс. бензотрихлорида (Патент США №5210345, 1993). Конверсия ДХЭ в отсутствии добавки составляла в условиях опытов 51.8%, а в присутствии ее в количестве 500 ppm составляла 81%. Отмечается, что концентрация хлораля (мг/100 граммов ДХЭ) при этом снижается от 0.4 до практически отсутствия. В обычной промышленной практике хлораль и хлоральгидрат стараются удалить из ДХЭ, поступающего на пиролиз (см., например, патенты США №№3488398, 3996300, 4151212, 4172099), из-за их коррозионной активности по отношению к материалам реактора. Однако авторы изобретения, описанного в международной заявке WO 96/35653, А1 (опубликована 14.11.96), считают, что, если материалы, из которых изготовлено оборудование, коррозионно устойчивы к хлоралю и хлоральгидрату, то их применение в пиролизе ДХЭ очень полезно. В присутствии 300 ppm хлораля выход ВХ в условиях эксперимента возрастает примерно на 10%. В промышленной печи наблюдался рост конверсии на 5-10% и снижение количества винилацетилена практически до нуля. Использование в пиролизе таких инициаторов, как тионилхлорид, сульфурилхлорид, нитрозилхлорид [5], приводит к необходимости разработки мероприятий для очистки потоков от соединений серы, оксидов азота. Органические инициаторы – гексахлорэтан, октахлорпропан, трихлорацетилхлорид, гексахлорацетон и др. должны быть специально синтезированы и очищены. Цель данного изобретения – улучшение процесса пиролиза ДХЭ, а именно повышение конверсии и снижение выхода побочных продуктов за счет применения дешевого, легко доступного инициатора. Поставленная цель достигается тем, что в способе инициированного пиролиза ДХЭ в качестве инициатора используется хлористый водород. Концентрация хлористого водорода варьируется в диапазоне 50-10000 ppm массовых. Пиролиз ДХЭ целесообразно проводить при температурах 350-650°С, при атмосферном или повышенном давлении до 40 бар (4 МПа) и времени пребывания 0.1-30 секунд. Заметный рост конверсии ДХЭ наблюдается уже в присутствии 100 ppm хлористого водорода. При пиролизе в присутствии 400 ppm конверсия возрастает на 7%, а в присутствии 500 ppm – на 14%. Дальнейшее увеличение концентрации хлористого водорода в исходном ДХЭ существенно не сказывается на росте конверсии (при концентрации 1000-9000 ppm хлористого водорода наблюдается рост конверсии на 16%). Более сильно от концентрации хлористого водорода зависит выход некоторых побочных продуктов пиролиза (см. таблицу). Сущность настоящего изобретения иллюстрируется примерами, приведенными ниже. Все эксперименты проводят в реакторе, представляющем собой кварцевую трубку, помещенную в рубашку с электрообогревом. К выходу реактора присоединен закалочный сосуд, заполненный стеклянными кольцами Рашига и орошаемый дистиллированной водой, подкрашенной индикатором (метилоранж). Затем по ходу потока находятся две ловушки, охлаждаемые до минус 70°С. В течение каждого опыта температуру в испарителе поддерживают в диапазоне 280-285°С, в реакторе, 480-485°С. Время пребывание ДХЭ в зоне реакции составляет 4-6 секунд. Хлористый водород предварительно растворяют в питающем ДХЭ. В экспериментах использовали ДХЭ с чистотой не менее 99.8%. За время опыта через пиролизную систему проходит 15-20 граммов ДХЭ. После установления стабильных условий время опытов составляло 1-2 часа. Органические продукты пиролиза анализируют методом ГЖХ. Количество хлористого водорода (исходного и продукта) определяют титрованием. Конверсию ДХЭ и выходы продуктов пиролиза рассчитывают как среднее арифметическое из данных 4-6 опытов. Пример 1. (Опыт без добавки хлористого водорода). ДХЭ поступает в испаритель, нагретый до 280-285°С, а затем в кварцевую трубку реактора с примерно постоянной скоростью. Температура в зоне реакции находится в диапазоне 480-485°С. Пирогаз на выходе охлаждается в закалочной колонке дистиллированной водой и основная часть не превращенного ДХЭ конденсируется внизу. Не сконденсировавшаяся часть потока поступает в охлаждаемые ловушки. На основе данных анализа продуктов пиролиза рассчитывают конверсию. Она составляет в указанных выше условиях 33%. Пример 2. В ДХЭ растворяют 60 ppm массовых хлористого водорода. Этот раствор подают в испаритель. Температуры в испарителе и реакторе составляют 280-285 и 480-485°С соответственно. Далее все операции выполняют как в примере 1. Конверсия ДХЭ составляет 33%. Выход 1,1,2-трихлорэтана уменьшается в 2 раза. Примеры 3-8. Пиролиз ДХЭ проводят в условиях, сопоставимых с примером 1, в присутствии 100, 270, 400, 500, 1000, 9000 ppm массовых хлористого водорода соответственно. Результаты приведены в таблице. Из приведенных примеров видно, что количество таких побочных продуктов, как трихлорэтилен, перхлорэтилен, 1,1,2-трихлорэтан, 1,1,2,2-тетрахлорэтан, сильно снижается, несмотря на то, что конверсия ДХЭ возрастает. Это можно объяснить тем, что при пиролизе ДХЭ на стадии зарождения цепного свободнорадикального процесса из хлористого водорода образуется дополнительный атом хлора, а хлорэтильный радикал, как источник дополнительных побочных реакций, исчезает. СН2Cl-СН2Сl СН2Сl-СН2+НСl Атомы хлора играют ключевую роль в развитии свободнорадикального цепного процесса. Таким образом, проведение процесса пиролиза ДХЭ в присутствии хлористого водорода позволяет повысить конверсию и уменьшить образование побочных продуктов. Использование хлористого водорода в качестве инициатора (промотора) очень удобно, поскольку он не является дефицитным продуктом, хорошо растворяется в ДХЭ (около 15000 ppm масс.) и сам в свою очередь является продуктом пиролиза.
Формула изобретения
1. Способ получения винилхлорида путем газофазного, термического дегидрохлорирования (пиролиза) 1,2-дихлорэтана, отличающийся тем, что процесс проводят в присутствии инициатора (промотора), в качестве которого выступает хлористый водород, концентрация которого составляет 50-10000 ppm массовых. 2. Способ по п.1, отличающийся тем, что пиролиз проходит при температурах 350-650°С и давлении от атмосферного до 40 бар (4Мпа). 3. Способ по п.1 или 2, отличающийся тем, что время пребывания реакционной смеси в зоне пиролиза составляет 0,1-30 с.
|
||||||||||||||||||||||||||

 СН2Сl-СН2+Сl
СН2Сl-СН2+Сl