|
(21), (22) Заявка: 2003120791/14, 07.07.2003
(24) Дата начала отсчета срока действия патента:
07.07.2003
(43) Дата публикации заявки: 10.01.2005
(45) Опубликовано: 10.07.2005
(56) Список документов, цитированных в отчете о
поиске:
РЕЧКИН М.Ю. “Изменения сосудистой реакции и репарации тканей конечностей после повторяющихся остеоперфораций”. Автореферат диссертации, Курган, 2000, 20-22. RU 2210326 C1, 20.08.2003. Лазеры в клинической медицине. Под ред. проф. С.Д.Плетнева, М., “Медицина”, 1996, с.8-35.
Адрес для переписки:
457100, Челябинская обл., г. Троицк, ул. Гагарина, 13, Уральская государственная академия ветеринарной медицины
|
(72) Автор(ы):
Молоканов В.А. (RU),
Привалов В.А. (RU),
Крочек И.В. (RU),
Циулина Е.П. (RU),
Лаппа А.В. (RU),
Стрижиков В.В. (RU),
Шумилин И.И. (RU)
(73) Патентообладатель(и):
Уральская государственная академия ветеринарной медицины (RU)
|
(54) СПОСОБ СТИМУЛЯЦИИ РЕПАРАТИВНОГО ОСТЕОГЕНЕЗА У ЖИВОТНЫХ И ЧЕЛОВЕКА
(57) Реферат:
Изобретение относится к медицине, а именно к ортопедии и травматологии. Осуществляют чрескожные остеоперфорации хирургическим лазером посредством моноволоконного кварцевого световода диаметром 0,4 мм с термостойким защитным покрытием в импульсно-периодическом режиме со средней мощностью 20-40 Вт. Остеоперфорации осуществляются в течение 3-10 с в очаге перелома не менее чем в пяти точках: первые две точки на расстоянии 1,0-1,5 см от зоны перелома в обоих костных отломках, вторые две точки на расстоянии 1,0-1,5 см от первых двух, пятая точка проходит через зону перелома. Формируются сквозные отверстия в зоне перелома кости в перпендикулярных к кости плоскостях. Способ позволяет обеспечить полное анатомо-функциональное восстановление поврежденной кости, предупредить развитие осложнений в виде остеомиелита, формирования ложных суставов. 2 табл., 9 ил.
Изобретение относится к области ветеринарии и медицины, а именно к ортопедии и травматологии, и может быть использовано для хирургического лечения переломов костей у людей и животных.
Известны способы стимуляции репаративного остеогенеза у животных и человека на фоне использования традиционных средств иммобилизации: шин, гипсовых повязок, интрамедуллярного, накостного и чрескостного остеосинтеза (1, 2, 3, 6). При этом для ускорения заживления переломов рекомендуют применять различные препараты.
Так, непосредственно в зону перелома рекомендуют вводить препарат коллапан в виде гранул, пластин и геля после репозиции отломков. Препарат представляет собой новый биокомпозиционный материал на основе особо чистого гидроксиапатита и коллагена, в его состав входят антибиотики – гентамицин и линкомицин.
Использование препарата коллапан ускоряет минерализацию костной мозоли травмированных животных после операции на 15% по сравнению с контролем (без коллапана), при этом реабилитация перелома трубчатых костей при интрамедуллярном остеосинтезе наступала на 13 дней раньше, чем без применения коллапана (4).
Кроме коллапана, рекомендуют для стимуляции заживления переломов костей препараты, содержащие жизненно важные макро- и микроэлементы в сбалансированных физиологически допустимых для организма животных формах (8).
Известен способ стимуляции репаративного остеогенеза с использованием подкожного введения цитотоксической остеогенной сыворотки на фоне применения интрамедуллярного и чрескостного остеосинтеза (5).
Разработан способ стимуляции репаративного остеогенеза за счет стимуляции биосинтетических процессов с использованием эритропоэтической сыворотки (экзогенного эритропоэтина), что ускоряет созревание костной ткани в регенерате (6).
В комплексном лечении переломов у животных и человека, их последствий и различных заболеваний опорно-двигательной системы широко используются и различные физические факторы: УФО, УВЧ, Са- и Р-электрофорез, индуктотермия, ультразвук, оксибаротерапия, оптические квантовые генераторы, а также постоянное магнитное поле (7, 9).
Однако известные способы не всегда эффективны, предусматривают обязательную стабильную фиксацию костных отломков, трудоемки, нередко возникают осложнения в виде остеомиелитов, формирования ложного сустава и другие осложнения, в результате чего у людей наступает инвалидность, а животные, как правило, выбраковываются.
Наиболее близок к заявляемому способ стимуляции репаративного остеогенеза с применением низкоинтенсивного лазерного излучения. При этом после проведения интрамедуллярного остеосинтеза наряду с общепринятыми в хирургии методами лечения в послеоперационный период проводится курс лазеротерапии с применением гелий-неонового лазерного излучения лазерным аппаратом ЛНГ – 111, длина волны – 632,8 нм, мощность излучения – 12 мВт, экспозиция – 5 минут (9).
Автор рекомендует следующую схему лазеротерапии: облучение отломков непосредственно после восстановления целостности кости; облучение мягких тканей после проведенной операции и наложения швов; облучение мягких тканей в области перелома в радиусе 4-8 см на второй день после операции; облучение места перелома с третьего по десятый день после операции. При применении данного метода стимуляции репаративного остеогенеза к 25-26 дню после операции появлялась костная мозоль, формирование костной мозоли без стимуляции гелий-неоновым лазером заканчивалось к 35-40 дню.
Однако данный способ применим при свежих переломах, когда возможно проведение репозиции костных отломков с помощью интрамедуллярного остеосинтеза, требует довольно сложной и очень травматичной операции и длительного послеоперационного лечения с использованием гелий-неонового лазера.
Целью изобретения является разработка способа стимуляции репаративного остеогенеза у животных и человека, обеспечивающего полное анатомо-функциональное восстановление поврежденной кости, предупреждение развития осложнений в виде остеомиелитов, формирования ложных суставов и, как следствие, ускорение заживления переломов костей.
Указанная цель достигается тем, что в заявляемом способе производят лазерную остеоперфорацию в течение 3-10 с в очаге перелома в пяти точках: первые две точки на расстоянии 1,0-1,5 см от зоны перелома в обоих костных отломках, вторые две точки на расстоянии 1,0-1,5 см от первых двух, пятая точка проходит через зону перелома.
Используется хирургический лазер, излучающий в ближнем инфракрасном диапазоне (0,8-1,1 мкм) в импульсно-периодическом режиме со средней мощностью 20-40 Вт. В частности, могут использоваться диодные и YAG:Nd лазеры. Доставка энергии осуществляется чрескожно посредством моноволоконного кварцевого световода диаметром 0,4-0,6 мм с термостойким защитным покрытием.
Остеоперфорацию осуществляют следующим образом. Световодом перфорируется кожа, мягкие ткани и кость, причем в кости формируются сквозные отверстия в зоне перелома кости в перпендикулярных к кости плоскостях. При наличии большого мышечного массива подход к кости осуществляется с помощью пункции мягких тканей иглой диаметром 1-2 мм, через которую вводят световод. Время остеоперфорации (3-10 с) зависит главным образом от породы, возраста и толщины кости у животных.
Способ позволяет обеспечить бактерицидное действие, нормализовать внутрикостное давление. Способствует восстановлению костной структуры и ускоряет заживление переломов костей.
Таким образом, в сравнении с прототипом выявлены следующие отличительные признаки:
1. Используется хирургический лазер, излучающий в ближнем инфракрасном диапазоне (0,8-1,1 мкм) в импульсно-периодическом режиме со средней мощностью 20-40 Вт. В частности, могут использоваться диодные и YAG:Nd лазеры.
2. Доставка энергии осуществляется чрескожно посредством моноволоконного кварцевого световода диаметром 0,4-0,6 мм с термостойким защитным покрытием.
3. Остеоперфорация осуществляется в течение 3-10 с в очаге перелома не менее чем в пяти точках: первые две точки на расстоянии 1,0-1,5 см от зоны перелома в обоих костных отломках, вторые две точки на расстоянии 1,0-1,5 см от первых двух, пятая точка проходит через зону перелома. Формируются сквозные отверстия в зоне перелома кости в перпендикулярных к кости плоскостях.
Патентные исследования не выявили способов хирургического лечения переломов костей с использованием лазеров высокоинтенсивного излучения, характеризующихся заявляемой совокупностью признаков, следовательно, можно предположить, что указанный способ соответствует критерию “новизна”.
Использование совокупности существенных признаков также не известно, что говорит о соответствии критерию “изобретательский уровень”.
Заявляемый способ может быть осуществлен в любых специализированных медицинских и ветеринарных учреждениях, следовательно, он соответствует критерию “промышленная применимость”.
Заявленный способ иллюстрируется описанием его использования и клиническими примерами.
Экспериментальные исследования проводили на 16 беспородных животных, подобранных по принципу аналогов (возраст, вес, упитанность).
Животные содержались в индивидуальных клетках в условиях вивария УГАВМ. Кормили собак 3 раза в день по нормам, установленным приказом МЗ СССР №1179 от 10 октября 1983 г. Вода в поилках – постоянно. Собаки для поддержания физиологических функций получают полноценное, сбалансированное по основным элементам кормление. Основу их рациона составляют корма растительного и животного происхождения. Типичный рацион кормления собак приведен в таблице 1 (г/сутки на 1 животное).
В условиях клиники хирургии под действием миорелаксантов с соблюдением правил асептики и антисептики у всех животных выполнялась чрездиафизарная остеотомия лучевой кости, после чего накладывалась бинтовая повязка. Иммобилизация осуществлялась за счет локтевой кости.
| Таблица 1. Рацион кормления животных по возрастным группам (в расчете на одно животное) |
| Наименование продукта |
молоко |
крупа |
картофель |
капуста |
морковь |
хлеб |
корм. дрожжи |
соль |
мясо 2 кат |
мука, мясокостная |
| |
|
ячневая |
овсянная |
|
|
|
|
|
|
|
|
| Взрослые собаки |
200 |
100 |
100 |
200 |
75 |
50 |
200 |
6 |
20 |
300 |
10 |
| Щенки |
300 |
60 |
80 |
100 |
40 |
25 |
100 |
4 |
10 |
170 |
6 |
На 7-й день после перелома животных разделили на 2 группы по 8 голов в каждой.
Первая группа – контрольная, заживление проходило в естественных условиях.
Вторая группа – экспериментальная, где для стимуляции репаративных процессов в костной ткани использовали инфракрасный диодный лазер в импульсно-периодическом режиме, развивающий мощность свыше 30 Вт.
Доставка энергии осуществлялась чрескожно контактным путем через моноволоконный кварцевый световод диаметром 0,4 мм. При этом формировались сквозные перфорационные отверстия в диафизе кости в зоне перелома в перпендикулярных к кости плоскостях.
В послеоперационный период у животных обеих групп проводили рентгенографию с интервалом 7 дней.
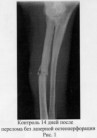
Через 14 дней после нанесения переломов у собак контрольной группы отмечался отек тканей в зоне перелома, что хорошо видно на рис.1, и начиналось формирование костной мозоли. Смещения костных отломков не наблюдалось. При движении животные частично пытались опираться на поврежденную конечность.
В опытной группе (рис.2) к 14 дню наблюдений, т.е. через 7 дней после лазерной остеоперфорации, отека мягких тканей не наблюдалось, отмечено также формирование костной мозоли. Собаки опытной группы к 14-му дню наблюдений осторожно опирались на поврежденную конечность. При этом следует отметить, что никакого дополнительного лечения (иммобилизация, применение антибиотиков) при проведении эксперимента в контрольной и опытной группах не проводилось.
В дальнейшем при анализе рентгенограмм можно отметить, что консолидация и репаративная регенерация костных фрагментов наступила значительно быстрее в экспериментальной группе и завершилась в среднем на 21-й день (рис.4). При этом следует отметить, что на фоне лазерной остеоперфорации к 21-му дню полностью сформировался кортикальный слой кости и животные при движении полностью опирались на поврежденную конечность. Клинически отмечалось полное выздоровление.
В контрольной группе на 21-й день наблюдений формирование костной мозоли еще не завершилось (рис.3) и при движении животные этой группы частично опирались на поврежденную конечность, наблюдалась хромота опирающейся конечности. У 2-х собак из 8 на месте перелома развился остеомиелит. Завершение формирования костной мозоли произошло только к 35-40 дню.
Отдаленные наблюдения показали, что на 60-й день после перелома в опытной группе у собак происходило полное анатомическое восстановление поврежденного участка лучевой кости (рис.6).
В контрольной группе, несмотря на видимое клиническое выздоровление к 60-му дню у 6-ти собак при рентгенографии установлено наличие большой периостальной костной мозоли (рис.5), что говорит о том, что восстановительные процессы еще не полностью завершились.
Динамика репаративных процессов по дням наблюдений приведена в таблице 2.
| Таблица 2. Динамика формирования костной мозоли при переломе лучевой кости у собак (n=8) |
| Группы животных |
Дни наблюдений |
Осложнения |
| |
14 |
21 |
60 |
|
| Контрольная |
Отек мягких тканей, начало формирования костной мозоли. Хромота опирающейся конечности. |
Продолжение формирования костной мозоли. Животные частично опираются на поврежденную конечность. |
Периостальная костная мозоль ярко выражена. Полного восстановления поврежденной кости не наступило. |
Остеомиелит у 2-х собак |
| Опытная |
Отсутствие отека мягких тканей, начало формирования костной мозоли. Животные частично опираются на поврежденную конечность. |
Окончание формирования костной мозоли. Полное восстановление функции поврежденной конечности. |
Полное восстановление поврежденной кости. |
нет |
В медицинской клинической практике данный метод применяется на кафедре общей хирургии Челябинской медицинской академии, находящейся на базе Челябинской городской клинической больницы №1 с 2000 года. Проведено лечение у 4 больных с замедленной консолидацией переломов крупных костей. При этом получены убедительные данные, доказывающие положительное влияние высокоинтенсивного лазерного излучения на скорость формирования костной мозоли.
Клинический пример
Больной М., 47 лет, поступил в травматологическое отделение Челябинской городской клинической больницы №1 22.11.2002 года после дорожно-транспортной травмы с клиникой открытого винтообразного перелома большеберцовой кости справа на границе средней и нижней трети со смещением. При поступлении произведено скелетное вытяжение за пяточную кость и первичная хирургическая обработка раны.
29.11.2002 года выполнена операция ЧКДО (чрескостного дистракционного остеосинтеза) по Илизарову. Фиксация в аппарате проводилась до 10.03.2003 года (свыше 3-х месяцев). При контрольном осмотре 11.03.2003 г. (рис.7) установлено, что имеется нагноение в области четырех спиц. Произведен демонтаж аппарата, отмечена патологическая подвижность в месте перелома на голени, на рентгенограммах – слабая костная мозоль. В этот же день произведены лазерные остеоперфорации места перелома, метаэпифизов большеберцовой кости и каналов проведения спиц. До 14.04.2003 года – иммобилизация конечности задней гипсовой лангетой. На контрольных рентгенограммах (рис.8 и 9) имеется прочная костная мозоль. Клинически отмечается улучшение; воспаление тканей купировано, патологической подвижности в месте перелома нет. Субъективно больной считает себя выздоравливающим. Ходит с полной нагрузкой на правую нижнюю конечность при помощи трости.
Таким образом, полученные результаты убедительно доказывают высокую эффективность применения высокоинтенсивного инфракрасного диодного лазера для стимуляции репаративных процессов в костной ткани при переломах костей.
Литература
1. Лукъяновский В.А., Белов А.Д., Беляков И.М. Болезни костной системы животных. – М. Колос: 1984, – 254 с. ил.
2. Чапкевич О.Б. Металлостеосинтез с применением накостных пластин. /Актуальные проблемы ветеринарной хирургии. Материалы международной научно-практической конференции, посвященной 70-летию каф. хирургии. – Воронеж. 1999. – с.107-109.
3. Ерофеев С.А., Петровская Н.В., Кононович Н.А. Технология лечения переломов костей голени у мелких домашних животных методом чрескостного остеосинтеза. Материалы 11 Московского международного конгресса. 17-19 апреля, 2003 г., Москва, Россия, с.153.
4. Башкатова Н.А. Рациональные способы лечения и стимуляции остеосинтеза у собак при переломах трубчатых костей. Автореф. дисс. на соиск. уч. степ. канд. вет. наук. Воронеж, 2000, 21 с.
5. Концевая С.Ю. Стимуляция остеогенеза при переломах костей у собак. Автореф. дисс. на соиск. уч. степ. канд. вет. наук. Троицк, 1999, 21 с.
7. Кочетков Ю.С. Биологические и хирургические аспекты стимуляции остеогенеза. (экспериментальное исследование). Автореф. дисс. на соиск. уч. степ. доктора мед. наук. Курган, 2002, 47 с.
8. Грищенко Н.В. Комбидаф-I – средство, ускоряющее регенерацию костей при переломах. Материалы международной научной конференции, посвященной 125-летию Казанской госакадемии ветеринарной медицины им. Н.Э.Баумана. – Казань, 1998. – Ч.2. – 20-21 (в соавт).
9. Грищенко Н.В. Влияние лазерного излучения и препарата комбидаф на регенерацию костной ткани при переломах трубчатых костей у собак. Автореф. дисс. на соиск. уч. степ. канд. вет. наук. Воронеж, 2000, 22 с.
Формула изобретения
Способ стимуляции репаративного остеогенеза, включающий применение лазера, отличающийся тем, что используется хирургический лазер, излучающий в ближнем инфракрасном диапазоне в импульсно-периодическом режиме со средней мощностью 20-40 Вт; доставка энергии осуществляется чрескожно посредством моноволоконного кварцевого световода диаметром 0,4 мм с термостойким защитным покрытием; остеоперфорация осуществляется в течение 3-10 с в очаге перелома не менее чем в пяти точках: первые две точки на расстоянии 1,0-1,5 см от зоны перелома в обоих костных отломках, вторые две точки на расстоянии 1,0-1,5 см от первых двух, пятая точка проходит через зону перелома; формируются сквозные отверстия в зоне перелома кости в перпендикулярных кости плоскостях.
РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 08.07.2005
Извещение опубликовано: 27.01.2007 БИ: 03/2007
|