|
|
(21), (22) Заявка: 2002118419/04, 08.07.2002
(24) Дата начала отсчета срока действия патента:
08.07.2002
(43) Дата публикации заявки: 20.01.2004
(45) Опубликовано: 10.06.2005
(56) Список документов, цитированных в отчете о
поиске:
US 6048847 А, 11.04.2000. SU 527442 A, 05.09.1975. Платонов В.Г. и др. Исследование противогриппозной активности терпеноидов. Химико-фармац. Журнал, 1995, №2, с.35-42.
Адрес для переписки:
199004, Санкт-Петербург, В.О., Большой пр., 31, патентная служба ИВС РАН, Г.М. Зарубинскому
|
(72) Автор(ы):
Назарова О.В. (RU),
Зорина А.Д. (RU),
Панарин Е.Ф. (RU),
Киселев О.И. (RU),
Боков С.Н. (RU),
Платонов В.Г. (RU),
Слита А.В. (RU),
Зарубаев В.В. (RU),
Афанасьева Е.В. (RU)
(73) Патентообладатель(и):
Институт высокомолекулярных соединений РАН (RU)
|
(54) ПОЛИМЕРНЫЕ ВОДОРАСТВОРИМЫЕ ПРОИЗВОДНЫЕ ТРИТЕРПЕНОИДОВ И СПОСОБ ИХ ПОЛУЧЕНИЯ
(57) Реферат:
Описаны полимерные производные тритерпеноидов общей формулы I
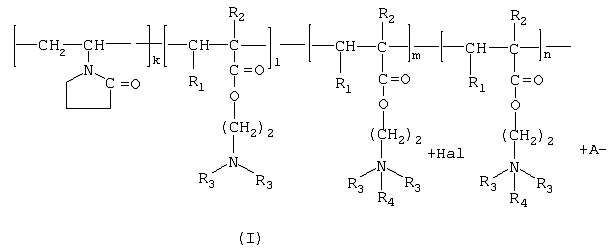
где в качестве полимера-носителя берут водорастворимые сополимеры N-винилпирролидона с алкиловыми эфирами  , , -(метил)акриловых кислот и их четвертичными аммониевыми солями общей формулы II -(метил)акриловых кислот и их четвертичными аммониевыми солями общей формулы II
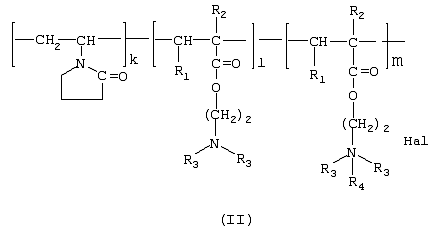
при этом А – остаток тритерпеноида из ряда, содержащего бетулиновую {1}, бетулоновую {2}, глицирретовую {3}, глицирризиновую {4}, урсоловую {5}, урсоновую {6}, олеаноловую {7}, олеаноновую {8}, меристотроповую {9}, дикетомеристотроповую {10}, мацедониковую {11}, дикетомацедониковую {12}, эхиноцистовую {13} кислоты, или смесь вышеуказанных карбоксилсодержащих тритерпеноидов; при этом – R1 – Н, СН3; R2 – Н, СН3; R3 – СН3, С2Н5; R4 – алкил из ряда С6Н13-С16Н33; Hal – J, Br или Cl; k=65-95 мол. %; l=0,1-34 мол.%, m=0,1-33,9 мол. %, n=0,5-5,4 мол.%; молекулярная масса (ММ)=(7-100)·103 дальтон. Способ получения полимерных производных тритерпеноидов заявленного строения реализуют взаимодействием тройного сополимера со структурой II, где k=65-95 мол.%; l=0,1-34 мол.%; х=1,0-34,9 мол.%; R1 – Н, СН3; R2 – Н, СН3; R3 – СН3, С2Н5; R4 – алкил из ряда С6Н13-С16Н33; Hal=J, Br, Cl; MM=(7-100)·103 дальтон с тритерпеноидом с получением целевого продукта. Взаимодействие с тритерпеноидом проводят в органическом растворителе при концентрации тройного сополимера 1-30 мас.%, концентрации тритерпеноида 0,05-3,4 мас. %; молярном отношении звена, содержащего четвертичный азот, к тритерпеноиду от 1 до 10; целевые полимерные водорастворимые производные тритерпеноидов выделяют удалением растворителя. 1 н.п. ф-лы, 2 табл., 6 ил.
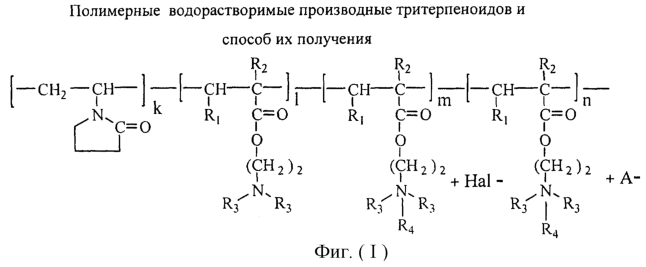
Изобретение относится к химии высокомолекулярных соединений, более точно к полимерным водорастворимым производным тритерпеноидов общей формулы I [фиг.I], где в качестве полимера-носителя берут водорастворимые сополимеры N-винилпирролидона с алкиловыми эфирами  , , -(метил)акриловых кислот и их четвертичными аммониевыми солями общей формулы II [фиг.II], при этом А – остаток тритерпеноида из ряда, содержащего бетулиновую {1}, бетулоновую {2}, глицирретовую {3}, глицирризиновую {4}, урсоловую {5}, урсоновую {6} [фиг.III], олеаноловую {7}, олеаноновую {8}, меристотроповую {9}, дикетомеристотроповую {10}, мацедониковую {11}, дикетомацедониковую {12}, эхиноцистовую {13} кислоты [фиг.III] или другой карбоксилсодержащий тритерпеноид или смесь карбоксилсодержащих тритерпеноидов; при этом – R1-Н, СН3; R2-Н, СН3; R3-СН3, С2Н5; R4 – алкил из ряда С6Н13-С16Н33; Hal-J, Br или Сl; k=65-95 мол.%; l=0,1-34 мол.%, m=0,1-33,9 мол.%, n=0,5-5,4 мол.%; молекулярная масса (ММ)=(7-100).103D. -(метил)акриловых кислот и их четвертичными аммониевыми солями общей формулы II [фиг.II], при этом А – остаток тритерпеноида из ряда, содержащего бетулиновую {1}, бетулоновую {2}, глицирретовую {3}, глицирризиновую {4}, урсоловую {5}, урсоновую {6} [фиг.III], олеаноловую {7}, олеаноновую {8}, меристотроповую {9}, дикетомеристотроповую {10}, мацедониковую {11}, дикетомацедониковую {12}, эхиноцистовую {13} кислоты [фиг.III] или другой карбоксилсодержащий тритерпеноид или смесь карбоксилсодержащих тритерпеноидов; при этом – R1-Н, СН3; R2-Н, СН3; R3-СН3, С2Н5; R4 – алкил из ряда С6Н13-С16Н33; Hal-J, Br или Сl; k=65-95 мол.%; l=0,1-34 мол.%, m=0,1-33,9 мол.%, n=0,5-5,4 мол.%; молекулярная масса (ММ)=(7-100).103D.
Изобретение относится также к способу получения полимерных водорастворимых производных тритерпеноидов указанного строения. Изобретение может найти широкое использование в качестве веществ с повышенной антивирусной активностью, которые в медицине и ветеринарии могли бы стать основой для создания лекарственных средств.
Многие широко используемые средства обладают антимикробным действием, но не активны в отношении вирусов.
Основными недостатками известных природных тритерпеноидов являются, во-первых, необходимость создания в организме большой концентрации дорогостоящего препарата, поскольку низкомолекулярные вещества быстро выводятся из организма, во-вторых, природные тритерпеноиды практически нерастворимы в воде, поэтому возникают сложности при их введении.
Задачей заявленного изобретения являлось придание тритерпеноидам водорастворимости при сохранении высокого уровня биологической активности и увеличение времени циркуляции при снижение концентрации вводимых в организм средств.
Эта задача решалась, во-первых, полимерными производными тритерпеноидов общей формулы [фиг.I], где в качестве полимера-носителя берут водорастворимые сополимеры N-винилпирролидона с аминоалкиловыми эфирами  , , -(метил)акриловых кислот и их четвертичными аммониевыми солями [фиг.II], при этом А – остаток тритерпеноида из ряда, содержащего бетулиновую {1}, бетулоновую {2), глицирретовую {3}, глицирризиновую {4}, урсоловую {5}, урсоновую {6} [фиг.III], олеаноловую {7}, олеаноновую {8}, меристотроповую {9}, дикетомеристотроповую {10}, мацедониковую {11}, дикетомацедониковую {12}, эхиноцистовую {13} кислоты [фиг.III], или другой карбоксилсодержащий тритерпеноид или смесь карбоксилсодержащих тритерпеноидов; при этом R1-Н, СН3; R2-Н, СН3; R3-СН3, С2Н5; R4 – алкил из ряда С6Н13-С16Н33; Hal-J, Br или Сl; k=65-95 мол.%; l=0,1-34 мол.%, m=0,1-33,9 мол.%, n=0,5-5,4 мол.%: молекулярная масса (ММ=(7-100).103 дальтон. -(метил)акриловых кислот и их четвертичными аммониевыми солями [фиг.II], при этом А – остаток тритерпеноида из ряда, содержащего бетулиновую {1}, бетулоновую {2), глицирретовую {3}, глицирризиновую {4}, урсоловую {5}, урсоновую {6} [фиг.III], олеаноловую {7}, олеаноновую {8}, меристотроповую {9}, дикетомеристотроповую {10}, мацедониковую {11}, дикетомацедониковую {12}, эхиноцистовую {13} кислоты [фиг.III], или другой карбоксилсодержащий тритерпеноид или смесь карбоксилсодержащих тритерпеноидов; при этом R1-Н, СН3; R2-Н, СН3; R3-СН3, С2Н5; R4 – алкил из ряда С6Н13-С16Н33; Hal-J, Br или Сl; k=65-95 мол.%; l=0,1-34 мол.%, m=0,1-33,9 мол.%, n=0,5-5,4 мол.%: молекулярная масса (ММ=(7-100).103 дальтон.
Во-вторых, задача решалась способом получения полимерных производных тритерпеноидов заявленного строения, который реализовался следующей совокупностью существенных признаков:
1. Проводят взаимодействие тройного сополимера со структурой II [фиг.II], где k=65-95 мол.%; l=0,1-34 мол.%; х=1,0-34,9 мол.%: R1-H, СН3; R2-H, СН3; R3-СН3, C2H5; R4 – алкил из ряда С6H13-С16Н33; Hal=J, Br, Cl; MM=(7100)103 D с тритерпеноидом с получением целевого продукта со структурой I [фиг.I], где А – остаток тритерпеноида из ряда, содержащего бетулиновую {1}, бетулоновую {2}, глицирретовую {3}, глицирризиновую {4}, урсоловую [5], урсоновую {6} [фиг.III], олеаноловую {7}, олеаноновую {8}, меристотроповую {9}, дикетомеристотроповую {10}, мацедониковую {11}, дикето-мацедониковую {12}, эхиноцистовую {13} кислоты [фиг.III] или другой карбоксилсодержащий тритерпеноид или смесь карбоксилсодержащих тритерпеноидов; при этом R1-Н, СН3; R2-Н, СН3; R3-СН3, С2Н5; R4 – алкил из ряда С6Н13-С16Н33; Hal-J, Br или Сl; k=65-95 мол.%; l=0,1-34 мол.%, m=0,1-33,9 мол.%, n=1-5,4 мол.%; молекулярная масса (ММ)=(7-100)·103 дальтон.
2. Взаимодействие с тритерпеноидом проводят в органическом растворителе при концентрации тройного сополимера 1-30 мас.%, концентрации тритерпеноида 0,05-3,4 мас.%; молярном отношении звена, содержащего четвертичный азот, к тритерпеноиду от 1 до 10.
3. Целевые полимерные водорастворимые производные тритерпеноидов выделяют удалением растворителя. Гомогенность полученных полимерных производных тритерпеноидов установлена методом гель-хроматографии. Состав полученных производных определен методом ПМР-спектроскопии по соотношению интенсивностей сигналов протонов при двойных связях в молекулах тритерпеноидов (в области 4,6-4,8 м.д.) и сигналов протонов в кольце N-винилпирролидона в  -положении к атому азота (в области 3,2 м.д.) [см. фиг.IV-VI]. -положении к атому азота (в области 3,2 м.д.) [см. фиг.IV-VI].
Водорастворимые сополимеры N-винилпирролидона с аминоалкиловыми эфирами  , ,
Полученные в соответствии с настоящим изобретением полимерные производные тритерпеноидов приобрели водорастворимость, при этом сохранили специфическую биологическую активность мономерных исходных тритерпеноидов можно ожидать, что их действие в организме будет характеризоваться значительной пролонгацией.
Анализ известного уровня науки и техники в отношении заявленных полимерных водорастворимых производных тритерпеноидов не позволил обнаружить известное решение, совпадающее с заявленным по всей совокупности существенных признаков. Более того, анализ известных публикаций как научных, так и патентных не позволил обнаружить каких-либо сведений о полимерных производных тритерпеноидов. Авторами настоящего изобретения у полученных полимерных тритерпеноидов заявленной структуры in vitro найдено неожиданное свойство – повышение удельной активности в расчете на действующее начало. Это подтверждено примерами конкретного выполнения. Таким образом, можно утверждать не только о соответствии заявленных полимерных водорастворимых производных тритерпеноидов такому условию патентоспособности, как новизна, но такому условию патентоспособности, как изобретательский уровень – неочевидность.
Анализ известного уровня науки и техники относительно способа получения полимерных водорастворимых производных тритерпеноидов также не позволил обнаружить какого-либо известного способа, совпадающего с заявленным по всей совокупности существенных признаков. Таким образом, заявленное решение в отношении независимого пункта формулы, относящегося к способу, соответствует такому условию патентоспособности, как новизна. Наиболее близким по совокупности существенных признаков решением является способ получения полимерных производных антибиотика леворина на основе сополимеров N-винилпирролидона с аминоакрилатами или аминами (10. Авторское свид. СССР №527442, МПК: 2 С 08 F 8/30; С 08 F 226/08; заявлено 18.06.1975; опубликовано 05.09.1976 ), который реализуется следующей совокупностью существенных признаков:
1. Сополимеры N-винилпирролидона с аммониевыми солями аминоалкиловых эфиров метакриловой кислоты, имеющих заместители у атома азота, предпочтительно C12-C16, растворяют в органическом растворителе.
2. К раствору добавляют суспензию леворина в том же растворителе и перемешивают при комнатной температуре.
3. Непрореагировавший леворин отделяют центрифугированием.
4. Из фильтрата удаляют растворитель.
Отличительным признаком заявленного способа является используемое для модификации биологически активное вещество. В известном способе – это антибиотик леворин. В заявленном – тритерпеноиды.
Неожиданным эффектом заявленного способа оказалось существенное увеличение удельной противовирусной активности полученных этим способом полимерных водорастворимых производных тритерпеноидов по сравнению с исходными низкомолекулярными тритерпеноидами. Этого не было найдено в известном способе. Впервые обнаруженная функция заявленного способа подтверждает соответствие решения такому условию патентоспособности, как “изобретательский уровень”.
Описание фигур.
Фигура I. Структура заявленного целевого продукта.
Фигура II. Структура полимера-носителя
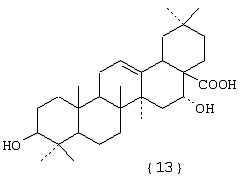
Фигура III. Структурные формулы тритерпеноидов: бетулиновая {1}, бетулоновая {2}, глицирретовая {3}, глицирризиновая {4}, урсоловая {5}, урсоновая {6} кислоты, олеаноловая {7}, олеаноновая {8}, меристотроповая {9}, дикетомеристотроповая {10}, мацедониковая {11}, дикетомацедониковая {12}, эхиноцистовая {13} кислоты.
Фигура IV. Спектр ПМР бетулиновой кислоты в CDCl3 на осях – х-химический сдвиг (м.д.); у – интенсивность сигнала.
Фигура V. Спектр ПМР исходного сополимера N- винилпирролидона с диметиламиноэтилметакрилатом и димегиллаурилмегакрилоилоксиэтиламмоний иодидом в CDCl3. на осях х-химический сдвиг (м.д.); у интенсивность сигнала.
Фигура VI. Спектр ПМР полимерного производного бетулиновой кислоты на основе сополимера N-винилпирролидона с диметиламиноэтилметакрилатом и диметиллаурилметакрилоилоксиэтиламмоний иодидом в CDCl3 нa осях х – химический сдвиг (м.д.); у – интенсивность сигнала.
Для подтверждения соответствия заявленного решения условию патентоспособности “промышленная применимость” и для лучшего понимания сущности изобретения приводим примеры конкретной реализации изобретения, которые не могут исчерпать сущности предложенного решения.
Пример 1. 3,5 г сополимера N-винилпирролидона (ВП) с диметиламиноэтилметакрилатом (ДМАЭМ) и диметиллаурилметакрилоилоксиэтиламмоний иодидом (ДМАЭМ·C12H25J) (состав тройного сополимера ВП:ДМАЭМ:ДМАЭМ·C12H25J=90,2:6,3:3,5 мол.%, М.М.=18000 Д) растворяют в 300 мл метанола и добавляют 0,44 г бетулиновой кислоты. Смесь перемешивают 1 час. Из фильтрата удаляют растворитель. Получают 3,8 г (выход=96%) полимера, содержащего по данным ПМР 3,5 мол.% бетулиновой кислоты (11,5 маc.%).
Примеры 2-15 выполнены в условиях примера 1, все данные представлены в Таблице 1. Использованы сокращения: ДЭАМА – диэтиламиноэтилмеиакрилат, ДМАЭА – диметиламиноэтилакрилат, ДЭАМК – диметиламиноэтилкротонат. Взаимодействие ведут при 15-30°С в течение 0,5-2 часов.
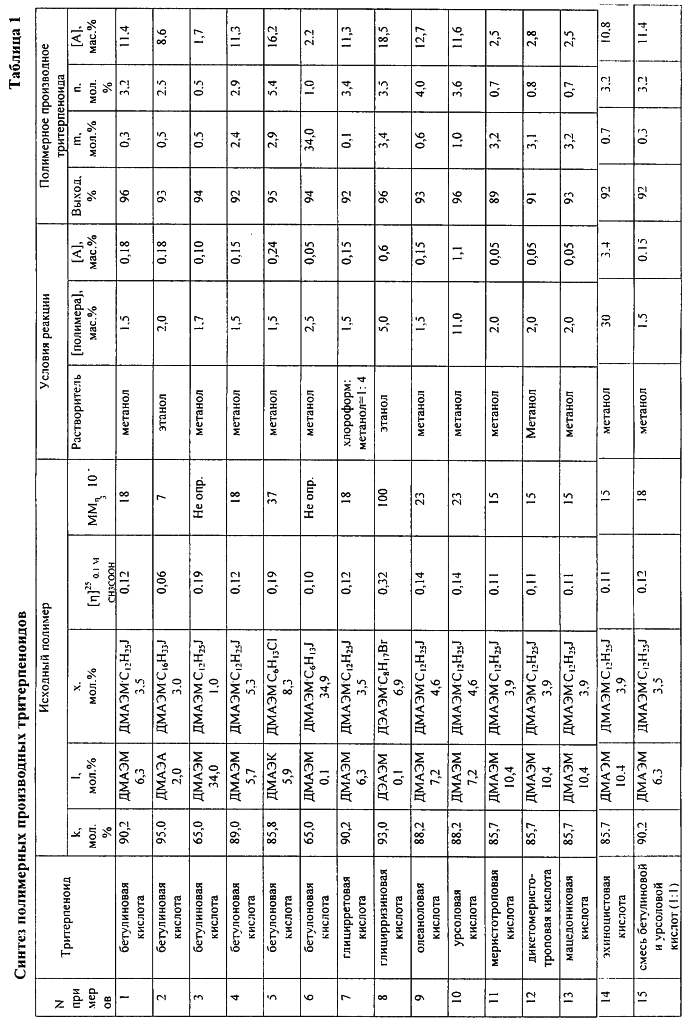
Противовирусную активность препаратов in vitro в отношении вирусов гриппа А и В (штаммы А/Йоханнесбург В/Йоханнесбург соответственно) исследовали на переживающих фрагментах хорионаллантоисной оболочки куриного эмбриона (ХАО) по методу Fasecas de St. Groth S. (11. Методы испытания и оценки противовирусной активности новых препаратов в отношении вируса гриппа. Ленинград. 1973. 36 с.). Для этого готовили ряд разведений испытуемого препарата на среде, которую разливали в лунки панелей, куда вносили подготовленные кусочки ХАО. Через 1 час контакта при комнатной температуре в эту же среду добавляли по 0,2 мл рабочего (ранее определенного) разведения вируса. Через 48 часов инкубации (при 33-34°С) отмечали количество живых и погибших кусочков. Лунки с погибшими ХАО из опытов исключают. В лунки с живыми кусочками ХАО добавляют 0,1 мл 5% эритроцитов курицы. Контролями при постановке опыта являлись обработанные таким же образом кусочки ХАО, но без добавления препарата. По результатам экспериментов рассчитывали индекс защиты (ИЗ): ИЗ=(КЗ-1)/КЗ×100, где КЗ – коэффициент защиты, определяемый как отношение процента образцов с вирусом в контроле к проценту образцов с вирусом в условиях введения препарата. При этом чем выше значение ИЗ, тем более активно исследуемое вещество. Противовирусную активность in vitro в отношении вируса простого герпеса (12. Вирусология. Методы. / под. Ред. Б. Мейха. М.: “Мир”. 1988. 420 с.) проводили в культуре клеток Vero при заражающей дозе вируса 100 ЦПД 50/мл. Вируссодержащую жидкость вносили в лунки после 30-минутной инкубации клеток с растворами исследуемых веществ. Результаты оценивали через 48 часов культивирования зараженных клеток. Данные по противовирусной активности приведены в Таблице 2. Анализ данных Таблицы 2 подтверждает, что достигнута заявленная задача как в отношении полученных новых полимерных водорастворимых производных, так и в отношении способа их получения.
| Таблица 2 |
| Противовирусная активность препаратов |
| № Примера |
Вещества |
Доза, мкг/мл |
Доза по тритерпеноиду, мкг/мл |
Индекс защиты, % |
| А/Йоханнесбург 33/94 |
В/Йоханнесбург 36/94 |
HSV |
| 16 |
бетулиновая кислота |
300
150
75 |
300
150
75 |
100
100
70 |
82
50
25 |
н.о.
72
10 |
| 17 |
бетулоновая кислота |
300
150
75 |
300
150
75 |
100
100
70 |
100
100
80 |
н.о.
н.о.
0 |
| 18 |
глицирретовая кислота |
300
150
75 |
300
150
75 |
90
75
50 |
15
0
0 |
н.о. н.о. н.о. |
| 19 |
поливинилпирролидон |
600
300 |
0
0 |
0
0 |
0
0 |
н.о. н.о. |
| 20 |
сополимер винилиирролидона с диметиаминоэтилметакрилатом (состав 90,2:9,8 моль %, мол. м.=18000) |
600
300
150 |
0
0 |
40
20
0 |
22
0
0 |
н.о. н.о. н.о. |
| 1 |
полимерное производное бетулиновой кислоты |
400
200
100 |
44
22
11 |
100
100
100 |
100
100
87 |
н.о.
100
45 |
| 4 |
полимерное производное бетулоновой кислоты |
300
150
75 |
33
17
8 |
100
100
33 |
100
100
37 |
н.о.
100 100 |
| 7 |
полимерное производное глицериновой кислоты |
600
300
150 |
66
33
17 |
100
74
37 |
100
100
0 |
н.о.
80
н.о. |
| Примечание: н.о. не определяли |
Формула изобретения
1. Полимерные производные тритерпеноидов общей формулы (I)
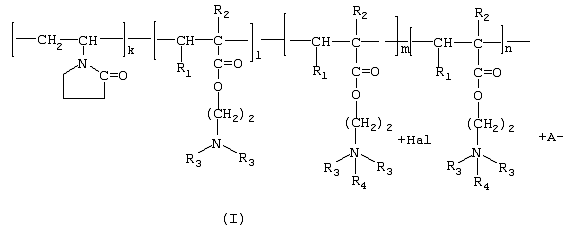
где в качестве полимера-носителя берут водорастворимые сополимеры N-винилпирролидона с алкиловыми эфирами  , , -(метил)акриловых кислот и их четвертичными аммониевыми солями общей формулы (II) -(метил)акриловых кислот и их четвертичными аммониевыми солями общей формулы (II)
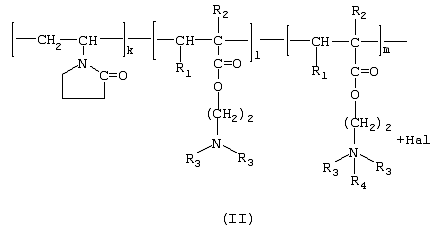
при этом А – остаток тритерпеноида из ряда, содержащего бетулиновую {1}, бетулоновую {2}, глицирретовую {3}, глицирризиновую {4}, урсоловую {5}, урсоновую {6}, олеаноловую {7}, олеаноновую {8}, меристотроповую {9}, дикетомеристотроповую {10}, мацедониковую {11), дикетомацедониковую {12}, эхиноцистовую {13} кислоты или смесь вышеуказанных карбоксилсодержащих тритерпеноидов
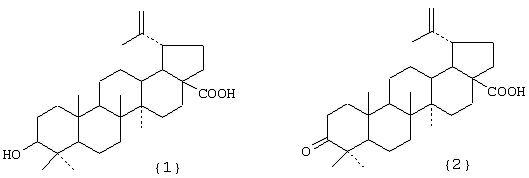
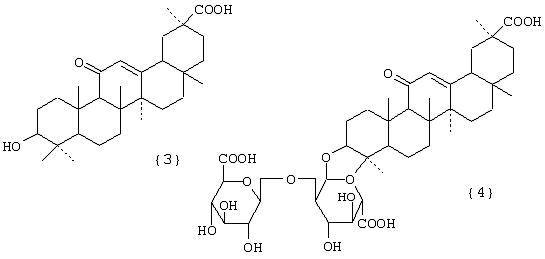
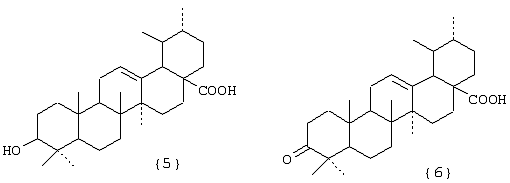
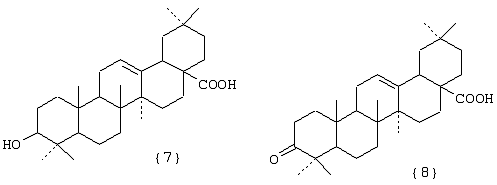
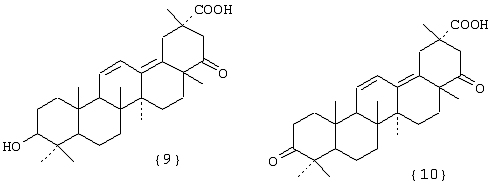
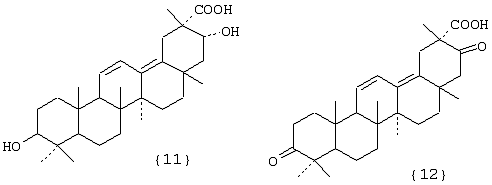
R1 – H, СН3; R2 – H, СН3; R3 – СН3, С2Н5;
R4 – алкил из ряда С6Н13-С16Н33; Hal – J, Br или Cl; k=65-95 мол.%; 1=0,1-34 мол.%, m=0,1-33,9 мол.%, n=0,5-5,4 мол.%; молекулярная масса (ММ)=(7-100)·103 дальтон.
2. Способ получения полимерных производных тритерпеноидов по п.1, включающий взаимодействие в органическом растворителе тройного сополимера формулы (II), где k=65-95 мол.%; l=0,1-34 мол.%; х=1,0-34,9 мол.%; R1 – Н, СН3; R2 – Н, СН3; R3 – СН3, С2Н5; R4 – алкил из ряда С6С13-С16Н33; Hal – J, Вr, Сl; ММ=(7-100)·103 Дальтон, с тритерпеноидом с получением целевого продукта формулы (I), где А – остаток тритерпеноида из ряда, содержащего бетулиновую {1}, бетулоновую {2}, глицирретовую {3}, глицирризиновую {4}, урсоловую {5}, урсоновую {6}, олеаноловую {7}, олеаноновую {8}, меристотроповую {9}, дикетомеристотроповую {10}, мацедониковую {11}, дикето-мацедониковую {12}, эхиноцистовую {13} кислоты или смесь вышеуказанных карбоксилсодержащих тритерпеноидов (III); R1 – Н, СН3; R2 – Н, СН3: R3 – СН3, С2Н5; R4 – алкил из ряда С6Н13-С16Н33; Hal – J, Вr или С1; k=65-95 мол.%; l=0,1-34 мол.%, m=0,1-33,9 мол.%, n – 1-5,4 мол.%; молекулярная масса (MM)=(7-100)·103 Дальтон, взаимодействие с тритерпеноидом проводят в растворе при концентрации тройного сополимера 1-30 мас.%, концентрации тритерпеноида 0,05-3,4 мас.%; молярном отношении звена, содержащего четвертичный азот, к тритерпеноиду от 1 до 10 при температуре 15-30°С в течение 0,5-2 ч; целевые полимерные водорастворимые производные тритерпеноидов выделяют удалением растворителя.
РИСУНКИ
|
|