Патент на изобретение №2253620
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ПЕНТАХЛОРИДОВ НИОБИЯ И/ИЛИ ТАНТАЛА (ВАРИАНТЫ)
(57) Реферат:
Изобретение относится к области получения пентахлоридов ниобия и/или тантала из их оксидов и/или оксихлоридов. Техническим результатом способа является экологическая безопасность самого реагента и продуктов реакции, полнота дохлорирования, низкая температура и высокая скорость процесса, снижение затрат на переделе. Способ получения пентахлорида ниобия и/или тантала включает взаимодействие оксидных или оксихлоридных соединений ниобия и/или тантала с хлорирующим агентом – двойным соединением хлорида алюминия с пентахлоридом фосфора формулы AlCl3 · PCl5. Процесс проводят при температуре 100-400° С. Для регенерации хлорирующего агента используют хлорирование отработанного агента в присутствии серы при 500-600° С или в присутствии углерода при 800-900° С. После хлорирования пентахлоридом фосфора формулы AlCl3 · PCl5 проводят хлорирование с использованием в качестве хлорирующего агента двойного соединения хлорида алюминия с хлорокисью фосфора формулы AlCl3 · POCl5. Другой вариант способа предусматривает использование в качестве хлорирующего агента расплавов на основе составов, близких к эвтектикам, образуемым двойными соединениями хлорида алюминия с пентахлоридом фосфора или с хлорокисью фосфора и хлоралюминатами и/или хлорферратами натрия и/или калия. Полученные пентахлориды ниобия и/или тантала выделяют из реакционной смеси ректификацией. 2 н. и 4 з.п. ф-лы.
Изобретение относится к области получения пентахлоридов ниобия и/или тантала из их оксидов и/или оксихлоридов. Одним из наиболее эффективных методов для разделения и глубокой очистки хлоридов ниобия и тантала является ректификация. Из всех хлоридов и оксихлоридов ниобия и тантала только пентахлориды обладают свойствами, позволяющими использовать ректификацию для их разделения и очистки. При хлорировании оксидных форм ниобий-танталсодержащего сырья, такого как колумбит, танталит, лопарит, ниобий и тантал, и часть сопутствующих примесей, например алюминий и железо, переходят в виде хлоридных возгонов в пылевые камеры. При этом ниобий в возгонах конденсируется преимущественно в виде его оксихлорида NbОСl3. Часть тантала в процессе сопутствует ниобию. Для перевода оксихлорида ниобия в пентахлорид ниобия проводят процесс хлорирования или, так называемого, дохлорирования возгонов, содержащих ниобий и/или тантал. Необходимость эффективного процесса перевода оксихлорида ниобия и оксида тантала (дохлорирование) вызвано несколькими причинами: – только пентахлориды ниобия и тантала кипят без разложения; – малая растворимость оксихлоридов в соответствующих хлоридах делает невозможным проведение ректификации; – продукты разложения оксихлоридов загрязняют ранее очищенные хлориды. Известен ряд дехлорирующих агентов: SOCl2, S2Cl2, C3Cl8, АlСl3, РСl5 и др. Однако они либо экономически неоправдан (SOCl2, C3Cl8), либо термически нестабильны в условиях дохлорирования (SOCl2, PCl5) или не технологичны из-за образования неплавких продуктов реакции (АlСl3). Существует способ перевода NbОСl3 в NbCl5 путем хлорирования оксихлорида в пульпе жидкого тетрахлорида титана хлоридом алюминия. Недостатком способа является его дороговизна и малая производительность: за 1 час в 1 м3 пульпы может прохлорироваться 10,4 кг NbOCl3 (см. Зеликман А.Н. и др. Ниобий и тантал. М., Металлургия, 1990, с.64). В настоящее время для дохлорирования продуктов первичного хлорирования ниобий-танталсодержащего сырья, так называемых возгонов, используют четыреххлористый углерод. Этот процесс хорошо изучен (см. Гаврилов О.Н., Семин М.О., Нисельсон Л.А. “О кинетике взаимодействия ниобий(-тантал)содержащих возгонов с четыреххлористым углеродом”, Научные труды института Гиредмет, т. xxv, M., Металлургия, 1969, с.71-76). Процесс дохлорирования возгонов четыреххлористым углеродом хорошо освоен в промышленности. Его проводят при температурах 300-380° С в многоподовых реакторах типа печей Гиресгофа (см. Зеликман А.Н. и др. Ниобий и тантал, M., Металлургия, 1990, с.63-64). Процесс описывается следующей реакцией: 2NbOCl3+CCl4 Недостатками этого метода являются: сложная конструкция реактора с необходимостью механического перемешивания продуктов дохлорирования, неполное извлечение в пентахлориды, что требует возвращения остатка на повторное хлорирование, образование фосгена, 2-3%об. которого попадает в отходящие газы и является токсичной и трудноудаляемой составляющей. Самое главное – это то, что используемый четыреххлористый углерод является веществом, разрушающим озоновый слой Земли, и его применение в промышленности ограничивается Международными соглашениями. Задачей изобретения является подбор нового реагента дохлорирования процесса получения пентахлоридов ниобия и/или тантала. Техническим результатом способа является экологическая безопасность самого реагента и продуктов реакции, полнота дохлорирования, низкая температура и высокая скорость процесса, снижение затрат на переделе. Для решения этой задачи в способе получения пентахлорида ниобия и/или тантала, включающем взаимодействие оксидных и/или оксихлоридных соединений ниобия и/или тантала с хлорирующим агентом, в качестве хлорирующего агента используют двойное соединение хлорида алюминия с пентахлоридом фосфора формулы АlСl3 · РСl5 и процесс проводят при температуре 100-400° С. Преимущественно полученные пентахлориды ниобия и/или тантала выделяют из реакционной смеси ректификацией. Кроме того, для регенерации хлорирующего агента используют хлорирование отработанного агента в присутствии серы при 500-600° С или углерода при 800-900° С. Для удешевления процесса за счет сокращения количества реагента дохлорирования после хлорирования пентахлоридом фосфора формулы АlСl3 · РСl5 проводят хлорирование с использованием в качестве хлорирующего агента двойного соединения хлорида алюминия с хлорокисью фосфора формулы АlСl3 · РОСl3. Преимущественно полученные пентахлориды ниобия и/или тантала выделяют из реакционной смеси ректификацией. Другим вариантом решения вышеуказанной задачи является то, что в способе получения пентахлорида ниобия и/или тантала, включающем взаимодействие оксидных и/или оксихлоридных соединений ниобия и/или тантала с хлорирующим агентом, в качестве хлорирующего агента используют расплавы на основе составов, близких к эвтектикам, образуемым двойными соединениями хлорида алюминия с пентахлоридом фосфора или с хлорокисью фосфора и хлоралюминатами и/или хлорферратами натрия и/или калия. Преимущественно полученные пентахлориды ниобия и/или тантала выделяют из реакционной смеси ректификацией. Сущность изобретения заключается в следующем. В качестве хлорирующего агента используют двойное соединение хлорида алюминия с пентахлоридом фосфора формулы АlСl3 · РСl5. По нашим исследованиям, это один из наиболее эффективных хлорирующих агентов. Реакция дохлорирования протекает с ним полностью, быстро и с большим выделением тепла. Степень дохлорирования исходных ниобий-танталсодержащих возгонов, которые могут содержать оксихлориды или непрохлорированные оксиды ниобия и/или тантала, составляет более 99%, что исключает необходимость возврата недохлорированных возгонов на повторное хлорирование, т.е. сокращает затраты на переделе. Предположительно реакция протекает по уравнению: При нагреве смеси хлоридных и/или оксихлоридных соединений ниобия и/или тантала с хлорирующим агентом AlCl3 · PCl5 интенсивная реакция с последующим саморазогреванием начинается при появлении первых признаков расплава. Реакция заканчивается в течение нескольких минут. При проведении процесса при температуре ниже 100° С проведение процесса невозможно, т.к. она ниже температуры плавления хлорирующего агента, а температура выше 400° С экономически неоправдана, т.к. не приводит к улучшению показателей процесса. Как сам хлорирующий агент, так и образующиеся в результате реакции соединения экологически безопасны. Для регенерации отработанного хлорирующего агента можно использовать его хлорирование хлором в присутствии серы или углерода. В первом случае процесс описывается реакцией: Реакция протекает в парах при 500-600° С в трубчатом реакторе с инертной насадкой. Снижение температуры ниже 500° С не позволяет получить пары соединений, а температура выше 600° С не приводит к улучшению процесса. Во втором случае процесс проходит при 800-900° С по реакции: В этом случае желательно использовать углерод в активной форме, например активированный уголь. Снижение температуры ниже 800° С не позволяет получить пары соединений, процесс протекает медленно и регенерация происходит не полно, а температура выше 900° С приводит к улетучиванию продуктов реакции. Кроме того, мы обнаружили, что образующееся в процессе реакции хлорирования исходных хлоридных и/или оксихлоридных соединений ниобия и/или тантала пентахлоридом фосфора формулы АlСl3 · РСl5 двойное соединение хлорида алюминия с хлорокисью фосфора формулы АlСl3 · РОСl3 также может быть использовано в качестве дехлорирующего агента. Системы АlСl3-РСl5 и АlСl3-РОСl3 хорошо изучены. В системе АlСl3-РСl5 имеется эвтектика с АlСl3, содержащая 43,7% мас. РСl5 и отрицательный азеотроп с температурой кипения 486° С и содержанием 54,3% маc. РСl5. Соединение АlСl3 · РСl5 имеет температуру плавления 345° С. В системе АlСl3-РОСl3 имеется эвтектика с АlСl3, содержащая 41,34% мас. РОСl3 и отрицательный азеотроп с температурой кипения 387° С и содержанием 51,35% маc. РОСl3. Соединение АlСl3 · РОСl3 имеет температуру плавления 120° С. Предположительно реакция протекает по уравнению: В случае использования для дохлорирования соединения АlСl3· РОСl3 образующиеся продукты реакции АlOСl· РОСl3 плохо растворимы в расплаве пентахлоридов ниобия и тантала. Это ограничивает их дехлорирующую способность на 20-25% и использование их в качестве самостоятельного агента хлорирования является нецелесообразным. Как сам хлорирующий агент, так и образующиеся в результате реакции соединения экологически безопасны. Полученные пентахлориды ниобия и тантала далее легко отделяются ректификацией от алюминий- и фосфорсодержащих соединений. Для дохлорирования могут быть также использованы расплавы на основе составов, близких к эвтектике в системах, образуемых двойными соединениями хлорида алюминия с пентахлоридом фосфора или с хлорокисью фосфора, т.е. AlCl3 · PCl5 и АlСl3 · РОСl3, и хлоралюминатами и/или хлорферратами натрия и/или калия: Na(K)AlCl4 или Na(K)FeCl4. Эти соединения и эвтектики с ними имеют еще более низкие температуры плавления, что упрощает процесс хлорирования. Таким образом, как двойные соединения хлорида алюминия с пентахлоридом фосфора или с хлорокисью фосфора, так и расплавы на основе составов, близких к эвтектике в системах, образуемых двойными соединениями хлорида алюминия с пентахлоридом фосфора или с хлорокисью фосфора и хлоралюминатами и/или хлорферратами натрия и/или калия, позволяют проводить процесс при низкой температуре. Полученные пентахлориды ниобия и тантала далее легко отделяются ректификацией от алюминий- и железосодержащих и фосфорсодержащих соединений. Изобретения иллюстрируются следующими примерами. Пример 1 В качестве исходного сырья были использованы промышленные “камерные возгоны”, содержащие, %мас.: NbOCl3+5%Nb2O5 – основа; Та – 3; (Na+K) – 0,07; Ca – 0.02, Ti – 0,05; Fe – 0,1; Al – 0,05; Si – 2, редкоземельные металлы – 0,1; Zr – 0,03; Th – 0,02. Процесс проводили в кубе из кварцевого стекла, объемом 1,6 л, снабженном воздухоохлаждаемым обратным холодильником в виде вертикальной трубки диаметром 30 мм и длиной 400 мм, В опыте было использовано 402 г возгонов, 332 г АlСl3 и 500 г РСl5. В начале процесса в куб засыпали весь АlСl3 и 250 г РСl5. Это позволяет создать расплав с температурой плавления 120-130° С. После взаимодействия компонентов расплава с образованием жидкой фазы при 150° С в расплав через воздухоохлаждаемый холодильник порциями подавали возгоны и оставшуюся часть PCl5. Дохлорирование протекало очень энергично с закипанием продуктов реакции за счет экзотермичности процесса. Весь процесс закончился за 25 мин. После замены обратного холодильника на ректификационную колонну с 5-ю реальными тарелками со щелевой перфорацией была проведена перегонка продуктов реакции. Получена основная фракция в виде смеси пентахлоридов ниобия и тантала в количестве 472 г, что соответствует 97% прямого извлечения ниобия из исходных возгонов. Ввиду малой эффективности ректификационной колонны и отбора продукта с небольшими флегмовыми числами при перегонке практически не происходило разделение пентахлоридов ниобия и тантала. В то же время химический анализ на содержание характерных примесей в полученных пентахлоридах основной фракции дал следующие, %мас.: Та – 3; Аl – 0,002; Р – 0,2; Ti – 0,1; Si – 0,002; Fe – 0,0002. Кроме основной, были отобраны головная фракция в количестве 6 г и промежуточная в количестве 170 г. Основная масса промежуточной фракции была отобрана при 375-385° С. По данным химического анализа головная фракция является практически чистым NbСl5 с примесью TaCl5. Промежуточная фракция представляет собой азеотроп АlСl3 · РОСl3 с примесью 3% NbCl5. Суммарное содержание пентахлоридов ниобия и тантала в головной и промежуточной фракциях составляет около 11 г. Эти фракции заворачивают на повторную ректификацию для разделения, увеличивая таким образом извлечение ниобия и тантала, считая от исходных возгонов, до их пентахлоридов до более 99%. Для регенерации отработанного хлорирующего агента АlСl3 · РОСl3 его разделили на две части. Одну часть хлорировали хлором в присутствии серы. Реакцию проводили в парах реагентов при 500-600° С в трубчатом реакторе с инертной насадкой. Другую часть хлорировали хлором в присутствии активированного угля при 800-900° С. В обоих случаях процесс образования АlСl3 · РСl5 из АlСl3 · РОСl3 происходит не менее чем на 90%. Пример 2 В опыте было использовано 403 г тех же возгонов, что и в примере 1, 265 г АlСl3 и 400 г РСl5. В начале процесса в куб засыпали весь АlСl3 и 200 г РСl5. Это позволяет создать расплав с температурой плавления 120-130° С. После взаимодействия компонентов расплава с образованием жидкой фазы при 150° С в расплав через воздухоохлаждаемый холодильник порциями подавали возгоны и оставшуюся часть РСl5. Затем температуру процесса увеличили до 275° С. В результате ректификации получена основная фракция в виде смеси пентахлоридов ниобия и тантала в количестве 356 г, что соответствует 98% прямого извлечения ниобия из исходных возгонов. Промежуточная фракция представляет собой АlOСl3 · РОСl3 с примесью NbCl5 (около 2%). Количество исходных реагентов дохлорирования АlСl3 и РСl5 сокращено на 20% по сравнению с примером 1. Пример 3 В качестве исходного продукта были использованы промышленные “венулетные возгоны”, содержащие, %мас.: основа – NbОСl3; Та – 6; (Na+K) – 0,3; Са – 0,02; Ti – 0,3; Fe – 0,2; Al – 0,02; Si – 0,05; редкоземельные металлы – 0,2; Zr – 0,1; Th – 0,06. Аппаратурное оформление и проведение процесса в этом опыте те же, что и в примере 1. Исключение составляет больший диаметр трубки воздухоохлаждаемого холодильника (40 мм) и существенно меньшее отношение количества дехлорирующего агента к количеству исходных возгонов. Было взято 580 г возгонов, 320 г АlСl3 и 485 г РСl5. Так же, как и в примере 1, процесс дохлорирования протекал очень энергично и завершился за 18 минут. После ректификации продуктов реакции получена основная фракция NbCl5+TaCl5 в количестве 654,7 г, что соответствует прямому извлечению ниобия и тантала в пентахлориды 97,5%. Содержание примесей в ней составило, %мас.: Ti – 0,02; Fe – 0,003; Al – 0,008; Si – 0,006; P – 0,02. Была отобрана промежуточная фракция в количестве 305 г. Содержание NbCl5 с примесью TaCl5 составило в ней 4,2%, что соответствует 12,8 г пентахлоридов. С их учетом общее извлечение ниобия и тантала в пентахлориды при дохлорированиии венулетных возгонов составило более 99,5%. Пример 4 В этом маломасштабном опыте было опробовано хлорирование пятиокиси ниобия. В кубе объемом 600 мл было синтезировано 29бг соединения АlCl3 Пример 5 В качестве исходного сырья были использованы промышленные “камерные возгоны”, содержащие, %мас.: NbOCl3 – основа; Та – 2,7; (Na+K) – 0,06; Са – 0,02; Ti – 0,06; Fe – 0,1; Al – 0,05; Si – 2; редкоземельные металлы – 0,1; Zr – 0,03; Th – 0,02. Процесс проводили в кубе из кварцевого стекла, снабженном воздухоохлаждаемым обратным холодильником. Все возгоны были разделены на четыре части для четырех опытов. В каждом опыте было использовано по 400 г возгонов. В первом опыте было использовано 552 г АlСl3, 470 г РСl5 и 63,2 г NaCl, во втором 552 г АlСl3, 470 г РСl3 и 87,7 г КСl, в третьем 320 г АlСl3, 470 г РСl5, 215 г FeCl5 и 63,2 г NaCl, в четвертом 320 г АlСl3, 470 г PCl5, 215 г FeCl3 и 87,7 г КСl. Все опыты проводили по одной схеме. В начале процесса в куб засыпали весь АlСl3, 250 г РСl3. Это позволяет создать расплав с температурой плавления 100-110° С. После взаимодействия компонентов расплава при 120° С в расплав подавали весь NaCl или КСl или весь NaCl или КСl и FеСl3. В результате реакции компонентов расплава образовывались расплавы, близкие по составу к эвтектикам, имеющимся между двойными соединениями хлорида алюминия с пентахлоридом фосфора или с хлорокисью фосфора и хлоралюминатами и/или хлорферратами натрия и/или калия. Затем порциями подавали возгоны и оставшийся РСl5. Процесс дохлорирования протекал очень энергично и закончился за 23 мин. После замены обратного холодильника на ректификационную колонну с 6-ю реальными тарелками была проведена перегонка продуктов реакции. Получена основная фракция в количестве 470 г, что соответствует 94% извлечению ниобия из исходных возгонов. Фракция содержит, % мас.: Та – 2,7; Аl – 0,01; Р – 0,2; Ti – 0,1; Si – 0,002; Fe – 0,005. Степень извлечения ниобия и/или тантала может быть увеличена до 99,7% при проведении повторных процессов ректификации. Таким образом, новые хлорирующие агенты позволяют не только проводить процесс с высоким выходом хлоридов, но и делают его простым и экономичным.
Формула изобретения
1. Способ получения пентахлорида ниобия и/или тантала, включающий взаимодействие оксидных или оксихлоридных соединений ниобия и/или тантала с хлорирующим агентом, отличающийся тем, что в качестве хлорирующего агента используют двойное соединение хлорида алюминия с пентахлоридом фосфора формулы АlСl3· РСl5 и процесс проводят при температуре 100-400° С. 2. Способ по п.1, отличающийся тем, что полученные пентахлориды ниобия и/или тантала выделяют из реакционной смеси ректификацией. 3. Способ по п.1 или 2, отличающийся тем, что для регенерации хлорирующего агента используют хлорирование отработанного агента в присутствии серы при 500-600° С или в присутствии углерода при 800-900° С. 4. Способ по п.1, отличающийся тем, что после хлорирования пентахлоридом фосфора формулы АlСl3· РСl5 проводят хлорирование с использованием в качестве хлорирующего агента двойного соединения хлорида алюминия с хлорокисью фосфора формулы АlСl3· РОСl3. 5. Способ получения пентахлорида ниобия и/или тантала, включающий взаимодействие оксидных или оксихлоридных соединений ниобия и/или тантала с хлорирующим агентом, отличающийся тем, что в качестве хлорирующего агента используют расплавы на основе составов, близких к эвтектикам, образуемым двойными соединениями хлорида алюминия с пентахлоридом фосфора, или с хлорокисью фосфора и хлоралюминатами, и/или хлорферратами натрия и/или калия. 6. Способ по п.5, отличающийся тем, что полученные пентахлориды ниобия и/или тантала выделяют из реакционной смеси ректификацией.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 19.05.2007
Извещение опубликовано: 27.07.2008 БИ: 21/2008
|
||||||||||||||||||||||||||

 2NbCl5+СO2.
2NbCl5+СO2.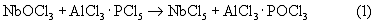
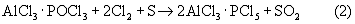
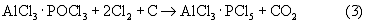
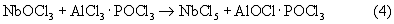
 РСl5 сплавлением АlСl3 и PCl5. К расплаву этого соединения при 340-350° С через трубку обратного холодильника засыпали 48 г Nb2О5. Реакция протекает с интенсивным разогревом и кипением продуктов. Внешний нагрев был выключен. Время на проведение хлорирования составило 8 мин. После замены обратного холодильника на ректификационную колонну диаметром 20 мм с 8-ю ситчатыми тарелками провели перегонку продуктов реакции. При температуре 245-247° С отобрана основная фракция в количестве 94,23 г. Следующая промежуточная фракция в количестве 51 г содержала 6,3% NbCl5. Таким образом, в этом опыте прямой выход NbCl5 при хлорировании Nb2О5 составил 96,55%, а с учетом его содержания в промежуточной фракции – 99,84%.
РСl5 сплавлением АlСl3 и PCl5. К расплаву этого соединения при 340-350° С через трубку обратного холодильника засыпали 48 г Nb2О5. Реакция протекает с интенсивным разогревом и кипением продуктов. Внешний нагрев был выключен. Время на проведение хлорирования составило 8 мин. После замены обратного холодильника на ректификационную колонну диаметром 20 мм с 8-ю ситчатыми тарелками провели перегонку продуктов реакции. При температуре 245-247° С отобрана основная фракция в количестве 94,23 г. Следующая промежуточная фракция в количестве 51 г содержала 6,3% NbCl5. Таким образом, в этом опыте прямой выход NbCl5 при хлорировании Nb2О5 составил 96,55%, а с учетом его содержания в промежуточной фракции – 99,84%.