|
|
(21), (22) Заявка: 2003125836/13, 21.08.2003
(24) Дата начала отсчета срока действия патента:
21.08.2003
(45) Опубликовано: 27.05.2005
(56) Список документов, цитированных в отчете о
поиске:
КРАТАСЮК В.А., ДМИТРИЕВА О.Н., БЕЛОБРОВ П.И. Свойства иммобилизованной в крахмальный гель люциферазы. Люминесцентный анализ в медико-биологических исследованиях. Рига: РМИ, 1986, с.93-97. ПЕТУШКОВ В.Н., ГУСЕЙНОВ О.А. Биолюминесцентный метод определения активности НАД-зависимой гидрогеназы. Прикладная биохимия и микробиология. – М.: Наука, 1992,
Адрес для переписки:
660041, г.Красноярск, пр. Свободный, 79, КрасГУ, отдел интеллектуальной собственности
|
(72) Автор(ы):
Кратасюк В.А. (RU),
Есимбекова Е.Н. (RU)
(73) Патентообладатель(и):
Красноярский государственный университет (RU),
Институт биофизики Сибирского отделения РАН (RU)
|
(54) СПОСОБ ПОЛУЧЕНИЯ ИММОБИЛИЗОВАННОГО МНОГОКОМПОНЕНТНОГО РЕАГЕНТА ДЛЯ БИОЛЮМИНЕСЦЕНТНОГО АНАЛИЗА
(57) Реферат:
Изобретение относится к биохимии, в частности к способам получения иммобилизованных ферментов, и может быть использовано в химии, биохимии, медицине, гистологии, микробиологии, экологии и сельском хозяйстве для анализа веществ биолюминесцентным методом. В способе получения иммобилизованного многокомпонентного реагента для биолюминесцентного анализа, заключающемся в приготовлении 3-5% геля кипячением суспензии крахмала в фосфатном буфере, охлаждении геля до 24-30°С, смешивании буферного раствора биферментной системы светящихся бактерий НАДН:ФМН-оксидоредуктаза-люцифераза с гелем крахмала, дозировании на лавсановую пленку и высушивании при 4-10°С, согласно изобретению компоненты биферментной реакции вводят в крахмальный гель в следующем порядке: миристиновый альдегид, никотинамидадениндинуклеотид, биферментная система НАДН:ФМН-оксидоредуктаза-люцифераза и флавинмононуклеотид. При этом растворы субстратов никотинамидадениндинуклеотида, флавинмононуклеотида и миристинового альдегида готовят на фосфатном буфере рН 6,8-7,0. Изобретение обеспечивает улучшение качества реагента для биолюминесцентного анализа путем уменьшения количества необходимых компонентов реакционной смеси (с четырех до одного), сокращение времени анализа в два раза и увеличение точности измерений при необходимости проведения длительных анализов. 1 з.п. ф-лы, 1 ил.
(56) (продолжение):
CLASS=”b560m”т.28, вып. 6, с.907-911. RU 2141108 С1, 10.11.1999. RU 2135586 С1, 27.08.1999. RU 2149182 С1, 20.05.2000.
Изобретение относится к биохимии, в частности к способам получения иммобилизованных ферментов, и может быть использовано в химии, биохимии, медицине, гистологии, микробиологии, экологии и сельском хозяйстве для анализа веществ биолюминесцентным методом.
Недостатком известного реагента и способа его приготовления является то, что получаемый реагент является малопригодным для аналитических исследований, поскольку для проведения анализа необходимо приготовление четырех растворов компонентов (3-х субстратов и буфера) с последующим их смешиванием в реакционную смесь, что существенно увеличивает время анализа и уменьшает точность измерений, в частности при проведении длительных анализов.
1. Приготовление 2-10% геля кипячением суспензии крахмала в фосфатном буфере.
2. Смешивание препарата НАДН:ФМН-оксидоредуктаза-люцифераза с гелем, охлажденным до 24-47°С.
3. Нанесение полученного препарата дозами по 50-100 мкл на лавсановую пленку.
4. Высушивание при температуре 4-8°С в течение 12 часов.
Недостатком известного реагента и способа его приготовления является отсутствие в иммобилизованном реагенте субстратов биферментной системы НАДН:ФМН-оксидоредуктаза-люцифераза, так что при проведении анализов необходимо приготовление четырех растворов компонентов биферментной реакции (субстратов и буфера) с последующим их добавлением к иммобилизованному препарату биферментной системы НАДН:ФМН-оксидоредуктаза-люцифераза, что существенно увеличивает время анализа и уменьшает точность измерений, в частности, при проведении длительных анализов.
Технический результат изобретения состоит в улучшении качества реагента для биолюминесцентного анализа путем уменьшения количества необходимых компонентов реакционной смеси (с четырех до одного), сокращения времени анализа в два раза и увеличения точности измерений при необходимости проведения длительных анализов.
Технический результат достигается тем, что в способе получения иммобилизованного многокомпонентного реагента для биолюминесцентного анализа, заключающемся в приготовлении 3-5% геля кипячением суспензии крахмала в фосфатном буфере, охлаждении геля до 24-30°С, смешивании буферного раствора биферментной системы светящихся бактерий НАДН:ФМН-оксидоредуктаза-люцифераза с гелем крахмала, дозировании на лавсановую пленку и высушивании при 4-10°С, согласно изобретению компоненты биферментной реакции вводят в крахмальный гель в следующем порядке: миристиновый альдегид, никотинамидадениндинуклеотид, биферментная система НАДН:ФМН-оксидоредуктаза-люцифераза и флавинмононуклеотид. При этом растворы субстратов никотинамидадениндинуклеотида, флавинмононуклеотида и миристинового альдегида готовят на фосфатном буфере рН 6,8-7,0.
Иммобилизованный многокомпонентный реагент для биолюминисцентного анализа готовят следующим образом (пример 1):
раствор биферментной системы НАДН:ФМН-оксидоредуктаза-люцифераза готовят на 0,05 М фосфатном буфере, рН 7,0. Растворы НАДН и ФМН готовят на дистиллированной воде или 0,05 М фосфатном буфере, рН 7,0. 0,002% раствор миристинового альдегида готовят из 0,2% спиртового раствора разбавлением в дистиллированной воде или 0,05 М фосфатном буфере, рН 7,0. Навеску 1,1 г крахмала помещают в 30 мл 0,05 М фосфатного буфера, рН 7,0, интенсивно перемешивают на мешалке, и кипятят полученную смесь до получения прозрачного 3,5% раствора. К 5 мл охлажденного до 28°С геля приливают 130 мкл 0,002% раствора миристинового альдегида, 130 мкл 1,6-10-2 М раствора НАДН, 130 мкл раствора биферментной системы НАДН:ФМН-оксидоредуктаза-люцифераза, содержащей 0,25 мг люциферазы и 0,7 единиц активности НАДН:ФМН-оксидоредуктазы, 130 мкл 1,3-10-3 М раствора ФМН, интенсивно перемешивают в течение 20 с. Наносят полученную смесь по 50 мкл на лавсановую пленку и высушивают при температуре 4°С в течение 12 часов. Многокомпонентный иммобилизованный реагент представляет собой диск диаметром 7-8 мм, толщиной 50-60 микрон, сухой вес 9±0,5 мг.
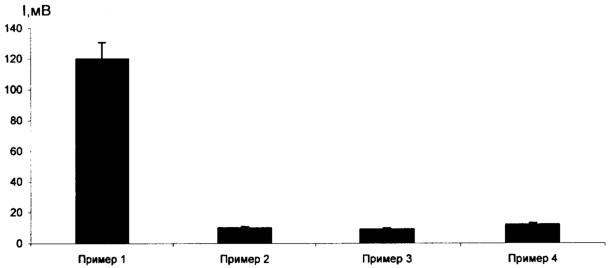
Активность иммобилизованного реагента определяют по максимальной интенсивности свечения в реакционной смеси, содержащей иммобилизованный реагент и 400 мкл фосфатного буфера, рН 7,0. Свечение регистрируют с помощью биолюминометра BLM 8801 (СКТБ “Наука” КНЦ СО РАН г. Красноярск), сигнал с которого подается на самописец (LKB, Швеция). Активность полученного реагента составляет 120 мВ.
Примеры 2-4 отличаются от заявляемого способа порядком добавления компонентов.
Пример 2
Иммобилизацию биферментной системы НАДН:ФМН-оксидоредуктаза-люцифераза и ее субстратов проводили аналогичным образом, добавляя компоненты в охлажденный до 28°С 3,5% гель в следующем порядке: 130 мкл раствора биферментной системы НАДН:ФМН-оксидоредуктаза-люцифераза, 130 мкл раствора миристинового альдегида, 130 мкл раствора НАДН, 130 мкл раствора ФМН. Концентрации всех компонентов соответствовали концентрациям в примере 1. Активность полученного реагента составляла 10 мВ.
Пример 3
Аналогичным образом проводили иммобилизацию биферментной системы НАДН:ФМН-оксидоредуктаза-люцифераза и ее субстратов, добавляя компоненты в охлажденный до 28°С 3,5% гель в следующем порядке: 130 мкл раствора биферментной системы НАДН:ФМН-оксидоредуктаза-люцифераза, 130 мкл раствора НАДН, 130 мкл раствора миристинового альдегида, 130 мкл раствора ФМН. Концентрации всех компонентов соответствовали концентрациям в примере 1. Активность полученного реагента составляла 9 мВ.
Пример 4
Аналогичным образом проводили иммобилизацию биферментной системы НАДН:ФМН-оксидоредуктаза-люцифераза и ее субстратов, добавляя компоненты в охлажденный до 28°С 3,5% гель в следующем порядке: 130 мкл раствора биферментной системы НАДН:ФМН-оксидоредуктаза-люцифераза, 130 мкл раствора ФМН, 130 мкл раствора НАДН, 130 мкл раствора миристинового альдегида. Концентрации всех компонентов соответствовали концентрациям в примере 1. Активность полученного реагента составляла 12 мВ.
Активность полученных в примерах 1-4 многокомпонентных иммобилизованных реагентов представлена на чертеже.
Использование описываемого реагента позволяет существенно сократить время проведения биолюминесцентного анализа. Обычный способ анализа веществ, описываемый в прототипе, требует разведения 4-х компонентов биферментной реакции с последующим введением каждого из них в реакционную смесь в процессе одиночного измерения. Процедура анализа с использованием описываемого реагента сводится к добавлению одного компонента – буфера (в качестве контрольного образца) или анализируемой смеси. Кроме того, при проведении стандартной процедуры анализа растворы субстратов биферментной реакции (миристинового альдегида и НАДН) быстро инактивируются, что приводит к уменьшению точности анализов. Описываемый реагент отличается стабильностью при хранении, что позволяет увеличить точность, в частности, при проведении длительных анализов.
Формула изобретения
1. Способ получения иммобилизованного многокомпонентного реагента для биолюминесцентного анализа, заключающийся в приготовлении 3-5% геля кипячением суспензии крахмала в фосфатном буфере, охлаждении геля до 24-30°С, смешивании буферного раствора биферментной системы светящихся бактерий НАДН:ФМН-оксидоредуктаза-люцифераза с гелем крахмала, дозировании на лавсановую пленку и высушивании при 4-10°С, отличающийся тем, что компоненты биферментной реакции вводят в крахмальный гель в следующем порядке: миристиновый альдегид, никотинамидадениндинуклеотид, биферментная система НАДН:ФМН-оксидоредуктаза-люцифераза и флавинмононуклеотид.
2. Способ получения по п.1, отличающийся тем, что растворы субстратов никотинамидадениндинуклеотида, флавинмононуклеотида и миристинового альдегида готовят на фосфатном буфере рН 6,8-7,0.
РИСУНКИ
PD4A – Изменение наименования обладателя патента Российской Федерации на изобретение
(73) Новое наименование патентообладателя:
Государственное образовательное учреждение высшего профессионального образования “Красноярский Государственный Университет” (RU)
(73) Новое наименование патентообладателя:
Институт биофизики Сибирского отделения РАН (RU)
Извещение опубликовано: 20.11.2006 БИ: 32/2006
QB4A Регистрация лицензионного договора на использование изобретения
Лицензиар(ы): Государственное образовательное учреждение высшего профессионального образования “Красноярский государственный университет”, Институт биофизики Сибирского отделения Российской академии наук
ИЛ
Лицензиат(ы): Общество с ограниченной ответственностью “Прикладные биосистемы”
Договор № РД0015063 зарегистрирован 07.12.2006
Извещение опубликовано: 20.01.2007 БИ: 02/2007
* ИЛ – исключительная лицензия НИЛ – неисключительная лицензия
|
|