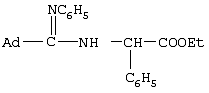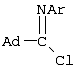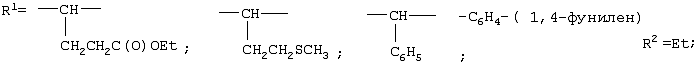Патент на изобретение №2250897
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ АДАМАНТИЛСОДЕРЖАЩИХ N-ИМИДОИЛИРОВАННЫХ ЭФИРОВ АМИНОКАРБОНОВЫХ КИСЛОТ
(57) Реферат:
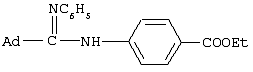
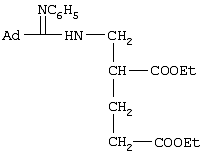
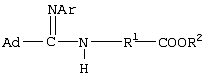
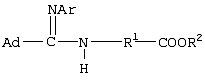
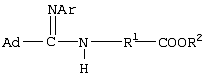
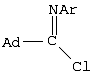
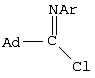
Изобретение относится к получению N-замещенных эфиров аминокарбоновых кислот, в частности к получению адамантилсодержащих N-имидоилированных эфиров аминокарбоновых кислот общей формулы: Способ осуществляют путем взаимодействия адамантилсодержащих имидоилхлоридов общей формулы: где Ad=1-адамантильная группа, Ar=С6Н5, с эфирами аминокарбоновых кислот общей формулы H2N-R1-COOR2 в среде органического растворителя, в присутствии акцептора хлористого водорода, в качестве которого используют триэтиламин. В качестве эфиров аминокарбоновых кислот используют гидрохлориды эфиров аминокарбоновых кислот. Технический результат – расширение арсенала химических соединений, получение новых адамантилсодержащих N-имидоилированных эфиров аминокарбоновых кислот. 2 з.п. ф-лы.
Изобретение относится к химии органических соединений, а именно к новому способу получения N-замещенных эфиров аминокарбоновых кислот, в частности адамантилсодержащих N-имидоилированных эфиров аминокарбоновых кислот, имеющих общую формулу: где Ad- 1-адамантильная группа, R2=Et-, Аr=С6Н5-. Получаемые соединения содержат у атома азота аминогруппы имидольную группу AdC(=NAr)- и являются новыми производными аминокарбоновых кислот и могут найти применение в качестве биологически активных соединений для нужд медицины и сельского хозяйства. Осуществление предлагаемого способа стало возможным благодаря использованию в качестве исходных реагентов эфиров аминокарбоновых кислот. Известен способ получения N-ацилированных эфиров аминокарбоновых кислот с использованием производного аминокарбоновой кислоты – эфира или гидрохлорида эфира аминокарбоновой кислоты (Дж. Гринштейн, М. Виниц. Химия аминокислот и пептидов. М.: Мир, 1965, 821 с.). Процесс проводят в среде органического растворителя в присутствии акцептора хлористого водорода. Выход продуктов 85-91%. Однако указанным способом получают N-ацилированные эфиры аминокарбоновых кислот, которые являются соединениями иной структуры, чем в предлагаемом изобретении. Известен способ получения адамантилсодержащих амидинов (Но Б.И., Шишкин Е.В., Сафиев P.P., Шишкин В.Е. Синтез N2 Недостатками данного способа являются необходимость использования большого избытка амина по отношению к исходным имидоилхлоридам, а также возможность протекания реакции гидролиза, что снижает выход целевого продукта. Данным способом получены соединения иной структуры, чем в предлагаемом способе. Известен способ получения амидинпроизводных, наиболее близких по структуре к предлагаемому изобретению (патент RU №2130014, С 07 С 257/14, А 61 К 31/155, опубл. 10.05.99 г.). Данные вещества предназначены для производства лекарственных средств для лечения состояний, при которых показано ингибирование продуцирования NO из L-аргинина под действием NO-синтетазы. Процесс проводят с использованием производных имидовых кислот – имидатов и тиоимидатов, в качестве производных аминокарбоновых кислот применяют соли аминокарбоновых кислот. Взаимодействие осуществляют в подходящем растворителе, например воде, в присутствии основания гидроксида натрия. Отличительной особенностью данного способа является использование в качестве исходных веществ имидатов и тиоимидатов – соединений иной структуры, чем в предлагаемом нами изобретении. Недостатком данного способа является многостадийность процесса, низкий выход – 68-72%. Задачей предлагаемого изобретения является создание нового технологичного способа получения адамантилсодержащих N-имидоилированных эфиров аминокарбоновых кислот. Техническим результатом предлагаемого изобретения является расширение арсенала химических соединений, получение новых N-имидоилированных эфиров аминокарбоновых кислот, включая эфиры многоосновных аминокарбоновых кислот, с выходом 85-95%, перспективных в качестве биологически активных соединений для нужд медицины и сельского хозяйства. Указанная задача достигается созданием нового способа получения адамантилсодержащих N-имидоилированых эфиров аминокарбоновых кислот, имеющих формулу: заключающегося во взаимодействии адамантилсодержащих имидоилхлоридов общей формулы: где Ad=1-адамантильная группа; Аr=С6Н5– с эфирами аминокарбоновых кислот общей формулы: R2=Et- в среде органического растворителя в присутствии акцептора хлористого водорода, в качестве которого используют триэтиламин. В качестве эфиров аминокарбоновых кислот используют гидрохлориды эфиров аминокарбоновых кислот. В качестве органических растворителей используют бензол, хлороформ, толуол или смесь растворителей хлороформ: бензол. Химическая схема предложенного способа получения адамантилсодержащих N-имидоилированных эфиров аминокарбоновых кислот: В известном способе получения адамантилсодержащих амидинов (Но Б.И., Шишкин Е.В., Сафиев P.P., Шишкин В.Е. Синтез N2 где Ad – 1-адамантильная группа; Ar=С6Н5-; 2-СН3С6Н4-; 3-СН3С6Н4-; 4-СН3С6Н4-; 4-NO2С6Н4-; 1-С10Н7. Таким образом, адамантилсодержащие имидоилхлориды с различными арильными заместителями в иминогруппе вступают в реакцию нуклеофильного замещения с аммиаком с образованием адамантилсодержащих амидинов. Предлагаемое изобретение иллюстрируется примерами с использованием одного адамантилсодержащего имидоилхлорида. Очевидно, что применение всех других перечисленных выше имидоилхлоридов, а не только приведенного в примерах N-фенилзамещенного имидоилхлорида также позволит получить адамантилсодержащие N-имидоилированные эфиры аминокарбоновых кислот. Ближайшими структурными аналогами имидовых кислот являются карбоновые кислоты. В известном способе получения N-ацилированных эфиров аминокарбоновых кислот в реакции с хлорангидридами карбоновых кислот (Дж. Гринштейн, М. Виниц. Химия аминокислот и пептидов. М., Мир. 1965. 821 с.) в качестве N-нуклеофильных реагентов применяют эфиры аминокарбоновых кислот с различными заместителями в эфирной группе (Me, Et, Pr, С6Н5СН2-). Предлагаемое изобретение иллюстрируется примерами с использованием в качестве эфиров аминокарбоновых кислот только этилового эфира. Очевидно, что применение других выше перечисленных эфиров аминокарбоновых кислот, а не только приведенного в примерах этилового эфира также позволит получить адамантилсодержащие N-имидоилированные эфиры аминокарбоновых кислот. В реакциях нуклеофильного замещения подобного типа необходимо связывание хлористого водорода, для чего применяют либо избыток второго реагента (N-нуклеофила), либо другого более сильного основания, чем является второй реагент. В предлагаемом способе применение избытка дорогостоящего второго реагента нецелесообразно, поэтому в качестве акцептора хлористого водорода применяли сильное основание, например триэтиламин. При выборе растворителя для проведения реакции нами были учтены следующие требования: создание гомогенной реакционной массы, возможность поддержания необходимого температурного режима и инертность к используемым реагентам. В случае реакции с эфирами аминокарбоновых кислот этим требованиям удовлетворяют углеводородные растворители, например бензол, толуол, в них растворяются все исходные компоненты и не растворяется образующийся в ходе реакции гидрохлорид триэтиламина, что дает возможность осуществлять визуальный контроль за ходом реакции и упростить стадию выделения целевого продукта. В случае реакции с гидрохлоридами эфиров аминокарбоновых кислот этим требованиям удовлетворяют как хлороформ, так и смешанный растворитель хлороформ:бензол, взятых в объемных соотношениях 1:1. Предложенный метод получения адамантилсодержащих N-имидоилированных эфиров аминокарбоновых кислот характеризуется простотой эксперимента, осуществляется в достаточно мягких условиях и обеспечивает высокий выход (85-95%) целевых соединений. Способ осуществляется следующим образом. Для синтеза N-имидоилированных эфиров аминокарбоновых кислот адамантилсодержащий имидоилхлорид растворяют в органическом растворителе, к раствору прибавляют триэтиламин, затем эфир аминокарбоновой кислоты или гидрохлорид эфира аминокарбоновой кислоты, мольное соотношение имидоилхлорид:триэтиламин:эфир аминокарбоновой кислоты = 1:1.05-1.15:1, мольное соотношение имидоилхлорид:триэтиламин:гидрохлорид эфира аминокарбоновой кислоты = 1:2.1-2.3:1. Процесс ведут при температурах 50-110°С в течение 1-3 ч. Для получения химически чистых веществ их очистку проводили методом перекристаллизации. Идентификацию полученных соединений осуществляли по данным элементного анализа, методами ИК-, масс -спектроскопии. Существо изобретения иллюстрируется, но не ограничивается следующими примерами конкретного выполнения: Пример 1. Этиловый эфир N-(N’-фенил-1-адамантанкарбоксимидоил)-метионина 3.7 г (13.6 ммоль) N-фенил-1-адамантанкарбоксимидоилхлорида растворяют в бензоле, к раствору прибавляют последовательно 1.6 г (14.2 ммоль) триэтиламина и 2.4 г (13.6 ммоль) этилового эфира метионина (мольное соотношение 1:1.05:1). Реакционную смесь выдерживают при температуре 80°С (кипения) 2 ч, горячим фильтрованием отделяют образовавшийся гидрохлорид триэтиламина. Из фильтрата отгоняют растворитель. Оставшееся масло кристаллизуется. Вещество очищают перекристаллизацией из гексана. Получили 5.1 г (92%) этилового эфира N-(N’-фенил-1-адамантанкарбоксимидоил)-метионина, Тпл 103-105°С. ИК-спектр Пример 2. Этиловый эфир N-(N’-фенил-1-адамантанкарбоксимидоил)-метионина 3.0 г (11.02 ммоль) N-фенил-1-адамантанкарбоксимидоилхлорида растворяют в смешанном растворителе бензол:хлороформ (1:1). К раствору прибавляют последовательно 2.33 г (23.03 ммоль) триэтиламина и 2.34 г (11.02 ммоль) гидрохлорида этилового эфира метионина (мольное соотношение (1:2.1:1)). Реакционную смесь выдерживают при температуре 50°С 1 ч. По окончании реакции отогнали растворитель и добавили бензол. Образовавшийся с количественным выходом гидрохлорид триэтиламина отделяли горячим фильтрованием из бензола. Дальнейшее выделение аналогично примеру 1. Получили 4.1 г (90%) этилового эфира N-(N’-фенил-1-адамантанкарбоксимидоил) метионина. Пример 3. Этиловый эфир N-(N’-фенил-1-адамантанкарбоксимидоил)-метионина 3.7 г (13.6 ммоль) N-фенил-1-адамантанкарбоксимидоилхлорида растворяют в хлороформе, к раствору прибавляют последовательно 1.6 г (14.2 ммоль) триэтиламина и 2.4 г (13.6 ммоль) этилового эфира метионина (мольное соотношение (1:1.05:1)). Реакционную смесь выдерживают при температуре 50°С 1 ч. По окончании реакции отогнали растворитель и добавили бензол. Образовавшийся с количественным выходом гидрохлорид триэтиламина отделяли горячим фильтрованием из бензола. Дальнейшее выделение аналогично примеру 1. Получили 4.9 г (88%) этилового эфира N-(N’-фенил-1-адамантанкарбоксимидоил)-метионина. Пример 4. Этиловый эфир N(N’-фенил-1-адамантанкарбоксимидоил)-4-аминобензойной кислоты 2.0 г (7.35 ммоль) N-фенил-1-адамантанкарбоксимидоилхлорида растворяют в бензоле, к раствору прибавляют последовательно 1.06 г (7.71 ммоль) триэтиламина и 1.2 г (7.35 ммоль) этилового эфира 4-аминобензойной кислоты (мольное соотношение (1:1.05:1)). Реакционную смесь выдерживают при температуре 80°С (кипения) 3 ч, горячим фильтрованием отделяют выпавший гидрохлорид триэтиламина. Из фильтрата отгоняют растворитель. Вещество очищают перекристаллизацией из бензола. Получили 2.7 г (94%) этилового эфира N-(N’-фенил-1-адамантанкарбоксимидоил)-4-аминобензойной кислоты, ТПЛ 131-133°С. ИК-спектр Пример 5. Этиловый эфир N-(N’-фенил-1-адамантанкарбоксимидоил)-4-аминобензойной кислоты 2.0 г (7.35 ммоль) N-фенил-1-адамантанкарбоксимидоилхлорида растворяют в толуоле, к раствору прибавляют последовательно 1.06 г (7.71 ммоль) триэтиламина и 1.2 г (7.35 ммоль) этилового эфира 4-аминобензойной кислоты (мольное соотношение (1:1.05:1)). Реакционную смесь выдерживают при температуре 110°С (кипения) 3 ч, горячим фильтрованием отделяют выпавший гидрохлорид триэтиламина. Из фильтрата отгоняют растворитель. Вещество очищают перекристаллизацией из бензола. Получили 2.5 г (89%) этилового эфира N-(N’-фенил-1-адамантанкарбоксимидоил)-4-аминобензойной кислоты. Пример 6. Этиловый эфир N-(N’-фенил-1-адамантанкарбоксимидоил)-фенилглицина 3.0 г (11.02 ммоль) N-фенил-1-адамантанкарбоксимидоилхлорида растворяют в бензоле, к раствору прибавляют последовательно 1.11 г (11.57 ммоль) триэтиламина и 1.97 г (11.02 ммоль) этилового эфира фенилглицина (мольное соотношение (1:1.05:1)). Реакционную смесь выдерживают при температуре 80°С (кипения) 1 ч, горячим фильтрованием отделяют образовавшийся гидрохлорид триэтиламина. Из фильтрата отгоняют растворитель. Вещество очищают перекристаллизацией из бензола. Получили 4.34 г (95%) этилового эфира N-(N’-фенил-1-адамантанкарбоксимидоил)-фенилглицина, Тпл 197-199°С. ИК-спектр Пример 7. Этиловый эфир N(N’-фенил-1-адамантанкарбоксимидоил)-фенилглицина 3.0 г (11.02 ммоль) N-фенил-1-адамантанкарбоксимидоилхлорида растворяют в бензоле, к раствору прибавляют последовательно 1.21 г (12.67 ммоль) триэтиламина и 1.97 г (11.02 ммоль) этилового эфира фенилглицина (мольное соотношение (1:1.15:1)). Реакционную смесь выдерживают при температуре 80°С (кипения) 1 ч, горячим фильтрованием отделяют образовавшийся гидрохлорид триэтиламина. Из фильтрата отгоняют растворитель. Вещество очищают перекристаллизацией из бензола. Получили 4.26 г (93%) этилового эфира N(N’-фенил-1-адамантанкарбоксимидоил)-фенилглицина. Пример 8. Диэтиловый эфир N-(N’-фенил-1-адамантанкарбоксимидоил)-глутаминовой кислоты 3.0 г (11.02 ммоль) N-фенил-1-адамантанкарбоксимидоилхлорида растворяют в бензоле, к раствору прибавляют последовательно 1.11 г (11.57 ммоль) триэтиламина и 2.3 г (11.02 ммоль) диэтилового эфира глутаминовой кислоты (мольное соотношение (1:1.05:1)). Реакционную смесь выдерживают при температуре 80°С (кипения) 1 ч, горячим фильтрованием отделяют образовавшийся гидрохлорид триэтиламина. Из фильтрата отгоняют растворитель. Вещество очищают перекристаллизацией из гексана. Получили 4.2 г (87%) диэтилового эфира N-(N’-фенил-1-адамантанкарбоксимидоил)-глутаминовой кислоты, Тпл 89-91°С. ИК-спектр Пример 9. Диэтиловый эфир N-(N’-фенил-1-адамантанкарбоксимидоил)-глутаминовой кислоты 2.85 г (10.46 ммоль) N-фенил-1-адамантанкарбоксимидоилхлорида растворяют в хлороформе, к раствору добавляют последовательно 3.2 г (10.98 ммоль) триэтиламина и 2.5 г (10.46 ммоль) гидрохлорида диэтилового эфира глутаминовой кислоты (мольное соотношение (1:2.3:1)). Реакционную смесь выдерживают при температуре 50°С 1 ч. Из фильтрата отгоняют растворитель. Вещество очищают перекристаллизацией из бензола. Выделение аналогично примеру 8. Получили 4.2 г (86%) этилового эфира N(N’-фенил-1-адамантанкарбоксимидоил)-глутаминовой кислоты. Пример 10. Диэтиловый эфир N-(N’-фенил-1-адамантанкарбоксимидоил)-глутаминовой кислоты 2.87 г (10.46 ммоль) N-фенил-1-адамантанкарбоксимидоилхлорида растворяют в смешанном растворителе бензол:хлороформ. К раствору последовательно добавляют 3.08 мл (2.21 г) триэтиламина и 2.5 г (10.46 ммоль) гидрохлорида диэтилового эфира глутаминовой кислоты (мольное соотношение (1:2.1:1)). Реакционную смесь выдерживают при температуре 50°С 1 ч, Из фильтрата отгоняют растворитель. Вещество очищают перекристаллизацией из бензола. Дальнейшее выделение аналогично примеру 8. Получили 4.2 г (91%) диэтилового эфира N-(N’-фенил-1-адамантанкарбоксимидоил)-глутаминовой кислоты. Предложенный метод позволяет осуществить синтез адамантилсодержащих N-имидоилированных эфиров аминокарбоновых кислот из соответствующих исходных соединений, что оказалось возможным благодаря использованию в качестве исходных реагентов эфиров аминокарбоновых кислот и гидрохлоридов эфиров аминокарбоновых кислот. Метод заключается во взаимодействии адамантилсодержащего имидоилхлорида с эфирами аминокислот или их гидрохлоридами в присутствии органического растворителя и акцептора хлористого водорода с образованием адамантилсодержащих N-имидоилированных эфиров аминокарбоновых кислот. Достоинством разработанного метода является простота технологии и универсальность.
Формула изобретения
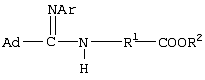
1. Способ получения адамантилсодержащих N-имидоилированных эфиров аминокарбоновых кислот общей формулы заключающийся во взаимодействии адамантилсодержащих имидоилхлоридов общей формулы где Аd=1-адамантильная группа; Аr=С6Н5– с эфирами аминокарбоновых кислот общей формулы H2N-R1-COOR2 в среде органического растворителя в присутствии акцептора хлористого водорода, в качестве которого используют триэтиламин. 2. Способ по п.1, отличающийся тем, что в качестве эфиров аминокарбоновых кислот используют гидрохлориды эфиров аминокарбоновых кислот. 3. Способ по п.1, отличающийся тем, что в качестве органических растворителей используют бензол, хлороформ, толуол или смесь растворителей хлороформ : бензол.
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 16.12.2005
Извещение опубликовано: 27.01.2007 БИ: 03/2007
|
||||||||||||||||||||||||||

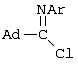
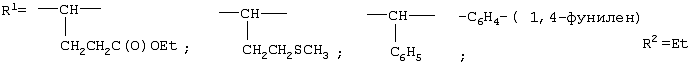
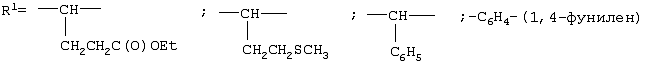
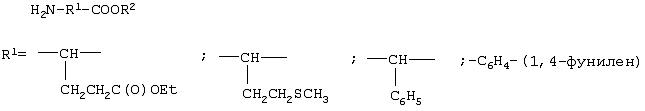
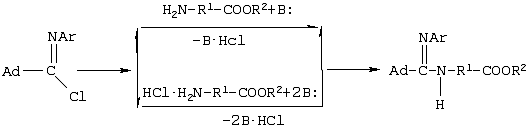
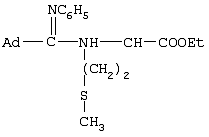
 , см-1: 740, 1100 (Ad), 1348 (C-N), 1184 (С-O), 1604 (Ar), 1636 (C=N), 1732 (С=O), 3368 (NH). Масс-спектр (1%, отн.): 369[М-OС2Н5]+(18); 308[М- OC2H5,- CH2SСН3]+(100); 293[M-OC2H5,-Ph]+(51); 218[М-Аd, -СН2SСН3]+(28); 135[Ag]+(97). Найдено, %: С 69.76; Н 8.50; N 6.49. С25Н36N2O2S. Вычислено, %: С 70.05; Н 8.47; N 6.54.
, см-1: 740, 1100 (Ad), 1348 (C-N), 1184 (С-O), 1604 (Ar), 1636 (C=N), 1732 (С=O), 3368 (NH). Масс-спектр (1%, отн.): 369[М-OС2Н5]+(18); 308[М- OC2H5,- CH2SСН3]+(100); 293[M-OC2H5,-Ph]+(51); 218[М-Аd, -СН2SСН3]+(28); 135[Ag]+(97). Найдено, %: С 69.76; Н 8.50; N 6.49. С25Н36N2O2S. Вычислено, %: С 70.05; Н 8.47; N 6.54.