Патент на изобретение №2153282
|
||||||||||||||||||||||||||
(54) СПОСОБ ДИНАМИЧЕСКОЙ ОЦЕНКИ ТЕЧЕНИЯ РЕСПИРАТОРНОГО ДИСТРЕСС-СИНДРОМА
(57) Реферат: Изобретение относится к медицине и может быть использовано в интенсивной терапии и реанимации, Определяют ежечасно отношение парциального давления кислорода в артериальной крови к фракции вдыхаемого кислорода, растяжимость легких, давление в легочной артерии. Рассчитывают скорость изменения отношения парциального давления кислорода в артериальной крови к фракции вдыхаемого, скорость изменения растяжимости легких и скорость изменения давления в легочной артерии по оригинальным математическим формулам. Эффективность лечения оценивают по полученным расчетным величинам при прогрессирующем или регрессирующем течении респираторного дистресс-синдрома (РДС). Способ позволяет оптимизировать лечение больных с РДС на основе применения количественной оценки динамики функционального состояния легких, оценки эффективности лечения и выявления клинико-динамических стадий течения РДС. 1 табл. Изобретение относится к области медицины и может быть использовано в интенсивной терапии и реанимации для количественной оценки динамики функционального состояния легких при респираторном дистресс-синдроме (РДС). Основной причиной летальности в отделениях интенсивной терапии и реанимации является полиорганная недостаточность (ПОН). Самым распространенным компонентом ПОН была и остается дыхательная недостаточность, как проявление РДС. Несмотря на успехи современной медицинской технологии, в особенности респираторной, средняя смертность при РДС не снижается ниже 60%. Это послужило причиной появления и внедрения в практику множества новых методик лечения РДС, воздействующих на разные звенья патогенеза. Все эти методики в клинических исследованиях обычно сравниваются с традиционным (общепринятым) способом лечения и редко сравниваются между собой. И даже в работах, сравнивающих новые методики, отсутствует легко сопоставимая – повременная количественная оценка динамики функций легких, как мера эффективности того или иного способа лечения РДС, а выводы традиционно делаются на простом сравнении основных показателей. Известно, что в течении РДС есть различия в зависимости от этиологического фактора и патогенетического варианта. Лечение больных с РДС – прерогатива отделений интенсивной терапии и реанимации. Важная часть интенсивной терапии – интенсивное наблюдение – постоянный мониторинг, поэтому все данные, характеризующие РДС, должны мониторироваться. Основными показателями, характеризующими развитие РДС, являются: соотношение парциального давления кислорода в артериальной крови к фракции вдыхаемого кислорода (PaO2/FiO2), растяжимость легких (C, комплайнс, мл/см вод.ст. ), давление в легочной артерии (ДЛА, мм рт.ст.), уровень необходимого при ИВЛ положительного давления конца выдоха (ПДКВ), данные рентгенографии. – способ подразделяет признаки РДС на 5 уровней (от 0 до 4) и не принимает в расчет промежуточные значения, т.е. обладает малой точностью; – не связан со временем и поэтому обладает малой чувствительностью к различным вариантам течения РДС, а также не позволяет оперативно сравнивать эффективность лечения; – данные рентгенографии, используемые в шкале, – это относительно субъективный признак который не может быть оценен количественно и не может часто мониторироваться; – ПДКВ также не может служить критерием РДС, так как в последние годы появились высококачественные респираторы, позволяющие обходиться малыми значениями ПДКВ при ИВЛ; – не позволяет дифференцировать кардиогенный или некардиогенный механизмы отеков легкого. – способ обладает низкой чувствительностью к промежуточным значениям исследуемых показателей; – не связан с временным фактором и первоначально не предназначался для мониторирования; – содержит малоинформативный при интенсивном мониторировании признак – рентгенографию. Задачей настоящего изобретения является оптимизация лечения больных с РДС на основе применения количественной оценки динамики функционального состояния легких, оценки эффективности лечения и выявления клинико-динамических стадий течения РДС. Задача решается тем, что фиксацию отношения парциального давления кислорода в артериальной крови к фракции вдыхаемого кислорода, растяжимости легких, давления в легочной артерии производят ежечасно, при этом рассчитывают скорость изменения отношения парциального давления кислорода в артериальной крови к фракции вдыхаемого кислорода (VPaO2/FiO2, скорость изменения растяжимости легких (Vcomp) и скорость изменения давления в легочной артерии (VДЛА) по формулам VPaO2/FiO2 = (РаO22 – PaO21)/t  FiO2, FiO2,если FiO2 не изменяется, VPaO2/FiO2 = (PaO22/FiO22 – PaO21/FiO21)/t, если FiO2 изменяется, где PaO21 -парциальное давление кислорода в артериальной крови в начале измерения, РаO22 – парциальное давление кислорода в артериальной крови в конце измерения, FiO21 – фракция вдыхаемого кислорода в начале измерения, FiO22 – фракция вдыхаемого кислорода в конце измерения, t – время за которое проводилось измерение. Vcomp = (C2 – C1)/t, где C1 – растяжимость легких в начале измерения, C2 -растяжимость легких в конце измерения. VДЛА = (ДЛА2 – ДЛА1)/t, где ДЛА1 – давление в легочной артерии в начале измерения, ДЛА2 – давление в легочной артерии в конце измерения, и при VPaO2/FiO2> > мм рт.ст./ч, Vcomp > 0,16 мл/см вод.ст./ч, VДЛА < – 0,05 мм рт. ст./ч эффективность лечения считают высокой при регрессирующем течении РДС, при VPaO2/FiO2 < 1 мм рт.ст./ч, Vcomp < 0,16 мл/см вод.ст./ч, VДЛА > – 0,05 мм рт.ст./ч эффективность лечения считается низкой при регрессирующем течении РДС, при VPaO2/FiO2 < 0 мм рт.ст./ч, Vcomp < 0 мм/см вод.ст./ч, VДЛА > 0 мм рт.ст./ч лечение считается не эффективным при прогрессирующем течении РДС. СПОСОБ ОСУЩЕСТВЛЯЕТСЯ СЛЕДУЮЩИМ ОБРАЗОМ. При проведении интенсивной терапии респираторного дистресс-синдрома производится ежечасная запись мониторных данных: парциального давления кислорода в артериальной крови (РаO2), фракции вдыхаемого кислорода (FiO2), их соотношения (PaO2/FiO2), растяжимости легких (C, комплайнс, мл/см. вод. ст. ), давления в легочной артерии (ДЛА, мм.рт.ст.). Затем изменения показателей (PaO2/FiO2; C, комплайнса, ДЛА) делятся на время, за которое эти изменения произошли. В результате получаем 3 показателя: скорость изменения оксигенации (VPaO2/FiO2), скорость изменения комплайнса (Vcomp), скорость изменения давления в легочной артерии (VДЛА): VPaO2/FiO2 = (РаO22 – PaO21)/t  FiO2, FiO2,если FiO2 не изменяется, VPaO2/FiO2 = (PaO22/FiO22 – PaO21/FiO21)/t, если FiO2 изменяется, где PaO21 – парциальное давление кислорода в артериальной крови в начале измерения, РаO22 – парциальное давление кислорода в артериальной крови в конце измерения, FiO21 – фракция вдыхаемого кислорода в начале измерения, FiO22 – фракция вдыхаемого кислорода в конце измерения, t – время за которое проводилось измерение. Vcomp = (C2 – C1)/t, где C1 – растяжимость легких в начале измерения, C2 – растяжимость легких в конце измерения. VДЛА = (ДЛА2 – ДЛА1)/t, где ДЛА1 – давление в легочной артерии в начале измерения, ДЛА2 – давление в легочной артерии в конце измерения. На основании полученных результатов оценивается динамика течения РДС. Для достоверной оценки необходимо наличие трех показателей (VPaO2/FiO2, Vcomp, VДЛА). Оценка динамики течения РДС. При VPaO2/FiO2 > 1 мм рт.ст./ч, Vcomp > 0,16 мл/см.вод.ст./ч, VДЛА < – 0,05 мм рт.ст. /ч эффективность лечения считают высокой при регрессирующем (на основании клинических проявлений) течении РДС. При VPaO2/FiO2 < 1 мм рт.ст. /ч, Vcomp < 0,16 мл/см вод.ст. /ч, VДЛА > – 0,05 мм рт.ст. /ч эффективность лечения считается низкой при регрессирующем течении РДС. При VPaO2/FiO2 < 0 мм рт.ст./ч, Vcomp < 0 мл/см вод.ст./ч. VДЛА > 0 мм рт.ст./ч лечение считается не эффективным при прогрессирующем течении РДС. Способ позволяет: 1) сравнивать эффективность различных методов лечения РДС, в том числе в малых группах больных и даже на одном больном, что способствует выбору оптимального лечения; 2) выявить 2 клинико-динамические стадии течения РДС: прогрессирования и регрессирования клинических проявлений; 3) прогнозировать течение РДС на основании эффективности лечения. ПРИМЕР 1 Больной П. , 39 лет, история болезни N 466, доставлен после аварии в шахте. Диагноз при поступлении: сочетанная травма, закрытая черепномозговая травма, ушиб головного мозга тяжелой степени, закрытый перелом левого бедра, закрытый перелом правого предплечья, ушиб левого легкого, травматический шок 2 ст. Состояние при поступлении тяжелое за счет травматического шока, острой дыхательной недостаточности, комы. Сознание – кома 1, дыхание самостоятельное, ЧД 30 в одну минуту. Гемодинамика: АД 90/40 мм рт.ст. , ЧСС 110 в минуту. Начато проведение комплексной противошоковой терапии, включающей инфузионную, антикоагулянтную, обезболивающую, седативную, антибактериальную и симптоматическую посиндромную терапии. Больной переведен на ИВЛ респиратором “Beer 33” через интубационную трубку. Выполнено наложение диагностических фрезевых отверстий в черепе, произведено скелетное вытяжение левого бедра. Через сутки состояние больного ухудшилось за счет прогрессирования РДС: рентгенографически “шоковое легкое”, PaO2/FiO2 = 172, комплайнс = 22 мл/см вод. ст., ДЛА = 20 мм рт.ст. Эти данные приняты за исходные. Начатое лечение продолжалось. На 2 сутки PaO2/FiO2 = 195, комплайнс = 25 мл/см вод.ст. , ДЛА = 19 мм рт.ст. Скорости изменений показателей за первые сутки: VPaO2/FiO2 = 0,97 мм рт. ст./ч, Vcomp = 0,15 мл/см вод.ст./ч , VДЛА = 0,04 мм рт.ст./ч. Течение РДС в первые сутки оценено как регрессирующее, эффективность лечения низкая. В дальнейшие 5 суток отмечалась аналогичная положительная динамика данных, сознание оценивалось как сопорозное. Через 7 суток с момента поступления больной был переведен на самостоятельное дыхание: PaO2/FiO2 = 309, комплайнс = 42 мл/см вод.ст. , ДЛА = 15 мм рт.ст. Скорости изменений показателей за 6 суток: VPaO2/FiO2 = 0,95 мм рт.ст./ч, Vcomp = 0,138 мл/см вод. ст. /ч , VДЛА = 0,035 мм рт.ст./ч. Лечение за 6 суток оценено как низкоэффективное, течение РДС – регрессирующее. На 9 сутки, при прояснении сознания, больной был экстубирован. Рентгенографически признаки “шокового легкого” исчезли. На 16 сутки – переведен в травматологическое отделение. Выздоровление. ПРИМЕР 2 Больной Б., 40 лет, история болезни N 859, доставлен в приемное отделение машиной скорой помощи после получения термотравмы на производстве. Диагноз при поступлении: термический ожог пламенем 3 степени головы, шеи, рото- и носоглотки, гортани, внутренний ожог легких. Состояние при поступлении тяжелое, обусловлено ожоговым шоком, дыхательной недостаточностью. Сознание сопорозное, дыхание самостоятельное, не эффективное, ЧД 38 в 1 мин, артериальное давление 90/50 мм рт.ст. Проводилась комплексная противошоковая терапия. Вентиляция осуществлялась респиратором “Beer 33” во вспомогательном режиме SIMV. Через сутки состояние больного ухудшилось за счет РДС: рентгенографически “шоковое легкое”, PaO2/FiO2 = 162, комплайнс = 19 мл/см вод.ст., ДЛА = 21 мм рт.ст. Эти данные приняты за исходные. Начато проведение кинетической терапии. Через сутки с начала проведения кинетической терапии PaO2/FiO2 = 205, комплайнс = 29 мл/см вод.ст., ДЛА = 18 мм рт. ст. Скорости изменений данных показателей за первые сутки: VPaO2/FiO2 = 1,8 мм.рт. ст./ч, Vcomp = 0,42 мл/см вод.ст./ч , VДЛА = 0,125 мм рт.ст./ч. Течение РДС в первые сутки оценено как регрессирующее, эффективность лечения высокая. В дальнейшие 3 суток отмечалась аналогичная положительная динимика данных. Через 4 суток с момента проведения кинетической терапии больной был переведен на самостоятельное дыхание: PaO2/FiO2 = 348, комплайнс = 48 мл/см вод.ст., ДЛА = 16 мм рт.ст. Скорости изменений показателей за 4 суток: VPaO2/FiO2 = 1,94 мм рт.ст./ч, Vcomp = 0,42 мл/см вод.ст. /ч, VДЛА = 0,05 мм рт.ст./ч. Лечение за 4 суток оценено как высокоэффективное, течение РДС – регрессирующее. На 6 сутки больной был экстубирован. Рентгенографически признаки “шокового легкого” исчезли. На 16 сутки – переведен в ожоговое отделение. Выздоровление. По заявляемому способу обследовано 32 больных обоего пола с РДС 2-3 степени после геморрагического, ожогового, травматического шоков, эндо- и экзотоксикозов, остановок кровообращения, черепно-мозговых травм (средний балл по шкале повреждения легких Мюррея 2,5 – 3,66). Возраст больных 16 – 69 лет. В зависимости от применяемого лечения РДС больные были разделены на 3 группы: леченные по общепринятой (традиционной) методике 12 человек (1 группа), 10 человек получали общепринятое лечение с кинетической терапией и седацией пропофолом (2 группа), 8 человек получали общепринятое лечение и кинетическую терапию (КТ) без седации пропофолом. Оценку показателей газообмена проводили путем определения парциального давления кислорода в капиллярной крови транскутанным методом с помощью отечественного прибора “чкРО2 – 01”, и анализатором КЩС. Оценку показателей центральной гемодинамики проводили только 6 больным в 1 и 3 группах по данным монитора MX-03 путем установки катетера Сван-Ганса в легочную артерию. Статистическую обработку полученных результатов осуществляли с помощью пакета прикладных программ “Адан”, разработанного на кафедре медицинской кибернетики и информатики Новокузнецкого ГИДУВа с использованием “t” критерия Стьюдента на IBM-AT 486. Первичные данные фиксировались с момента стабилизации гемодинамики больного, позволяющей проводить КТ, что в нашем исследовании соответствовало подбору адекватной респираторной терапии и полноценного восполнения ОЦК на фоне развившегося РДС (1 – 2 сутки течения РДС). В процессе лечения во всех трех группах у выживших больных наблюдались однонаправленные положительные изменения, но с разной интенсивностью (Таблица 1. Приложение 1). Увеличение PaO2/FiO2, комплайнса и уменьшение ДЛА коррелировали со скоростями изменения данных показателей и были наиболее выражены во 2 группе, где применялась КТ с седацией пропофолом (VPaO2/FiO2 = 1,83; Vcomp = 0,28; VДЛА во второй группе не измерялось). Динамика улучшения исследуемых показателей в 1 группе (традиционная терапия) была самой низкой (VPaO2/FiO2 = 1, Vcomp = 0,16, VДЛА = 0,052) Изменения в 3 группе (традиционная терапия + КТ) были значительно лучше, чем в 1 группе, но уступали 2 группе по скорости наступления (VPaO2/FiO2 = 1,64, Vcomp = 0,24, VДЛА = 0,083). Летальность составила: в 1 группе 58,3% (умерло 7 из 12), во 2 группе 40% (умерло 4 из 10), в 3 группе 50% (умерло 4 из 8), общая летальность 47%. Сравнивая скорости изменений данных за 5 суток со скоростями подобных изменений в течении 1-х, 2-х, 3-х, 4-х, 5-х суток отдельно мы обнаружили, что скорости за каждые отдельные сутки имели близкие общим (за 5 суток) значения. Но наибольшая корреляция между отдельными значениями скоростей за сутки и общими значениями наблюдалась в первые сутки (Таблица 1. Приложение 1). О высокой прогностической ценности способа говорят данные сравнения летальности с динамической оценкой течения РДС за первые-вторые сутки применения ИВЛ: у 12 умерших из 15 эффективность лечения РДС была низкой или лечение было неэффективно, а у 20 выживших из 17 эффективность лечения РДС была высокой. Показательным является время достижения PaO2/FiO2 = 300 в каждой из групп: в 1 группе время возрастания PaO2/FiO2 до 300 с исходного времени составило в среднем 104 ч, во второй – 60 ч, в третьей – 72 ч. Применение способа оценки эффективности РДС позволяет просто и наглядно оценить выраженность изменений функций легких в ходе лечения, причем как положительных, так и отрицательных, позволяет сравнить эффективность различных способов терапии, в том числе и на одном больном, позволяет прогнозировать исход течения РДС и выявляет клинико-динамические стадии течения РДС. Формула изобретения
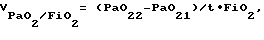 если FiO2 не изменяется, 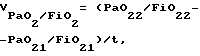 если FiO2 изменяется, где 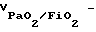 скорость изменения отношения парциального давления кислорода в артериальной крови к фракции вдыхаемого кислорода; скорость изменения отношения парциального давления кислорода в артериальной крови к фракции вдыхаемого кислорода;PaO21 – парциальное давление кислорода в артериальной крови в начале измерения; PaO22 – парциальное давление кислорода в артериальной крови в конце измерения; FiO21 – фракция вдыхаемого кислорода в начале измерения; FiO22 – фракция вдыхаемого кислорода в конце измерения; t – время, в течение которого проводилось измерение, скорость изменения растяжимости легких рассчитывают по формуле Vcomp = (C2 – C1)/t, где Vcomp – скорость изменения растяжимости легких; C1 – растяжимость легких в начале измерения, C2 – растяжимость легких в конце измерения, и скорость изменения давления в легочной артерии рассчитывают по формуле VДЛА = (ДЛА2 – ДЛА1)/t, где VДЛА – скорость изменения давления в легочной артерии; ДЛА1 – давление в легочной артерии в начале измерения; ДЛА2 – давление в легочной артерии в конце измерения, и при 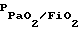 более 1 мм рт.ст./ч, Vcomp более 0,16 мл/см вод.ст./ч, VДЛА менее – 0,05 мм рт. ст./ч эффективность лечения считают высокой при регрессирующем течении респираторного дистресс-синдрома, при более 1 мм рт.ст./ч, Vcomp более 0,16 мл/см вод.ст./ч, VДЛА менее – 0,05 мм рт. ст./ч эффективность лечения считают высокой при регрессирующем течении респираторного дистресс-синдрома, при 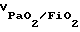 менее 1 мм рт.ст./ч, Vcomp менее 0,16 мл/см вод. ст./ч, VДЛА более – 0,05 мм рт. ст/ч эффективность лечения считается низкой при регрессирующем течении респираторного дистресс-синдрома, при менее 1 мм рт.ст./ч, Vcomp менее 0,16 мл/см вод. ст./ч, VДЛА более – 0,05 мм рт. ст/ч эффективность лечения считается низкой при регрессирующем течении респираторного дистресс-синдрома, при 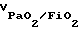 менее 0 мм рт.ст./ч, Vcomp менее 0 мл/см вод.ст./ч, VДЛА более 0 мм рт.ст./ч лечение считается неэффективным при прогрессирующем течении респираторного дистресс-синдрома. менее 0 мм рт.ст./ч, Vcomp менее 0 мл/см вод.ст./ч, VДЛА более 0 мм рт.ст./ч лечение считается неэффективным при прогрессирующем течении респираторного дистресс-синдрома.
РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 18.07.2001
Номер и год публикации бюллетеня: 12-2003
Извещение опубликовано: 27.04.2003
|
||||||||||||||||||||||||||
