|
(21), (22) Заявка: 2003125486/15, 18.08.2003
(24) Дата начала отсчета срока действия патента:
18.08.2003
(45) Опубликовано: 10.04.2005
(56) Список документов, цитированных в отчете о
поиске:
KOPRESKI M.S. et al., Somatic mutation screening: identification of individuals harboring K-ras mutations with the use of plasma DNA, J. of the Nat. Cancer Justitute, 2000, v.92, p.11. RU 2164419 C2, 27.03.2001. US 2002132227 A, 19.09.2002.
Адрес для переписки:
630060, г.Новосибирск, Экваторная, 11-12, П.П. Лактионову
|
(72) Автор(ы):
Лактионов П.П. (RU),
Скворцова Т.Э. (RU),
Тамкович С.Н. (RU),
Рыкова Е.Ю. (RU),
Власов В.В. (RU)
(73) Патентообладатель(и):
Лактионов Павел Петрович (RU),
Власов Валентин Викторович (RU)
|
(54) СПОСОБ РАННЕЙ ДИАГНОСТИКИ ЗАБОЛЕВАНИЙ, СВЯЗАННЫХ С НАРУШЕНИЕМ ФУНКЦИОНИРОВАНИЯ ГЕНЕТИЧЕСКОГО АППАРАТА КЛЕТКИ
(57) Реферат:
Изобретение относится к области диагностической медицины, а именно к разработке неинвазивных способов ранней диагностики различных заболеваний человека, в частности к выявлению ранних стадий рака, патологии беременности, а также мониторинга эффективности терапии. Сущность способа заключается в том, что после забора крови ее разделяют на плазму и фракцию клеток крови, затем фракцию клеток крови разделяют на эритроциты и лейкоциты, далее последовательно элюируют внеклеточные нуклеиновые кислоты, связанные с поверхностью эритроцитов и лейкоцитов, из полученных элюатов выделяют фракции внеклеточных нуклеиновых кислот и проводят амплификационный анализ не менее 2-х известных специфических последовательностей нуклеиновых кислот, ассоциированных с определенным заболеванием, с использованием соответствующего метода (полимеразная цепная реакция, лигазная цепная реакция, мультиплексная ПЦР и др.). Преимущество изобретения заключается в повышении точности диагностики. 5 з.п. ф-лы, 4 табл., 1 ил.

Изобретение относится к области диагностической медицины, а именно к разработке неинвазивных способов ранней диагностики различных заболеваний человека, в частности к выявлению предраковых состояний и ранних стадий рака, патологии беременности, а также мониторинга эффективности противораковой терапии.
Онкологические, аутоиммунные и наследственные болезни возникают вследствие нарушений функционирования генетического аппарата клетки. Способы, ориентированные на исследование нуклеиновых кислот (НК), таким образом, выявляют причину дисфункции и являются способами ранней диагностики, поскольку позволяют выявлять нарушения в функционировании генетического аппарата задолго до проявления клинических признаков заболевания.
Раннее выявление в крови специфических последовательностей нуклеиновых кислот, ассоциированных с различными заболеваниями, является важной проблемой в диагностической медицине. В то время как прямой анализ пораженных тканей бывает затруднен или недоступен (нет симптоматики), периферическая кровь является легкодоступным биологическим материалом для получения нуклеиновых кислот, которые могут быть использованы в амплификационном анализе.
Известен способ диагностики рака предстательной железы путем выявления мутантных генов раковых клеток методами ПЦР-анализа (1). Известно, что на поздних стадиях рака метастатические клетки циркулируют в крови, поэтому для анализа используют клеточную фракцию крови, из которой выделяют РНК одним из известных способов, а затем проводят мультиплексную ОТ-ПЦР. При раке предстательной железы у 84% пациентов (43/51) со злокачественной опухолью были выявлены значительные количества (3800 копий/0.5 мл крови) PSA и hK2 мРНК, тогда как лишь у одного из 19 пациентов (5%) с доброкачественной опухолью было обнаружено присутствие фрагментов PSA и hK2 мРНК в количестве 1500 и 3100 копий/0,5 мл крови. Главным недостатком этого способа является то, что требуется обязательное наличие метастатических, циркулирующих в крови больного раковых клеток (для негематологических опухолей), что ограничивает использование амплификационного анализа для больных в предраковом состоянии и с раком на начальной стадии.
Известно, что в плазме крови циркулируют нуклеиновые кислоты (2), количества которых в 10-100 раз выше у раковых больных (3, 4). При этом количество внеклеточных нуклеиновых кислот (ВНК) в плазме крови коррелирует со стадией развития рака и размером опухоли (5). На ранних стадиях возникновения рака количества ВНК в плазме относительно нормы практически не увеличиваются. Циркулирующие ВНК крови, выделенные из плазмы крови, используют для уточнения диагноза при онкологических, аутоиммунных и наследственных заболеваниях (6).
Известен способ диагностики онкозаболеваний путем выявления мутантных онкогенов ras в плазме периферической крови с помощью аллельспецифичной ПЦР с последующим секвенированием полученных фрагментов ДНК (7). Недостатками этого способа являются большая трудоемкость и длительность выделения ДНК, а также низкая достоверность результатов диагностики раковых и особенно предраковых состояний из-за небольшого удельного содержания специфических последовательностей НК, что затрудняет клиническое использование данного способа.
Известен способ диагностики преэклампсии путем оценки количества ВНК, циркулирующих в плазме беременных женщин, методами амплификации (8). Для анализа используют ДНК плазмы, выделенную любым известным способом, а затем проводят количественный ПЦР анализ. Недостатком данного способа является низкая достоверность результатов диагностики ранней патологии беременности.
Наиболее близким к заявленному способу – прототипом – является способ диагностики онкозаболеваний путем выявления онкоспецифических маркеров в плазме или сыворотке крови амплификационными методами (9), включающий следующие стадии: разделение крови на форменные элементы и плазму, выделение внеклеточной циркулирующей ДНК из плазмы сорбцией на мелкодисперсном стекле (ММС), выявление мутантной ДНК методами амплификационного анализа (полимеразная цепная реакция, лигазная цепная реакция, мультиплексная ПЦР и другие), с последующим анализом продуктов реакции и проведением, в случае необходимости, рестрикционного анализа.
Недостатком прототипа является низкая достоверность результатов диагностики ранних стадий онкозаболеваний, так как основная доля циркулирующих ВНК крови ассоциирована с клеточной поверхностью форменных элементов крови, что снижает удельное содержание специфических последовательностей НК в плазме и приводит к получению ложноотрицательных результатов.
Технической задачей изобретения является повышение достоверности ранней диагностики заболеваний, связанных с нарушением функционирования генетического аппарата клетки.
Поставленная техническая задача достигается предлагаемым способом, который заключается в следующем.
Производят забор крови, разделяют собранную кровь на плазму и фракцию клеток крови при помощи центрифугирования, затем фракцию клеток крови разделяют на эритроциты и лейкоциты при помощи центрифугирования в градиенте плотности. Далее элюируют ВНК, связанные с поверхностью эритроцитов в две стадии: сначала элюцию осуществляют 10 объемами фосфатного буферного раствора (ФБР), содержащего 5 мМ ЭДТА (этилендиаминтетрауксусная кислота) при 4°С, с последующим осаждением клеток центрифугированием и сбором супернатанта, а затем элюцию проводят равным объемом 0,25% раствора трипсина при 4°С, с последующим добавлением ингибитора фермента, осаждением клеток центрифугированием и сбором супернатанта. Элюцию ВНК, связанных с поверхностью лейкоцитов, также проводят в две стадии: сначала элюцию осуществляют 10 объемами ФБР, содержащим 5 мМ ЭДТА при 4°С, с последующим осаждением клеток центрифугированием и сбором супернатанта, а затем элюцию проводят равным объемом 0,125% раствора трипсина при 4°С, с последующим добавлением ингибитора фермента, осаждением клеток центрифугированием и сбором супернатанта.
Далее выделяют ВНК из полученных супернатантов (элюатов) и проводят амплификационный анализ не менее 2-х специфических последовательностей НК с использованием соответствующего метода (полимеразная цепная реакция, лигазная цепная реакция, мультиплексная ПЦР и другие).
Использование для анализа ВНК, связанных с поверхностью клеток крови, особенно эффективно для диагностики ранних стадий патогенеза, в частности рака, когда основная масса ВНК крови связана с клеточной поверхностью.
Определяющими отличительными признаками предлагаемого способа по сравнению с прототипом являются:
1. Использование в качестве диагностического объекта ВНК, связанных с поверхностью клеток крови (эритроцитов и лейкоцитов), что позволяет значительно повысить достоверность выявления специфических последовательностей НК на ранних стадиях заболеваний, связанных с нарушением функционирования генетического аппарата клетки, когда основная масса ВНК связана с клеточной поверхностью эритроцитов и лейкоцитов, а в плазме находятся лишь незначительные ее количества.
ВНК, связанные с поверхностью клеток крови, могут быть связаны с клеточной поверхностью в виде свободных НК, а также в составе комплексов с белками, липидами, липопротеинами (протеолипидами), в виде рибонуклеопротеиновых комплексов, нуклеосом и апоптических телец (10, 11). В прототипе анализируют специфические последовательности НК, выделенных из плазмы.
2. Разделение клеточной фракции крови на эритроциты и лейкоциты, что позволяет повысить достоверность диагностики за счет увеличения удельного содержания специфических последовательностей НК для дальнейшего амплификационного анализа.
3. Последовательная двухстадийная элюция ВНК с поверхности эритроцитов и лейкоцитов, что позволяет уменьшить количество балластных нуклеиновых кислот из нормальных клеток крови и увеличить удельное содержание выявляемых специфических последовательностей.
4. Проведение ПЦР-анализа не менее чем по двум известным специфическим последовательностям НК, вовлеченным в патогенез, и при их выявлении диагностирование наличия соответствующего заболевания.
Использование нового диагностического объекта – ВНК крови, связанных с клеточной поверхностью, позволяет увеличить чувствительность детекции специфических последовательностей ДНК и РНК за счет их повышенного удельного содержания на ранних стадиях патологенеза.
Изобретение иллюстрируется следующими примерами конкретного выполнения способа.
Пример 1
При проведении ежегодного обследования рабочих (производство плутония и, как следствие, риск онкозаболеваний дыхательных путей) в 1999 и 2000 годах были взяты образцы крови. Целью обследования было выявление среди рабочих с неопределенными хроническими заболеваниями легких (группа риска) профиля гиперметилирования генов (АРС и RASSF1A), вовлеченных в регуляцию онкообразований.
Взятую кровь, разделяли на плазму и фракцию клеток крови при помощи центрифугирования в течение 20 мин при 400 g, затем фракцию клеток крови разделяли на эритроциты и лейкоциты при помощи центрифугирования через среду для разделения лимфоцитов (Flow, USA) в течение 30 мин при 400 g. Далее элюировали ВНК, связанные с поверхностью эритроцитов в две стадии: сначала отмывали клетки добавлением 10 объемов ФБР, содержащего 5 мМ ЭДТА при 4°С, с последующим осаждением клеток центрифугированием и сбором супернатанта, а затем элюцию проводили равным объемом 0,25% раствора трипсина при 4°С, с последующим добавлением ингибитора фермента, осаждением клеток центрифугированием и сбором супернатанта. Элюцию ВНК, связанных с поверхностью лейкоцитов, также провели в две стадии: сначала элюировали ВНК 10 объемами ФБР, содержащего 5 мМ ЭДТА при 4°С, с последующим осаждением клеток центрифугированием и сбором супернатанта, а затем элюировали прочносвязанные ВНК равным объемом 0,125% раствора трипсина при 4°С, с последующим добавлением ингибитора фермента, осаждением клеток центрифугированием и сбором супернатанта.
ДНК выделяли из полученных элюатов, а также плазмы (для сравнения) методом сорбции на мелкодисперсном стекле (12). ДНК модифицировали обработкой бисульфитом натрия, при которой неметилированные цитозины в 5 положении превращаются в урацил (20 минут при 75°С в присутствии 3М NaOH; 4 часа при 56°С в присутствии Nа2S2О5; 30 минут при 37°С в присутствии 3М NaOH).
После начальной термической обработки модифицированной ДНК в течение 5 минут при 95°С добавляли 1 ед. Taq ДНК полимеразы (производства Института Цитологии и Генетики СО РАН, Россия) и проводили 55 циклов полимеразной цепной реакции в следующем режиме:
– для гена АРС – 45 секунд при 95.5°С, 45 секунд при 64°С, 45 секунд при 72°С; были использованы праймеры (13):
метилированная пара – 5’-TATTGCGGAGTGCGGGTC-3’ (Пр1),
5’-TCGACGAACTCCCGACGA-3’ (Пр2);
неметилированная пара – 5’-GTGTTATTGTGGAGTGTGGGTT-3’ (Пр1),
5’-ССААТСААСАААСТСССААСАА-3’ (Пр2);
– для гена RASSF1A – 45 секунд при 95.5°С, 45 секунд при 64°С (для метелированной пары праймеров), 45 секунд при 59°С (для неметилированной пары праймеров), 45 секунд при 72°С; были использованы праймеры (14):
метилированная пара – 5’-GGGTTTTGCGAGAGCGCG-3’ (Пр1),
5’-GCTAACAAACGCGAACCG-3’ (Пр2);
неметилированная пара – 5’-GGTTTTGTGAGAGTGTGTTTAG-3’ (Пр1),
5’-САСТААСАААСАСАААССАААС-3’ (Пр2);
После окончания 55 циклов полимеразной цепной реакции реакционную смесь инкубировали 5 минут при 72°С и охлаждали до 4°С.
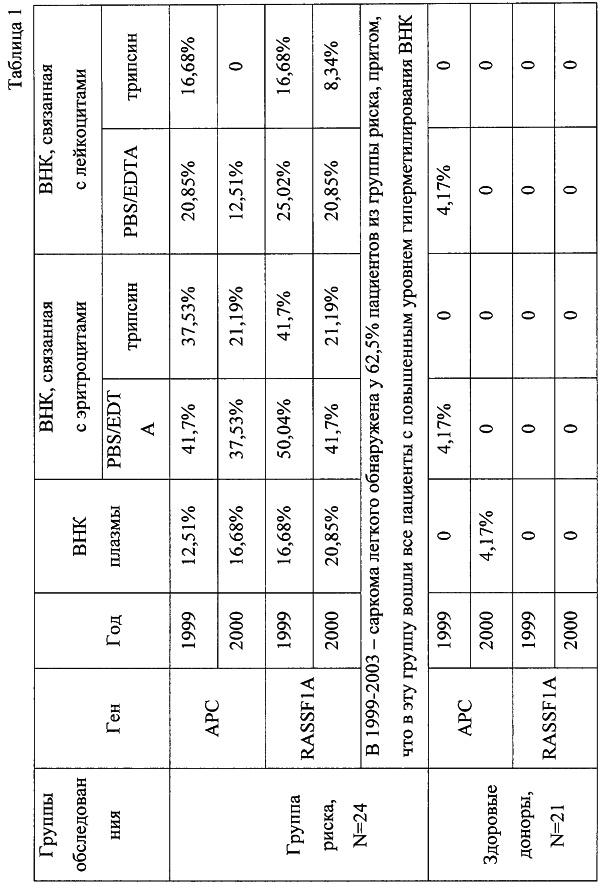
Полученные данные представлены в табл.1, из которой видно, что метилированные маркеры АРС и RASSF1A, ассоциированные с легочным канцерогенезом, выявляются с большой частотой (до 50,04%) в элюатах ВПК, связанных с клеточной поверхностью, на ранней стадии заболевания (обследование 1999 г.), что позволило поставить предварительный диагноз. Через год при повторном обследовании более высокий процент гиперметилированных маркеров в группе риска (до 20,85%) выявлялся уже и в образцах плазмы, что объясняется уменьшением количества ВНК, связанных с клеточной поверхностью. В течение 5 лет с момента первого взятия крови у 60% пациентов из группы риска был клинически подтвержден рак легкого. У всех больных, показавших положительный профиль гиперметилирования, был диагностирован рак легкого. Наиболее эффективное выявление специфических последовательностей обнаружено во фракции, содержащей ВНК, элюированные с поверхности эритроцитов обработкой ФБР/ЭДТА.
Данный пример иллюстрирует, что заявляемый способ может быть использован для ранней диагностики рака легкого, что способствует своевременному выбору правильной стратегии лечения.
Пример 2
У группы женщин (N=32), успешно прооперированных два года назад по поводу раковой опухоли груди и прошедших курс химиотерапии, были взяты образцы крови с профилактической целью, так как пациентки с раком груди входят в группу онкобольных с высоким риском повторных новообразований. Выделение ВНК, циркулирующих в плазме (для сравнения) и связанных с поверхностью эритроцитов и лейкоцитов, проводили аналогично примеру 1.
Для оценки экспрессии онкогенов, имеющих важное прогностическое значение при раке груди, мультиплексный количественный ПЦР-анализ провели с использованием праймеров, специфичных для генов с-mус и с-еrbВ2.
Без предварительной термической денатурации в реакционную смесь добавляли 1 ед. Tfl ДНК полимеразы (производства Tpicentre Technologies) и проводили 30 циклов полимеразной цепной реакции в следующем режиме:
– для гена c-myc – 1 минута при 94°С, 1 минута при 65°С, 2 минуты при 72°С; были использованы праймеры (15):
5’-CTCGAATTCCTTCCAGATATCCTCGCTG-3’ (Пр1);
5’-CACTGCGCGCTGCGCCAGGTTT-3’ (Пр2);
– для гена c-erbB2 – 1 минута при 94°С, 1 минута при 56°С, 2 минуты при 72°С; были использованы праймеры (16):
5’-CAGGTAGTTTGGCGTAAAAATAAA-3’ (Пр1);
5’-CAAAATCCAGGGTTTTTTAAGAGGT-3’ (Пр2).
После окончания 30 циклов ПЦР продукты были разделены в агарозном геле методом электрофореза, окрашены бромистым этидием и количественно оценены при помощи Системы Gel Doc 2000 (Bio-Rad) и компьютерной программы Quantity One (Bio-Rad).
Процент выявленной у пациенток (N=32) сверхэкспрессии исследованных генов представлен в табл.2
| Таблица 2 |
| Гены |
ДНК плазмы |
ДНК, связанная с клеточной поверхностью |
| Эритроциты |
Лейкоциты |
| с-mус |
0 |
9% |
9% |
| с-еrbВ2 |
0 |
9% |
9% |
Из табл.2 видно, что анализ ДНК, связанной с клеточной поверхностью, как эритроцитов, так и лейкоцитов, выявил сверхэкспрессию исследованных генов у 9% женщин (3/32), в то время как при анализе плазмы тех же пациенток были получены отрицательные результаты. В течение последующих двух лет у 9% пациенток были клинически диагностированы повторные метастазы в региональных лимфоузлах. При этом обнаружена одинаковая эффективность выявления специфических последовательностей из фракций, содержащих элюаты с поверхности и эритроцитов, и лейкоцитов.
Данный пример иллюстрирует, что разработанный способ может быть использован для оценки эффективности хирургического вмешательства и постоперационной терапии.
Пример 3
У 38 пациентов с подозрением на рак прямой кишки (группа риска) и у контрольной группы здоровых доноров были взяты образцы крови.
Выделение РНК, связанных с поверхностью эритроцитов и лейкоцитов, проводили аналогично примеру 1. Выявление двух маркерных последовательностей мРНК, цитокератина19 (СК19) и карциномоэмбрионального антигена (СЕА), проводили методом RT-PCR.
В реакционную смесь сразу добавляли 0,5 ед. Amply Taq Gold ДНК полимеразы и 3 ед. MultiScribe обратной транскриптазы (РЕ Diosystems, USA). Затем реакционную смесь последовательно инкубировали 12 минут при 42°С и денатурировали 9 минут при 95°С, после чего проводили 43 цикла (для СК19) и 40 циклов (для СЕА) полимеразной цепной реакции в следующих режимах:
– для гена СК19 – 30 секунд при 95°С, 30 секунд при 58°С, 1 минута при 72°С; были использованы праймеры (17):
5’-GTGGAGGTGGATTCCGTCC-3’ (Пp1),
5’-TGGCAATCTCCTGCTCCAGC-3’ (Пр2);
– для гена СЕА – 30 секунд при 95°С, 30 секунд при 65°С, 1 минута при 72°С; были использованы праймеры (17):
5’-TCTGGAACTTCTCCTGGTCTCTCAGCTGG-3’ (Пр1),
5’-TGTAGCTGTTGCAATGCTAAGGAAGAAGC-3’ (Пр2);
После окончания 43(40) циклов полимеразной цепной реакции реакционную смесь инкубировали 11 минут при 72°С.
Далее ПЦР продукты были разделены в полиакриламидном геле методом электрофореза и оценены денситометрически при помощи Системы GS-690 Imaging Densitometry (Bio-Rad) и компьютерной программы Multi-Analyst/PC (Bio-Rad).
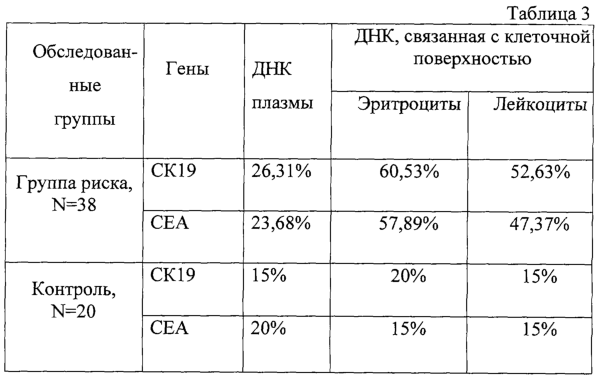
Полученные данные представлены в табл.3. Из табл.3 видно, что по результатам исследования ВНК, связанных с клеточной поверхностью, 60,53% предраковых пациентов имеют положительный результат хотя бы по одному из маркеров, в то же время в плазме выявляется только 26,31%. При этом более эффективное выявление специфических последовательностей обнаружено во фракции, содержащей ВНК, элюированные с поверхности эритроцитов.
Данный пример иллюстрирует, что разработанный способ может быть использован для диагностики онкозаболеваний на ранних стадиях.
Пример 4
У 32 женщин с преэклампсией были взяты образцы крови, 8 случаев были диагностированы как тяжелые. Для контроля были взяты пробы крови у женщин с нормально протекающей беременностью. Выделение ВНК, связанных с поверхностью эритроцитов и лейкоцитов, проводили аналогично примеру 1. Количественное определение (эквивалент генома на 1 мл крови) суммарной внеклеточной ДНК и мужской плодной внеклеточной ДНК, связанной с поверхностью клеток, проводили методом TaqMan real-time ПЦР с использованием праймеров, специфичных для генов SRY (локализация на Y-хромосоме) и GAPDH.
В реакционную смесь сразу добавлялась Amply Taq Gold ДНК полимераза (Perkin Eimer) из расчета 0, 025 ед. на 1  l и AmpErase урацил-N-гликозилаза (Perkin Eimer) из расчета 0,01 ед. на 1 l и AmpErase урацил-N-гликозилаза (Perkin Eimer) из расчета 0,01 ед. на 1  l. Затем реакционную смесь последовательно инкубировали 2 минуты при 50°С и денатурировали 10 минут при 95°С, после чего для обоих генов проводили 40 циклов полимеразной цепной реакции в следующем режиме: 1 минута при 60°С и 15 секунд при 95°С; были использованы следующие праймеры и флуоресцентные зонды (8): l. Затем реакционную смесь последовательно инкубировали 2 минуты при 50°С и денатурировали 10 минут при 95°С, после чего для обоих генов проводили 40 циклов полимеразной цепной реакции в следующем режиме: 1 минута при 60°С и 15 секунд при 95°С; были использованы следующие праймеры и флуоресцентные зонды (8):
– для гена GAPDH-
5’-CCCCACACACATGCACTTACC-3’ (Пр1);
5’-CCTAGTCCCAGGGCTTTGATT-3’ (Пр2);
5’-(FAM)AAAGAGCTAGGAAGGACAGGCAACTTGGG(TAMPA)-3’ (зонд).
– для гена SRY-
5’-TCCTCAAAAGAAACCGTGCAT-3’ (Пр1);
5’-AGATTAATGGTTGCTAAGGACTGGAT-3’ (Пр2);
5’-(6-carboxyfluorescein; FAM) CACCAGCAGTAACTCCCCACAACCTCTTT (6-carboxytetramethylrhodamine; TAMPA)-3’ (зонд).
Полученные данные представлены в табл.4. Из табл.4 видно, что количества ДНК, связанной с клеточной поверхностью (как суммарной, так и плодной), в группе женщин с тяжелой преэклампсией повышены в 10 раз по сравнению с группой женщин, беременность которых протекает нормально.
Данный пример иллюстрирует, что разработанный способ может быть использован для оценки тяжести патологии беременности, уточнения диагноза и мониторинга эффективности терапии.

Использование предлагаемого способа позволит по сравнению с прототипом повысить достоверность ранней диагностики заболеваний, связанных с нарушением функционирования генетического аппарата клетки, за счет:
– уменьшения количества балластных нуклеиновых кислот из нормальных клеток крови;
– увеличения удельного содержания выявляемых специфических последовательностей ВНК, связанных с клеточной поверхностью, по сравнению с содержанием специфических последовательностей ВНК, выделенных из плазмы крови;
– увеличения чувствительности детекции специфических (маркерных) последовательностей ДНК и РНК, связанных с клеточной поверхностью эритроцитов и лейкоцитов, что особенно важно на ранних стадиях развития патологий, когда основная масса внеклеточных кислот связана с поверхностью клеток крови.
ИСТОЧНИКИ ИНФОРМАЦИИ
16. Lonn U, Lonn S, Nilsson B, Stenkvist B. Prognostic value of erb-B2 and myc amplification in breast cancer imprints. Cancer, 1995, V.75 (11): 2681-2687.
Формула изобретения
1. Способ ранней диагностики заболеваний, связанный с нарушением функционирования генетического аппарата клетки, включающий забор крови, разделение собранной крови на плазму и клеточную фракцию, выделение внеклеточной нуклеиновой кислоты (ВНК), выявление специфической последовательности нуклеиновой кислоты методами амплификационного анализа с последующим анализом ПЦР-продуктов и составлением заключения о наличии или отсутствии детектируемых нуклеотидных последовательностей, отличающийся тем, что в качестве источника ВНК используют ВНК, связанные с поверхностью клеток крови, при этом фракцию клеток крови разделяют на эритроциты и лейкоциты, далее последовательно элюируют ВНК, связанные с клеточной поверхностью эритроцитов и лейкоцитов, из полученных элюатов выделяют ВНК, которые используют для выявления не менее двух известных специфических последовательностей нуклеиновой кислоты, связанных с определенным заболеванием.
2. Способ по п.1, отличающийся тем, что элюцию ВНК, связанных с поверхностью эритроцитов, осуществляют в две стадии: сначала элюцию осуществляют 10 объемами ФБР, содержащим 5 мМ ЭДТА при 4°С, с последующим осаждением клеток центрифугированием и сбором супернатанта, а затем элюцию проводят равным объемом 0,25% раствора трипсина при 4°С, с последующим добавлением ингибитора фермента, осаждением клеток центрифугированием и сбором супернатанта.
3. Способ по п.1, отличающийся тем, что элюцию ВНК, связанных с поверхностью лейкоцитов, осуществляют в две стадии: сначала элюцию осуществляют 10 объемами ФБР, содержащим 5 мМ ЭДТА при 4°С, с последующим осаждением клеток центрифугированием и сбором супернатанта, а затем элюцию проводят равным объемом 0,125% раствора трипсина при 4°С, с последующим добавлением ингибитора фермента, осаждением клеток центрифугированием и сбором супернатанта.
4. Способ по п.1, отличающийся тем, что ВНК из клеточных фракций крови выделяют преимущественно при помощи мелкодисперсного мешированного стекла в присутствии хаотропных солей.
5. Способ по п.1, отличающийся тем, что в качестве амплификационных методов используют полимеразную цепную реакцию, лигазную цепную реакцию, мультиплексную ПЦР.
6. Способ по п.1, отличающийся тем, что преимущественно осуществляют раннюю диагностику онкозаболеваний и патологий беременности.
РИСУНКИ
|