Патент на изобретение №2249818
|
||||||||||||||||||||||||||
(54) СПОСОБ ОПРЕДЕЛЕНИЯ СОДЕРЖАНИЯ БЕЛКОВ
(57) Реферат:
Изобретение относится к методам анализа различных объектов на содержание в них белков и может быть использовано в ряде отраслей пищевой промышленности, в частности молочной. Способ предусматривает создание аналитической среды с электрохимически активными компонентами, в которую вводят анализируемый на белки образец, измеряют потенциал индикаторного электрода и по калибровочному графику определяют содержание в нем белков. При этом в качестве аналитической среды используют щелочной раствор, содержащий ионы гидроксила и ионы меди(II) с массовым отношением 76-119, а измерение потенциала производят на медном индикаторном электроде при массовом отношении ионов меди(II) к белкам 0,156-6,97. Обеспечивается упрощение методики определения белков и повышение надежности измерений.
Изобретение относится к методам анализа различных объектов на содержание в них белков и может быть использовано в ряде отраслей пищевой промышленности, в частности молочной, а также при анализе других биологических систем. Известны различные способы определения содержания белков, например ультразвуковой, спектральный, рефрактометрический и др. [Бруславский Л.П., Фетисов Е.А., Шидловская В.П. Приборы контроля состава и качества молока. Молочная промышленность, №1, 1998, с.22-23]. Известен также потенциометрический способ определения белков с использованием ферментных электродов, основанном на том, что в результате реакции того или иного вещества с ферментом образуются продукты (ионы водорода, аммония, пероксид водорода и т.п.), к которым чувствителен тот или иной индикаторный электрод [Никольский Б.П, Матерова Е.А. Ионоселективньв электроды. – Л.: Химия, 1980. – 240 с., ил. (с.126-140). Морф В. Принципы работы ионоселективных электродов и мембранный транспорт: Пер. с англ. – М: Мир, 1985. – 280 с., ил (с.265-269)]. Измерив потенциал такого электрода в растворе с неизвестным содержанием белка, по предварительно построенному калибровочному графику находят содержание белка. Общим недостатком потенциометрии с использованием ферментных электродов является сложность их изготовления, связанная, в частности, с необходимостью фиксирования фермента на поверхности ионоселективного электрода (иммобилизации), сложностью выделения и очистки фермента, большая нестабильность показаний во времени. Цель изобретения – упрощение методики определений и повышение надежности измерений. Реализация предложенного способа осуществляется следующим образом. Создают аналитическую среду с электрохимически активными компонентами, вводят в нее анализируемый на белки образец, измеряют потенциал инцикаторного электрода относительно электрода сравнения и определяют по величине потенциала количество белков посредством калибровочного графика. Отличительной особенностью предлагаемого способа является то, что в качестве аналитической среды используют щелочной раствор, содержащий ионы гидроксила и ионы меди(II) с массовым отношением 76-119, а измерение потенциала производят на медном индикаторном электроде при массовом отношении ионов меди(II) к белкам 0,156 – 6,97. Предложенный способ выгодно отличается от прототипа простотой, поскольку не требуется специально готовить фермент, производить его очистку, фиксировать на поверхности ионоселеактивного электрода, периодически производить повторную калибровку электрода из-за естественного старения фермента. Последний факт особенно неприятен, поскольку существенно влияет на надежность измерений. Результаты произведенных измерений демонстрируются следующими примерами на серии стандартных образцов молока, содержание белков в которых определялось формольным методом и составляло 2,50% при плотности молока 1,028 г/мл. Пример 1. В стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 2,00 М водного раствора гидроксида натрия, 0,50 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. При этом отношение массы гидроксильных ионов к массе ионов Cu2+ Затем электрод извлекают из раствора, промывают, протравливают в кислоте, снова промывают в водопроводной и дистиллированной воде и удаляют остатки ее фильтровальной бумагой. В стакан с раствором вносят пипеткой 0,50 мл молока, что соответствует 0,0128 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -337 мВ. Пример 2. В другой стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 2,00 М водного раствора гидроксида натрия, 0,50 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. Затем в указанный раствор вносят 1,00 мл молока, что соответствует 0,0257 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем предварительно подготовленный, как в примере 1, медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -364 мВ. Пример 3. В третий стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 2,00 М водного раствора гидроксида натрия, 0,50 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. Затем в указанный раствор вносят 1,50 мл молока, что соответствует 0,0385 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем предварительно подготовленный, как в примере 1, медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -395 мВ. Пример 4. В четвертый стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 2,00 М водного раствора гидроксида натрия, 0,50 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. Затем в указанный раствор вносят 2,00 мл молока, что соответствует 0,0514 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем предварительно подготовленный, как в примере 1, медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -405 мВ. По экспериментальным данным примеров 1-3 строят калибровочный график в координатах: масса белков – потенциал электрода, которые укладываются на прямую (экспериментальные значения примера 4 не укладываются на этой прямой). Затем в условиях опытов, описанных в примере 1, в медно-щелочной раствор вносят: – 0,25 мл молока, смесь тщательно перемешивают, измеряют потенциал электрода при прочих равных условиях, который составляет -313 мВ, и по калибровочному графику определяют массу белков, которая составляет 0,0064 г, что в пересчете на процентное содержание белков в анализируемом образце составляет 2,5% при отношение массы Cu2+ к массе белков в образце – 1,40 мл молока, смесь тщательно перемешивают, измеряют потенциал электрода при прочих равных условиях, который составляет -392 мВ, и по калибровочному графику определяют массу белков, которая составляет 0,0360 г, что в пересчете на процентное содержание белков в анализируемом образце составляет 2,5% при отношение Пример 5. В стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 4,00 М водного раствора гидроксида натрия, 1,50 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. При этом отношение массы гидроксильных ионов к массе ионов Cu2+ Затем электрод извлекают из раствора, промывают, протравливают в кислоте, снова промывают в водопроводной и дистиллированной воде и удаляют остатки ее фильтровальной бумагой. В стакан с раствором вносят пипеткой 0,50 мл молока, что соответствует 0,0128 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -315 мВ. Пример 6. В другой стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 4,00 М водного раствора гидроксида натрия, 1,50 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. Затем в указанный раствор вносят 1,00 мл молока, что соответствует 0,0257 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем предварительно подготовленный, как в примерах 1, 5, медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -347 мВ. Пример 7. В третий стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 4,00 М водного раствора гидроксида натрия, 1,50 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. Затем в указанный раствор вносят 1,50 мл молока, что соответствует 0,0385 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем предварительно подготовленный, как в примерах 1, 5, медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -365 мВ. Пример 8. В четвертый стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 4,00 М водного раствора гидроксида натрия, 1,50 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. Затем в указанный раствор вносят 2,00 мл молока, что соответствует 0,0514 г белков, смесь тщательно перемешивают до однородного состояния, помешают в раствор электролитический ключ, затем предварительно подготовленный, как в примерах 1, 5, медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -393 мВ. По экспериментальным данным примеров 5-8 строят калибровочный график в координатах: масса белков – потенциал электрода, которые укладываются на прямую. Затем в условиях опытов, описанных в примере 5, в медно-щелочной раствор вносят: – 0,25 мл молока, смесь тщательно перемешивают, измеряют потенциал электрода при прочих равных условиях, который составляет -315 мВ, и по калибровочному графику определяют массу белков, которая составляет 0,0064 г, что в пересчете на процентное содержание белков в анализируемом образце составляет 2,5% при отношение массы Cu2+ к массе белков в образце – 1,80 мл молока, смесь тщательно перемешивают, измеряют потенциал электрода при прочих равных условиях, который составляет -380 мВ, и по калибровочному графику определяют массу белков, которая составляет 0,0463 г, что в пересчете на процентное содержание белков в анализируемом образце составляет 2,5% при отношении Пример 9. В стеклянный стакан на 50 мл вносят мерной пипеткой 22,5 мл 6,00 М водного раствора гидроксида калия, 2,00 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. При этом отношение массы гидроксильных ионов к массе ионов Cu2+ Затем электрод извлекают из раствора, промывают, протравливают в кислоте, снова промывают в водопроводной и дистиллированной воде и удаляют остатки ее фильтровальной бумагой. В стакан с раствором вносят пипеткой 0,50 мл молока, что соответствует 0,0128 г белков, смесь тщательно перемешивают до однородного состояния, помешают в раствор электролитический ключ, затем медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -362 мВ. Пример 10. В другой стеклянный стакан на 50 мл вносят мерной пипеткой 22,5 мл 6,00 М водного раствора гидроксида калия, 2,00 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. Затем в указанный раствор вносят 1,00 мл молока, что соответствует 0,0257 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем предварительно подготовленный, как в примерах 1, 5, медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -375 мВ. Пример 11. В третий стеклянный стакан на 50 мл вносят мерной пипеткой 22,5 мл 6,00 М водного раствора гидроксида калия, 2,00 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. Затем в указанный раствор вносят 1,50 мл молока, что соответствует 0,0385 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем предварительно подготовленный, как в примерах 1, 5, медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -395 мВ. Пример 12. В четвертый стеклянный стакан на 50 мл вносят мерной пипеткой 22,5 мл 6,00 М водного раствора гидроксида калия, 2,00 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. Затем в указанный раствор вносят 2,00 мл молока, что соответствует 0,0514 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем предварительно подготовленный, как в примерах 1, 5, медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -422 мВ. По экспериментальным данным примеров 9-12 строят калибровочный график в координатах: масса белков – потенциал электрода, которые укладываются на прямую. Затем в условиях опытов, описанных в примере 9, в медно-щелочной раствор вносят: – 0,25 мл молока, смесь тщательно перемешивают, измеряют потенциал электрода при прочих равных условиях, который составляет -352 мВ, и по калибровочному графику определяют массу белков, которая составляет 0,0064 г, что в пересчете на процентное содержание белков в анализируемом образце составляет 2,5% при отношении массы Cu2+ к массе белков в образце – 1,80 мл молока, смесь тщательно перемешивают, измеряют потенциал электрода при прочих равных условиях, который составляет -380 мВ, и по калибровочному графику определяют массу белков, которая составляет 0,0463 г, что в пересчете на процентное содержание белков в анализируемом образце составляет 2,5% при отношение Пример 13. В стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 10,00 М водного раствора гидроксида натрия, 4,00 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. При этом отношение массы гидроксильных ионов к массе ионов Cu2+ Затем электрод извлекают из раствора, промывают, протравливают в кислоте, снова промывают в водопроводной и дистиллированной воде и удаляют остатки ее фильтровальной бумагой. В стакан с раствором вносят пипеткой 1,00 мл молока, что соответствует 0,0257 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем медный электрод (как в примерах 1, 5) и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -383 мВ. Пример 14. В стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 10,00 М водного раствора гидроксида натрия, 4,00 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. Затем в указанный раствор вносят 2,00 мл молока, что соответствует 0,0514 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем предварительно подготовленный, как в примерах 1, 5, медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -403 мВ. Пример 15. В стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 10,00 М водного раствора гидроксида натрия, 4,00 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. Затем в указанный раствор вносят 3,00 мл молока, что соответствует 0,0771 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем предварительно подготовленный, как в примерах 1, 5, медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -421 мВ. По экспериментальным данным примеров 13-15 строят калибровочный график в координатах масса белков – потенциал электрода, которые укладываются на прямую. Затем в условиях опытов, описанных в примере 13, в медно-щелочной раствор вносят: – 0,25 мл молока, смесь тщательно перемешивают, измеряют потенциал электрода при прочих равных условиях, который составляет -372 мВ, и по калибровочному графику определяют массу белков, которая составляет 0,0068 г, что превышает действительную массу белков ва 6,2%, а в пересчете на процентное содержание белков в анализируемом образце оно составляет 2,65% при отношении массы Cu2+ к массе белков в образце – 2,50 мл молока, смесь тщательно перемешивают, измеряют потенциал электрода при прочих равных условиях, который составляет -380 мВ, и по калибровочному графику определяют массу белков, которая составляет 0,069 г, что превышает действительную массу белков на 7,8%, а в пересчете па процентное содержание белков в анализируемом образце оно составляет 2,68% при отношении Пример 16. В стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 10,00 м водного раствора гидроксида натрия, 7,00 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. При этом отношение массы гидроксильных ионов к массе ионов Cu2+ Затем электрод извлекают из раствора, промывают, протравливают в кислоте, снова промывают в водопроводной и дистиллированной воде и удаляют остатки ее фильтровальной бумагой. В стакан с раствором вносят пипеткой 1,00 мл молока, что соответствует 0,0257 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем медный электрод (как в примерах 1, 5) и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -356 мВ. Пример 17. В стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 10,00 М водного раствора гидроксида натрия, 7,00 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. Затем в указанный раствор вносят 2,00 мл молока, что соответствует 0,0514 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем предварительно подготовленный, как в примерах 1, 5, медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -365 мВ. Пример 18. В стеклянный стакан на 50 мл вносят мерной пипеткой 20,0 мл 10,00 М водного раствора гидроксида натрия, 7,00 мл водного раствора медного купороса с концентрацией Cu2+ 0,176 моль/л, смесь тщательно перемешивают до однородного состояния. Затем в указанный раствор вносят 3,00 мл молока, что соответствует 0,0771 г белков, смесь тщательно перемешивают до однородного состояния, помещают в раствор электролитический ключ, затем предварительно подготовленный, как в примерах 1, 5, медный электрод и производят измерение потенциала электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -371 мВ. По экспериментальным данным примеров 16-18 строят калибровочный график в координатах: масса белков – потенциал электрода, которые укладываются на прямую. Затем в условиях опытов, описанных в примере 16, в медно-щелочной раствор вносят: – 0,25 мл молока, смесь тщательно перемешивают, измеряют потенциал электрода при прочих равных условиях, который составляет -338 мВ, и по калибровочному графику определяют массу белков, которая составляет 0,0077 г, что превышает действительную массу белков на 20,3%, а в пересчете на процентное содержание белков в анализируемом образце оно составляет 3,0% при отношение массы Cu2+ к массе белков в образце – 2,50 мл молока, смесь тщательно перемешивают, измеряют потенциал электрода при прочих равных условиях, который составляет -370 мВ, и по калибровочному графику определяют массу белков, которая составляет 0,077 г, что превышает действительную массу белков на 20,3%, а в пересчете на процентное содержание белков в анализируемом образце оно составляет 3,0% при отношении Как следует из приведенных примеров, предложенный способ позволяет производить определение количественного содержания белков в анализируемых образцах потенциометрически в условиях, указанных в отличительной части описания. При этом он значительно проще прототипа, поскольку не требует дополнительных процедур по получению фермента, его закреплению на ионоселективном электроде, периодической калибровке электрода из-за старения фермента, что также повышает надежность результатов определений предлагаемым способом.
Формула изобретения
Способ определения содержания белков, включающий создание аналитической среды с электрохимически активными компонентами, введение в нее анализируемого на содержание белков образца, измерение потенциала индикаторного электрода относительно электрода сравнения и определение по величине потенциала количества белков посредством калибровочного графика, отличающийся тем, что в качестве аналитической среды используют щелочной раствор, содержащий ионы гидроксила и ионы меди (II) с массовым отношением 76÷119, а измерение потенциала производят на медном индикаторном электроде при массовом отношении ионов меди (II) к белкам 0,156÷6,97.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 18.07.2008
Извещение опубликовано: 20.07.2010 БИ: 20/2010
|
||||||||||||||||||||||||||

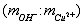 составляет 119. В раствор погружают на глубину 30 мм медный электрод, выполненный в виде стержня диаметром 1,8 мм и длиной около 100 мм, рабочую часть которого предварительно кратковременно протравливают в 3 М растворе соляной кислоты, тщательно промывают водопроводной и дистиллированной водой, остатки которой удаляют фильтровальной бумагой. Закрепляют медный электрод в штативе и подключают его проводником к клемме измерительного электрода датчика ДЛ-01. В стакан с анализируемым раствором помещают электролитический ключ, который через промежуточный сосуд с насыщенным раствором хлорида калия соединяют электролитически с насыщенным хлорсеребряным электродом сравнения, вмонтированным в датчик. Кабель датчика подключают к потенциометру, в качестве которого выступает рН-метр рН-340. Производят измерение потенциала медного электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -295 мВ.
составляет 119. В раствор погружают на глубину 30 мм медный электрод, выполненный в виде стержня диаметром 1,8 мм и длиной около 100 мм, рабочую часть которого предварительно кратковременно протравливают в 3 М растворе соляной кислоты, тщательно промывают водопроводной и дистиллированной водой, остатки которой удаляют фильтровальной бумагой. Закрепляют медный электрод в штативе и подключают его проводником к клемме измерительного электрода датчика ДЛ-01. В стакан с анализируемым раствором помещают электролитический ключ, который через промежуточный сосуд с насыщенным раствором хлорида калия соединяют электролитически с насыщенным хлорсеребряным электродом сравнения, вмонтированным в датчик. Кабель датчика подключают к потенциометру, в качестве которого выступает рН-метр рН-340. Производят измерение потенциала медного электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -295 мВ.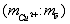 0,87;
0,87;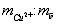 в образце 0,156.
в образце 0,156.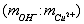 составляет 81. В раствор погружают на глубину 30 мм медный электрод, выполненный в виде стержня диаметром 1,8 мм и длиной около 100 мм, рабочую часть которого предварительно кратковременно протравливают в 3 М растворе соляной кислоты, тщательно промывают водопроводной и дистиллированной водой, остатки которой удаляют фильтровальной бумагой. Закрепляют медный электрод в штативе и подключают его проводником к клемме измерительного электрода датчика ДЛ-01. В стакан с анализируемым раствором помещают электролитический ключ, который через промежуточный сосуд с насыщенным раствором хлорида калия соединяют электролитически с насыщенным хлорсеребряным электродом сравнения, вмонтированным в датчик. Кабель датчика подключают к потенциометру, в качестве которого выступает рН-метр рН-340. Производят измерение потенциала медного электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -305 мВ.
составляет 81. В раствор погружают на глубину 30 мм медный электрод, выполненный в виде стержня диаметром 1,8 мм и длиной около 100 мм, рабочую часть которого предварительно кратковременно протравливают в 3 М растворе соляной кислоты, тщательно промывают водопроводной и дистиллированной водой, остатки которой удаляют фильтровальной бумагой. Закрепляют медный электрод в штативе и подключают его проводником к клемме измерительного электрода датчика ДЛ-01. В стакан с анализируемым раствором помещают электролитический ключ, который через промежуточный сосуд с насыщенным раствором хлорида калия соединяют электролитически с насыщенным хлорсеребряным электродом сравнения, вмонтированным в датчик. Кабель датчика подключают к потенциометру, в качестве которого выступает рН-метр рН-340. Производят измерение потенциала медного электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -305 мВ.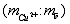 2,62;
2,62;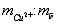 в образце 0,363.
в образце 0,363.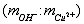 составляет 102. В раствор погружают на глубину 30 мм медный электрод, действуя далее согласно примерам 1, 5. Производят измерение потенциала медного электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -345 мВ.
составляет 102. В раствор погружают на глубину 30 мм медный электрод, действуя далее согласно примерам 1, 5. Производят измерение потенциала медного электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -345 мВ.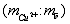 3,48;
3,48;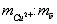 в образце 0,482.
в образце 0,482.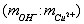 составляет 76. В раствор погружают на глубину 30 мм медный электрод, действуя далее согласно примерам 1, 5. Производят измерение потенциала медного электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -365 мВ.
составляет 76. В раствор погружают на глубину 30 мм медный электрод, действуя далее согласно примерам 1, 5. Производят измерение потенциала медного электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -365 мВ.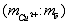 6,97;
6,97;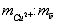 в образце 0,697.
в образце 0,697.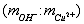 составляет 43. В раствор погружают на глубину 30 мм медный электрод, действуя далее согласно примерам 1,5. Производят измерение потенциала медного электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -342 мВ.
составляет 43. В раствор погружают на глубину 30 мм медный электрод, действуя далее согласно примерам 1,5. Производят измерение потенциала медного электрода после его стабилизации по истечении 3-5 минут при температуре раствора 25°С, который составляет -342 мВ.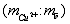 12,2;
12,2;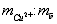 в образце 1,22.
в образце 1,22.