Патент на изобретение №2249479
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) КАТАЛИЗАТОР ДЛЯ ПОЛУЧЕНИЯ 2,3-ДИАЛКИЛ-1,10-ФЕНАНТРОЛИНОВ
(57) Реферат:
Изобретение относится к области катализаторов, в частности к катализатору для получения 2,3-диалкил-1,10-фенантролинов. Предлагаемый катализатор состоит из комплекса [Pr(NO3)5]·[C5H5NH]2, получаемого из нитрата празеодима, пиридина и азотной кислоты, взятых в соотношении 10:20:20 ммолей соответственно. Преимуществом катализатора является его доступность. 1 табл.
(56) (продолжение): CLASS=”b560m”Godard A. et. al. Synthesis of benzo[f]-1,7-naphthyridmes and benzo[h]-1,6-naphthyridines. Lab. Chim. Ord. Heterocycl. Inst. Natl. Super. Chim. Ind. Rouen, Mont-Saint-Aignan, Fr. Comptes Rendus des Seances de l’Academie des Sciences. Serie C: Sciences Chimiques. 284(12), 459-462, 1977.
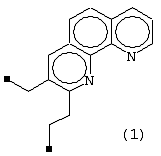
Изобретение относится к области катализаторов, в частности катализаторов для получения 2,3-диалкил-1,10-фенантролинов (1), которые могут найти применение в тонком органическом синтезе и аналитической химии в качестве индикатора окислительно-восстановительных реакций. Известен катализатор [У.М.Джемилев, Ф.А.Селимов, Р.А.Хуснутдинов, О.А.Пташко. Способ получения 1,10-, 1,7- и 4,7-фенантролинов. Патент №2117006 от 10.08.1998. Бюл. №22 (1998)] для получения смеси 1, 10-, 1,7- и 4,7-фенантролинов, состоящий из йодсодержащего соединения (KJ, СН3J, (СН3)4JN, (C2H5)4JN, (C3H7)4JN, (СН3)3С6H5JN, (С2Н5)3C6H5JN) и сульфата церия (IV), взятый в мольном соотношении 0.005:(0.005-0.01) соответственно. Процесс ведут при температуре 180-190°С и времени 8-10 часов. Известный катализатор не позволяет получать 2,3-диалкил-1,10-фенантролины. Известен катализатор [У.М.Джемилев, Ф.А.Селимов, Р.А.Хуснутдинов, А.А.Фатыхов, Е.Н.Андрейков, Г.А.Обанин. Синтез нафтиридинов и фенантролинов с использованием катализатора на основе переходных и редкоземельных металлов. Изв. АН. Серия хим., 1992, №5, 1139-1144] для получения 2.3-диалкил-1,10-фенантролинов, состоящий из хлорида празеодима (PrCl3), трифенилфосфина (Ph3Р) и диметилформамида (ДМФА). Недостатком известного катализатора является труднодоступность PrCl3 и Ph3P. Фосфорорганические соединения в стране не производятся, синтезируют их исходя из пирофорных Mg-органических реагентов и легко гидролизующихся галогенидов фосфора в две стадии. Предлагается новый катализатор для получения 2,3-диалкил-1,10-фенантролинов (1). Предлагаемый катализатор состоит из доступного комплекса [Pr(NО3)5]·[C5H5NH]2, получаемого из нитрата празеодима (Pr(NО3)3), пиридина (C5H5N) и азотной кислоты (НNО3), взятых в соотношении 10:20:20 ммолей соответственно. При другом соотношении исходных компонентов комплекс вида [Pr(NO3)5]·[С5Н5NН]2 не формируется. В присутствии указанного катализатора образуются 2,3-диалкил-1,10-фенантролины (1) с выходами 40-54%. Реакция осуществляется в инертной атмосфере при взаимодействии 8-аминохинолина с алифатическими альдегидами (RCH2CHO, где R=С2Н5, н-С3Н7, н-С4Н9), взятыми в соотношении 8-аминохинолин: RСН2СНО=10:20 ммолей, при температуре 150°С в течение 6 часов в смешанном растворителе этанол: ДМФА (3:1 объемные) по схеме: R=С2Н5, н-С3Н7, н-С4Н9; Кт=[Pr(NO3)5]·[C5H5NH]2 Количество катализатора, необходимое для проведения реакции, составляет 0.1-0.3 ммолей (1-3 мол.% по отношению к исходному 8-аминохинолину). Отличия предлагаемого катализатора от известных Предлагаемый катализатор состоит из доступного комплекса [Pr(NО3)5]·[C5H5NH]2, который получают смешиванием выпускаемого в стране Pr(NO3)3 (при извлечении празеодима из руды последнюю подвергают обработке азотной кислотой, при этом образуется нитрат празеодима), производимых в промышленных масштабах пиридина (C5H5N) и азотной кислоты (НNО3). Изобретение иллюстрируется примерами. Пример 1. Приготовление катализатора В стеклянный реактор объемом 100 мл, установленный на магнитной мешалке, помещают 20 мл воды, 20 ммоль пиридина (C5Н5N), прикапывают при перемешивании 20 ммоль HNO3, выдерживают ~1 час, затем добавляют 10 ммоль Pr(NО3)3, выдерживают при перемешивании ~1 час, удаляют при пониженном давлении воду до образования сухого остатка, представляющего собой комплекс состава [Pr(NО3)5]·[C5H5NH]2. Комплекс образуется практически с количественным выходом. Пример 2. Синтез 2,3-диалкил-1,10-фенантролинов Полученный катализатор, состоящий из комплекса [Pr(NО3)5]·[C5H5NH]2, взятый в количестве 0.2 ммоля, помещают в стальной автоклав, куда предварительно загружают 10 ммолей 8-аминохинолина, 20 ммолей масляного альдегида и смешанный растворитель, состящий из 3 мл этанола и 1 мл ДМФА. Автоклав нагревают 6 часов при температуре 150°С и постоянном перемешивании, затем охлаждают. Получают 2-(н-пропил)-3- этил-1,10-фенантролин (1) с выходом 48%. Спектр ЯМР 1Н ( Другие примеры, подтверждающие способ, приведены в табл.1.
Синтез 2,3-диалкил-1,10-фенантролинов проводили в смешанном растворителе, состоящем из этанола и ДМФА, взятых в соотношении 3:1 (объемные), при температуре 150°С в течение 6 часов в “пальчиковом” автоклаве при постоянном перемешивании.
Формула изобретения
Катализатор для получения 2,3-диалкил-1,10-фенантролинов, отличающийся тем, что он состоит из комплекса [Pr(NО3)5]·[С5Н5NН]2, получаемого из нитрата празеодима (Pr(NO3)3), пиридина (C5H5N) и азотной кислоты (HNO3), взятых в соотношении 10:20:20 ммолей.
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 24.06.2005
Извещение опубликовано: 27.01.2007 БИ: 03/2007
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

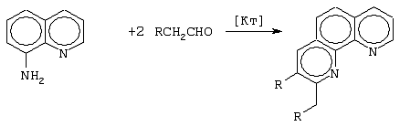
 , м.д.): 1.04 (т, 3Н, СН3), 1.29 (т, 3Н, СН3), 1.92 (м, 2Н, СН2), 2.95 (к, 2Н, СН2), 3.21 (т, 2Н, CH2), 7.65-9.27 (м, 6Н, аром.). Спектр ЯМР 13С (
, м.д.): 1.04 (т, 3Н, СН3), 1.29 (т, 3Н, СН3), 1.92 (м, 2Н, СН2), 2.95 (к, 2Н, СН2), 3.21 (т, 2Н, CH2), 7.65-9.27 (м, 6Н, аром.). Спектр ЯМР 13С (