|
|
(21), (22) Заявка: 2003104918/13, 18.02.2003
(24) Дата начала отсчета срока действия патента:
18.02.2003
(43) Дата публикации заявки: 27.11.2004
(45) Опубликовано: 20.03.2005
(56) Список документов, цитированных в отчете о
поиске:
RU 2193843 С2, 10.12.2002. RU 2150826 C1, 20.06.2000. RU 2129030 C1, 20.04.1999. SU 1757676 A1, 30.08.1992. SU 1804856 A1, 30.03.1993.
Адрес для переписки:
362040, РСО Алания, г. Владикавказ, ул. Кирова, 37, Горский ГАУ, патентный отдел
|
(72) Автор(ы):
Мамукаев М.Н. (RU),
Тохтиев Т.А. (RU)
(73) Патентообладатель(и):
Горский государственный аграрный университет (ГГАУ) (RU)
|
(54) СПОСОБ ПОВЫШЕНИЯ УСТОЙЧИВОСТИ ПТИЦЫ К ПУЛЛОРОЗУ
(57) Реферат:
Изобретение относится к птицеводству. В первую очередь, применено для повышения устойчивости. Яйца перед инкубацией облучают светом гелий-неонового лазера ЛГН-104, длиной волны 632,8 нм, плотностью мощности на поверхности яиц 50 мВт/см2· с, красным светом газоразрядной лампы ДНЕСГ-500, длиной волны 630-650 нм, мощностью на поверхности яиц 23,1 эрг и ультрафиолетом лампы ДРТ-400, длиной волны 185-400 нм, средней дозой на поверхности яиц 20 мэр/г, в экспозициях по 3 минуты. Способ эффективно повышает устойчивость птицы к пуллорозу. 4 ил., 4 табл.

Изобретение относится к птицеводству и может быть, в первую очередь, применено для повышения устойчивости птицы к воздействию возбудителя пуллороза Salmonella pullorum в производственных условиях.
Известен способ повышения жизнеспособности цыплят путем предынкубационной обработки яиц излучением гелий-неонового лазера ОКГ-12 длиной волны 632,8 нм, выходной мощностью 15 мВт/см2· с, при котором стимулируется рост, развитие, показатели естественной резистентности потомства /Петров Е.Б. Применение лучей гелий-неонового лазера для стимуляции эмбриогенеза кур и повышения жизнеспособности цыплят. – Автореф.дисс…канд. с/х наук: МВА – 1982 – 20 с./.
Известен способ стимуляции эмбрионального и постэмбрионального развития сельскохозяйственной птицы путем предынкубационного облучения яиц монохроматическим когерентным красным светом гелий-неонового лазера ЛГН-104, длиной волны 632,8 нм, мощностью на поверхности яиц 50 мВт/см2· с, при котором снижается эмбриональный отход, повышается вывод кондиционных цыплят на 7,56%, сохранность птицы к концу выращивания – на 5,95% /Мамукаев М.Н., Мамукаев Р.Х. Установка для лазерного облучения яиц. Авторское свидетельство № 1821958 /.
Известен способ профилактики пуллороза птиц путем предынкубационной обработки яиц излучением гелий-неонового лазера ЛГП-104, длиной волны 632,8 нм, плотностью мощности на поверхности яиц 50 мВт/см2· с /Мамукаев М.Н. Решение о выдачи патента по заявке № 2000110969/13/011534, прототип /.
Недостатками известных способов является то, что не выявляют специфическую устойчивость птицы к пуллорозу при комплексной предынкубационной обработке яиц излучением гелий-неонового лазера ЛГН-104, газоразрядной лампы ДНЕСГ-500 и ультрафиолета лампы ДРТ-400, не определены содержание и активность лизоцима сыворотки крови птицы, полученной из облученных яиц, относительно тест-культуры Micrococcus lisodeicticus и возбудителя пуллороза Salmonella pullorum не проведены микробиологические исследования.
Цель изобретения – повышение специфической устойчивости птицы к воздействию возбудителя пуллороза Salmonella pullorum в условиях неблагополучного птицехозяйства.
Эта цель достигается тем, что крупные эмбрионы перед инкубацией облучаются монохроматическим когерентным красным светом гелий-неонового лазера ЛГН-104 длиной волны 632,8 нм, плотностью мощности на поверхности яиц 50 мВт/ см2· с, красным светом газоразрядной лампы ДНЕСГ-500, длиной волны 630-650 нм, мощностью на поверхности яиц 23,1 эрг и ультрафиолетом лампы ДРТ-400, длиной волны 185-400 нм, средней дозой на поверхности яиц 20 мэр/г в экспозициях по 3 минуты.
Обработку инкубационных яиц лучистой энергией проводили в экспериментальной установке для светолазерной активации /Мамукаев М.Н. Авт. свид. № 1748768,1989 г./.
Содержание лизоцима в сыворотке крови бройлеров всех опытных групп по сравнению с показателем контроля во все возрастные периоды исследований было выше /табл.1/.
| ТАБЛИЦА 1 |
| Содержание лизоцима в сыворотке крови бройлеров при светолазерной активации, n=50 /X±mx/, мкг/мл |
| Группы |
Источники света |
Возраст птицы |
| |
|
1 |
15 |
30 |
45 |
| 1 |
2 |
3 |
4 |
5 |
6 |
| 1- контрольн. |
– |
4,05±0,02 |
3,35±0,05 |
2,97±0,05 |
2,67± 0,08 |
| 2 опыты |
ЛГН 104 |
5,93±0,06 |
4,36±0,06 |
3,79± 0,02 |
3,18± 0,05 |
| 3- ‘-“ |
ДНЕСГ – 500 |
4,52± 0,05 |
3,92±0,07 |
3,20±0,04 |
2,84± 0,06 |
4 – “- |
ДРТ – 400 |
6,02±0,06 |
4,36± 0,07 |
3,46±0,02 |
3,12± 0,05 |
| 5 – “-“ |
ЛГН – 104 |
6,33±0,04 |
5,14±0,07 |
4,12±0,02 |
3,88± 0,4 |
| |
ДНЕСГ – 500 |
|
|
|
|
| |
ДРТ – 400 |
|
|
|
|
У суточных бройлеров 2 группы содержание лизоцима по сравнению с 1 группой было выше на 1,88 мкг/мл, 3 – на 0,47 мкг/мл, 4 – на 0,97 мкг/мл и 5 – на 2,83 мкг/мл. При исследовании содержания лизоцима в остальные возрастные периоды сохраняется такая же закономерность с той разницей, что с возрастом птицы показатель снижается. Если у суточных цыплят всех групп показатель колебался от 4,05 до 6,33 мкг/мл, то у 15-дневных – от 3,35 до 5,14; 30-дневных – от 2,97 до 4,12 и у 45-дневных – от 2,67 до 3,88 мкг/мл. Причем различия содержания лизоцима между 30 – и 45 – дневными бройлерами менее контрастны, чем между суточными 15- и 30-дневными.
Содержание лизоцима в сыворотке крови бройлеров, выведенных из яиц после лазерного воздействия /2 г/, было выше, чем у цыплят 3 группы /красный свет/, а по сравнению с 5 группой /комплексная обработка/ было ниже. Различия по содержанию лизоцима в сыворотке крови бройлеров 2 и 4 групп /лазерное и ультрафиолетовое воздействие/ оказались несущественными и носили недостоверный характер / Р>0,05 /. Показатели активности лизоцима сыворотки крови опытных бройлеров относительно тест-культуры Micrococus lysodeicticus на 0,75 ч реакции достоверно превышали результаты контрольной группы /31,01% – лизиса во 2; 3; 4; 5 группах – на 10,68%; 3,12%; 10,96 и 11,98% /табл.2/. Аналогичные данные получены при исследованиях через 8, 16 и 24 часа реакции с той разницей, что различия результатов были более контрастны на 24 часе реакции.
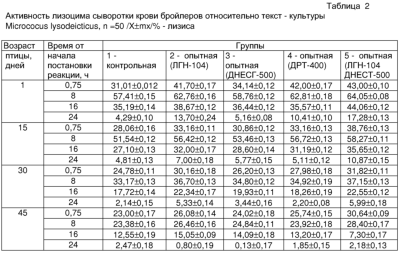
При исследовании бактерицидной активности лизоцима сыворотки крови 30-дневных бройлеров установлено, что по сравнению с первой группой у птицы 2 группы она была выше на 5,38%, 3 – на 1,42%, 4 – на 3,20 и 5 – на 7,04%. Аналогичная закономерность наблюдалась также через 8; 16 и 24 ч реакции сыворотки крови и тест-микробов, однако более высокие результаты 4 группы относительно контроля носили недостоверный характер /Р>0,05/.
Лизоцимная активность сыворотки крови бройлеров, выведенных из яиц после лазерного воздействия, была достоверно выше, чем при обработке красным светом /Р<0,001/. Различия между 1 и 4 группами оказались недостоверными /Р>0,05/. Активность лизоцима сыворотки крови 5 (комплексная обработка) группы во все периоды исследований была выше, чем у птицы 2 группы / Р<0,001/.
Установлено, что активность лизоцима сыворотки крови до 8 ч реакции возрастала, затем снижалась, достигая первоначального уровня у суточных цыплят к 22-23 ч, у 30-дневных – к 18-20 ч. Это указывает на то, что лизоцим сыворотки крови до 8 ч реакции проявляет бактерицидное действие, а с 8 до 16 ч – бактериостатическое.
Уровень лизоцимной активности сыворотки крови оказался более высоким у бройлеров 1- и 15-дневного возраста, чем у 30-и 45-дневных, что положительно коррелирует с показателями содержания лизоцима в сыворотке крови.
Анализ результатов исследования влияния световой энергии на активность сыворотки крови подопытных цыплят-бройлеров показал, что светолазерная обработка в оптимальных дозах в значительной мере способствует повышению бактерицидной и бактериостатической активности сыворотки крови относительно возбудителя пуллороза Salmonella pullorum /фиг.1; 2/.
На 0,75 часе реакции сыворотки крови суточных бройлеров и Salmonella pullorum относительно результатов контрольной группы % лизиса во 2 группе был достоверно выше на 1,70%, в 3 – на 0,44, в 4 – на 1,95 и в 5 группе – на 2,21%, соответственно через 8 ч реакции – на 1,78%; 0,98; 2,67 и 2,79%, через 16 ч – на 2,05%; 0,57; 1,64 и 2,72%, через 24 ч реакции – на 1,47%; 0,73; 0,15 и 2,41%, однако различия контроля и 4 группы были недостоверны /Р>0,05/.
Таким образом, результаты исследований активности сыворотки крови подопытных цыплят относительно бактерицидности и бактериостатичности к Salmonella pullorum показывают, что стабильное повышение этих показателей наблюдаются в группах применения лазерных, красных и ультрафиолетовых лучей в комплексе, а также при применении лазерных лучей. В группе ультрафиолета после 16 ч инкубирования ингредиентов, наблюдается быстрый спад активности сыворотки крови, достигая первоначального уровня оптической плотности.
В исследованиях просматривается закономерное повышение активности лизоцима до 8 ч инкубирования и снижение результатов после 8 ч, достигая минимальных величин, за исключением группы комплексного облучения яиц.
Установлено, что активность сыворотки крови месячных бройлеров во всех опытных группах была выше, чем в контроле. Исключение составляет 3 группа, где разница с контролем на 16 ч исследований была минимальной.
При учете оптической плотности некоторых проб после инкубирования сыворотки крови месячных бройлеров и возбудителя пуллороза Salmonella pullorum в растворе наблюдали резкое снижение оптической плотности и появление хлопьевидного осадка, что указывает на реакцию агглютинации.
Обобщая результаты исследований, следует отметить, что определение бактерицидной и бактериостатической активности сыворотки крови можно рекомендовать как тест для определения резистентности птицы при пуллорозе-тифе. Она свидетельствует о более высокой степени устойчивости организма птицы, полученного из яиц после световой обработки перед закладкой для инкубирования. Наиболее высокие результаты были зарегистрированы в группе молодняка, полученного из яиц после комплексной обработки лазерным, красным и ультрафиолетовым светом. При сравнении применения лазерного света и ультрафиолета до 16 ч инкубирования достоверно отличимых результатов не обнаружено, однако после 16 ч в группе применения ультрафиолета активность сыворотки крови снижается более резко у суточных цыплят, достигая величин контроля. Относительно группы применения монохроматического красного света лазерный свет более активен в стимуляции бактерицидных и бактериостатичаских свойств сыворотки крови.
Результаты исследований лизоцимной, бактерицидной и бактериостатической активности сыворотки крови бройлеров при светолазерной активности положительно согласуются с показателями жизнеспособности птицы в постнатальном онтогенезе /табл 3/.
| ТАБЛИЦА 3 |
| Сохранность бройлеров при светолазерной активации, n=200, /X±mx/ |
| Группы |
Источники света |
Возраст птицы, дней |
| |
|
15 |
30 |
45 |
| |
|
Гол. |
% |
Гол. |
% |
Гол. |
% |
| 1 – контр. |
– |
194,19±0,89 |
97,10 |
186,27± 2,18 |
93,14 |
180,18±1,84 |
90,09 |
| 2 – опытн. |
ЛГН-104 |
198,49±0,80 |
99,25 |
l95,97±1,13 |
97,99 |
190,82±1,40 |
95,41 |
| 3 опытн. |
ДНЕСГ-500 |
199,77±1,23 |
99,89 |
192,64±1,13 |
96,32 |
187,33±1,90 |
93,67 |
| 4 ~ опытн. |
ДРТ-400 |
199,16±0,33 |
99.58 |
195,9± 1,16 |
97,96 |
190,40±1,56 |
95,20 |
| 5 – опытн. |
ЛГН-104 ДНЕСГ-500 ДРТ-400 |
199,99±0,09 |
99,99 |
198,45±1,36 |
99,23 |
192,27±1,80 |
96.14 |
У бройлеров, выведенных при светолазерной обработке инкубационных яиц, побочных явлений не наблюдалось.
Установлено, что в 15-дневном возрасте сохранность бройлеров по сравнению с контролем была выше во 2 группе на 2,21%; в 3 – на 2,87%; в 4 – на 2,56% и в 5 группе – на 2,99%. Аналогичные результаты зарегистрированы на 30 день. На 45 день отбора по сравнению с контролем сохранность бройлеров была выше во 2 группе – на 5,91%, в 3 – на 3,97%, в 4 – на 5,67% и в 5 группе – на 6,71% /Р<0,01-0,001/.
Сохранность птицы была выше в группе бройлеров, полученных из яиц после комплексной обработки лазерным, красным и ультрафиолетовым светом. Существенных различий в жизнеспособности птицы после лазерного и ультрафиолетового облучения не выявлено.
Общая заболеваемость бройлеров к 30-дневному возрасту составила в контрольной группе -15,5%; при облучении лазерным светом – 16,5%, красным и ультрафиолетовым светом по 16,0% и при комплексном воздействии – 15%. Общая летальность составила соответственно 38,71%, 21,21%; 28,12%; 25,00%, 16,67%/табл. 4, фиг.3, 4/.
| ТАБЛИЦА 4 |
| Заболеваемость месячных бройлеров пуллорозом при светолазерной активации и летальность, n=200. |
| Группа |
Источник света |
Поголовье к месячному возрасту, гол |
Заболело. гол |
ППало всего, гол |
Выделено возбудителя пуллороза, проб |
Реагировало положительно по РА, проб |
Итого заболело пуллорозом гол. |
| 1 – контр. |
~ |
188 |
31 |
12 |
6 |
24 |
30 |
| 2-опытн. |
ЛГН-104 |
193 |
33 |
7 |
4 |
29 |
33 |
| 3-опытн. |
ДНЕСТ-500 |
191 |
32 |
9 |
5 |
26 |
31 |
| 4-опытн. |
ДРТ-400 |
192 |
32 |
8 |
5 |
28 |
33 |
| 5-опытн. |
ЛГН-104 ДНЕСТ-500 ДРТ-400 |
195 |
30 |
5 |
2 |
32 |
34 |
Бактериологические исследования отхода птицы до месячного возраста выращивания показали, что в контрольной группе из 12 исследованных павших цыплят выделено пуллороза Salmonella pullorum соответственно при воздействии лазера ЛГН-104 – 7 и 4, лампой ДНЕСТ-500 – 9 и 5, ДРТ-400 – 8 и 5 и при комплексном воздействии – 5 и 2.
При серологических исследованиях по реакции агглютинации положительно реагировало в 1 группе из 188 проб 24 /12,77%/, во 2 – из 193 29 /15,03%/, в 3 – из 191 26 /13,61%/, в 4 – из 192 28 /14,58/ и в 5 группе – из 195 32 /16,41%/.
Следовательно, по данным бактериологических, серологических исследований из 200 бройлеров в опыте контактировало с возбудителем пуллороза в 1 группе – 15%; во 2 и 4 – по 16,5%; в 3 – 15,5% и в 5 группе – 17%. Летальность составила 20,00; 12,12; 16,13; 15,15 и 5,88% в соответствующих группах.
Таким образом, результаты исследований общей жизнеспобности, выживаемости птицы в условиях неблагополучного по пуллорозу хозяйства, бактерицидной и бактериостатической активности лизоцима сыворотки крови относительно тест-микробов Micrococcus lisodeicticus, возбудителя пуллороза Salmonella pullorum серологических и микробиологических исследований показывают, что использование предлагаемого способа предынкубационной комплексной обработки эмбрионов кур излучениями лазера ЛГН-104, ламп ДНЕСГ-500 и ДРТ-400 в экспозициях по 3 минуты повышает устойчивость птицы к воздействию возбудителя пуллороза-тифа птиц.
Формула изобретения
Способ повышения устойчивости птицы к пуллорозу, включающий прединкубационную обработку яиц излучением гелий – неонового лазера ЛГН-104, длиной волны 632,8 нм, плотностью мощности на поверхности яиц 50 мВт/см2· с, отличающийся тем, что прединкубационную обработку яиц проводили комплексно светом гелий-неонового лазера ЛГН-104, длиной волны 632,8 нм, плотностью мощности на поверхности яиц 50 мВт/см2· с, газоразрядной лампой ДНЕСГ-500, длиной волны 630-650 нм, мощностью на поверхности яиц 23,1 эрг и ртутно-кварцевой лампой ДРТ-400, длиной волны 185-400 нм, мощностью на поверхности яиц 20 мэр/г, в экспозициях по 3 минуты.
РИСУНКИ
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 19.02.2005
Извещение опубликовано: 27.01.2007 БИ: 03/2007
|
|