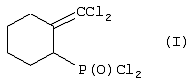Патент на изобретение №2247728
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ДИХЛОРАНГИДРИДА 2-ДИХЛОРМЕТИЛЕНЦИКЛОГЕКСИЛФОСФОНОВОЙ КИСЛОТЫ
(57) Реферат:
Изобретение относится к химии фосфорорганических соединений с Р-С связью, а именно к способу получения нового дихлорангидрида 2-дихлорметиленциклогексилфосфоновой кислоты формулы: Способ получения соединения формулы (I) включает взаимодействие 2-алкокси-7,7-дихлорбицикло [4,1,0] гептана с треххлористым фосфором и треххлористым алюминием при их молярном соотношении 1:1:1 или 1:2:1, с последующей обработкой образующегося комплекса водой в среде хлористого метилена. Технический результат: расширение арсенала фосфорорганических соединений для использования его в качестве полупродукта фосфорорганического синтеза.
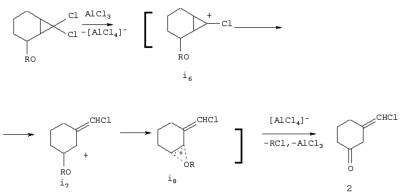
Изобретение относится к химии фосфорорганических соединений с Р-С связью, а именно к способу получения дихлорангидрида 2-дихлорметиленциклогексилфосфоновой кислоты формулы который может быть использован как ценный полупродукт фосфорорганического синтеза. Известен способ получения дихлорангидрида циклогексилфосфоновой кислоты, заключающийся во взаимодействии циклогексана и треххлористого фосфора в присутствии кислорода (Соборовский Л.З. и др. ДАН СССР, 1949. Т.67. С.293). Недостатками этого способа является низкий выход целевого продукта (36%) и высокая взрывоопасность процесса, связанного с применением газообразного окислителя – кислорода. Известен способ получения дихлорангидрида циклогексилиденметилфосфоновой кислоты, который заключается во взаимодействии метиленциклогексана с пятихлористым фосфором в инертном органическом растворителе с последующей обработкой промежуточного аддукта сернистым газом (Розинов В.Г. и др. Основной органический синтез и нефтехимия. Ярославль, 1978, №10, с.59-68). К недостаткам этого способа относится дополнительное использование токсичного газообразного сернистого газа, многостадийность процесса, а также образование побочного продукта – дихлорангидрида 1-хлорциклогексил фосфоновой кислоты. При этом получить указанными способами дихлорангидрид 2-дихлорметиленциклогексилфосфоновой кислоты формулы (1) не представляется возможным из-за особенности строения исходного соединения. Известен способ получения дихлорангидридов алкилфосфоновых кислот, который заключается во взаимодействии хлоралканов с трихлоридами фосфора и алюминия с последующей обработкой образующегося комплекса водой (Патент 707961 Великобритания, A.M.Kinnear, E.A.Perren. Заявлено 30.04.1948; опубл. 28.04.1954). Однако этот способ не позволяет получить дихлорангидрид 2-дихлорметиленциклогексилфосфоновой кислоты, поскольку в используемом для его синтеза исходном хлорциклоалкане – 2-хлор-1-дихлорметиленциклогексане, содержатся два реакционных электрофильных центра, что неизбежно приводит к неоднозначному протеканию процесса. При создании изобретения ставилась задача получить дихлорангидрид 2-дихлорметиленциклогексилфосфоновой кислоты, который расширит арсенал фосфорорганических соединений как ценный полупродукт фосфорорганического синтеза. Техническим результатом является получение дихлорангидрида 2-дихлорметиленциклогексилфосфоновой кислоты, который расширяет арсенал соединений, используемых в качестве полупродукта фосфорорганического синтеза. Поставленная задача достигается тем, что способ получения дихлорангидрида 2-дихлорметиленциклогексилфосфоновой кислоты формулы включающий взаимодействие 2-алкокси-7,7-дихлорбицикло [4,1,0] гептана с треххлористым фосфором и треххлористым алюминием при их молярном соотношении 1:1:1 или 1:2:1, с последующей обработкой образующегося комплекса водой в среде хлористого метилена. Сущность изобретения заключается в следующем способе получения дихлорангидрида 2-дихлорметиленциклогексилфосфоновой кислоты формулы: К суспензии, содержащей трихлорид алюминия и трихлорид фосфора прибавляют по каплям при комнатной температуре 2-алкокси-7,7-дихлорбицикло [4,1,0] гептаны. После перемешивания к образовавшемуся комплексу добавляют хлористый метилен и при 0°С прибавляют по каплям воду. Выпавший кристаллогидрат трихлорида алюминия отделяют фильтрованием и промывают хлористым метиленом. Выделение и очистку целевого продукта проводят обычными приемами. Строение полученного дихлорангидрида (1) подтверждено методами ИК, ЯМР 1H и 31P спектроскопии. Реакция протекает как по трехчленному циклу, так и с участием эфирной группы. При этом в результате атаки трихлорида алюминия по атому кислорода алкоксигруппы, по-видимому, образуются комплексы n Выход дихлорангидрида (1) обусловлен протеканием конкурирующей реакции по трехчленному циклу. При этом в интермедиате (i6), вероятнее всего, происходит разрыв связи С(1)-С(7), и образуются карбкатионы (i7), стабилизирующиеся за счет образования мостикового иона оксония (i8). Последний под действием трихлорида фосфора, хлорид- или тетрахлоралюминат-анионов, присутствующих в реакционной смеси, превращается в 3-хлорметиленциклогексанон (2). Для получения дихлорангидрида 2-дихлорметиленциклогексилфосфоновой кислоты использовали следующие вещества: Фосфор трехлористый – ГОСТ 91-41; Алюминий треххлористый, безводный ТУ 6-01-2-88; Метилен хлористый МРТУ 6-09-5362-98; 2-Метокси-7,7-дихлорбицикло[4,1,0] гептан, т.кип.122-124°С (28 мм рт.ст.), d20 41.2144, n20D1,4903; 2-Этокси-7,7-дихлорбицикло[4,1,0] гептан, т.кип.112-114°С (15 мм рт.ст.), d20 41.1675, n20D1,4905. Осуществление способа иллюстрируется следующими примерами. Пример 1. Дихлорангидрид 2-дихлорметиленциклогексилфосфоновой кислоты. К суспензии 3,7 г трихлорида алюминия и 7,2 г трихлорида фосфора прибавляли по каплям и комнатной температуре 5,4 г 2-метокси-7,7-дихлорбицикло[4.1.0] гептана. Через 1 час образовавшийся комплекс растворяли в 30 мл хлористого метилена и при 0°С прибавляли по каплям 4,5 г воды. Выпавший кристаллогидрат трихлорида алюминия, отфильтровали, промывали 10 мл хлористого метилена и перегонкой получили 2,9 г (40%) целевого дихлорангидрида, т. кип.127-129°С (5 мм рт. ст.), d204 1,4867, n20D 1,5346. Найдено, %: С1 50,12, Р 11,03. C7H9Cl2OP. Вычислено, %: Сl 50,30, Р 10,99. Спектр ЯМР 31Р: Пример 2. Аналогично примеру 1 к суспензии из 3,7 г трихлорида алюминия и 3,6 г трихлорида фосфора прибавляли по каплям при комнатной температуре 5,4 г 2-метокси-7,7-дихлорбицикло[4.1.0] гептана и 4,5 г воды в среде 50 мл хлористого метилена, получили 3,3 г (36%) целевого дихлорангидрида, т. кип.129-130°С (5 мм рт.ст.), d204 1,4865, n20D1,5343. Найдено, %: Сl 49,99, Р 10,80. C7H9Cl4OP. Вычислено, %: Сl 50,30, Р 10,99. Пример 3. Аналогично примеру 1 из 5,5 г трихлорида алюминия, 5,7 г трихлорида фосфора, 8,6 г 2-этокси-7,7-дихлорбицикло[4.1.0]гептана и 4,5 г воды в среде 50 мл хлористого метилена получили 3,3 г (36%) целевого дихлорангидрида, т. кип.128-130°С (5 мм рт.ст.), d204 1,486, n20D1,5341. Найдено, %: Сl 49,97, Р 10,79. C7H9Cl9OP. Вычислено, %: Сl 50,30, Р 10,99. Из низкокипящей фракции выделили 1,4 г (30%) 3-хлор-метиленциклогексанона т. кип.100-102°С (12 мм рт. ст.), d204 1,2471, n20D 1,5084. Найдено %: Сl 39,81. С7Н9СlO, Вычислено, %: Сl 39,60. Пример 4. Аналогично примеру 1 из 5,5 г трихлорида алюминия, 11,4 г трихлорида фосфора, 8,6 г 2-этокси-7,7-дихлорбицикло[4.1.0]гептана и 4,5 г воды в среде 50 мл хлористого метилена получили 3,3 г (36%) целевого дихлорангидрида, т. кип.128-130°С (5 мм рт. ст.), d204 1,4862, n20D1,5342. Найдено, %: Сl 49,95, Р 10,78. C7H9Cl4OP. Вычислено, %: Сl 50,31, Р 10,99. Таким образом, заявляемым изобретением получено не описанное в литературе фосфорорганические соединение, которое может найти применение для использования его в качестве полупродукта фосфорорганического синтеза.
Формула изобретения
Способ получения дихлорангидрида 2-дихлорметиленциклогексилфосфоновой кислоты формулы включающий взаимодействие 2-алкокси-7,7-дихлорбицикло [4,1,0] гептана с треххлористым фосфором и треххлористым алюминием при их молярном соотношении 1:1:1 или 1:2:1 с последующей обработкой образующегося комплекса водой в среде хлористого метилена.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 30.10.2005
Извещение опубликовано: 20.06.2007 БИ: 17/2007
|
||||||||||||||||||||||||||

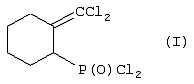
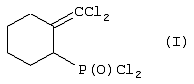
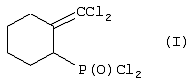
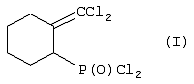
 -типа (i1), которые с разрывом С-O связи распадаются на алкокситрихлоралюминат-анион (i2) и 7,7-дихлорбицикло[4,1,0] гептил-2-катион (i3). Последний, с раскрытием трехчленного цикла, изомеризуется в более устойчивый карбкатион (i4) аллильного типа, стабилизирующийся присоединением трихлорида фосфора и аниона (i2). Последующий гидролиз этих комплексов i5 приводит к целевому дихлорангидриду 2-дихлорметиленциклогексилфсфоновой кислоты (1).
-типа (i1), которые с разрывом С-O связи распадаются на алкокситрихлоралюминат-анион (i2) и 7,7-дихлорбицикло[4,1,0] гептил-2-катион (i3). Последний, с раскрытием трехчленного цикла, изомеризуется в более устойчивый карбкатион (i4) аллильного типа, стабилизирующийся присоединением трихлорида фосфора и аниона (i2). Последующий гидролиз этих комплексов i5 приводит к целевому дихлорангидриду 2-дихлорметиленциклогексилфсфоновой кислоты (1).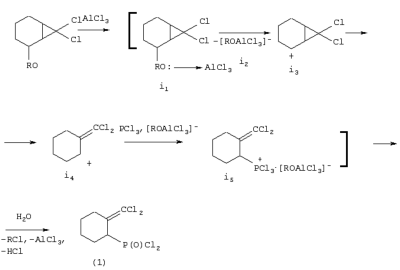
 р 52 м.д. ИК спектр (
р 52 м.д. ИК спектр (