Патент на изобретение №2247116
|
||||||||||||||||||||||||||
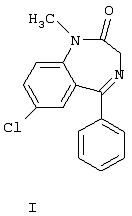
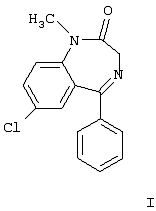
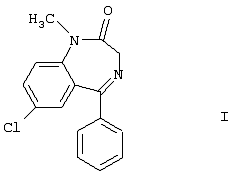
(54) ВЫСОКОМЕЧЕННЫЙ ТРИТИЕМ [3H]-7-ХЛОРО-1,3-ДИГИДРО-1-МЕТИЛ-5-ФЕНИЛ-2H-1,4- БЕНЗДИАЗЕПИН-2-ОН И СПОСОБ ЕГО ПОЛУЧЕНИЯ
(57) Реферат:
Изобретение относится к органической химии и может найти применение в биологии и медицине. Описывается высокомеченный тритием [3Н]-7-хлоро-1,3-дигидро-1-метил-5-фенил-2Н-1,4-бенздиазепин-2-он формулы I: Также описываются способы получения высокомеченного тритием [3Н]-7-хлоро-1,3-дигидро-1-метил-5-фенил-2Н-1,4-бенздиазепин-2-она. Технический результат – получен высокомеченный тритием аналог диазепама, который можно использовать при проведении медико-биологических исследований. 2 н. и 3 з.п. ф-лы.
Изобретение относится к органической химии и может найти применение в биологии и медицине. Известен 7-хлоро-1,3-дигидро-1-метил-5-фенил-2Н-1,4-бенздиазепин-2-он формулы I Данное соединение, получившее наименование “диазепам”, является одним из эффективных представителей транквилизаторов (R.F. Squires, С.Braestrup, Nature 266, 732 (1977). A.MacDonald et al., Anal. Profiles Drug Subs. 1, 79-99 (1972). M.Mandelli et al., Clin. Pharmacokinet. 3, 72 (1978)) [1]. Известно, что при введении метки в химические соединения их физиологическая активность не изменяется (Evans Е.А. – Tritium and its compounds London Butterworths, 1974, p.48) [2], а при проведении медико-биологических исследований необходимы меченые аналоги изучаемых физиологически активных соединений. В технической и патентной литературе не описан высокомеченный тритием аналог соединения формулы I и способ его получения. Техническим результатом, достигаемым настоящим изобретением, является получение высокомеченного тритием аналога диазепама (соединение формулы I). Указанный технический результат достигается тем, что получен высокомеченный тритием [3H]-7-хлоро-1,3-дигидро-1-метил-5-фенил-2Н-1,4-бенздиазепин-2-он формулы I Достигается указанный технический результат также тем, что способ получения высокомеченного тритием [3H]-7-хлоро-1,3-дигидро-1-метил-5-фенил-2Н-1,4-бенздиазепин-2-она заключается в нанесении его немеченого аналога на волокнистый углерод с последующим нагреванием в атмосфере газообразного трития в присутствии катализатора 5% PdO/BaSO4 при 140-160°С в течение 15-25 мин. Рекомендуется волокнистый углерод и катализатор 5% PdO/BaSO4 использовать в соотношении 1:1. Указанный технический результат достигается также тем, что способ получения высокомеченного тритием [3H]-7-xлopo-1,3-дигидро-1-метил-5-фенил-2Н-1,4-бенздиазепин-2-она заключается в нагревании его немеченого аналога в атмосфере газообразного трития в присутствии смеси катализатора 5% Pd/BaSO4 и RhCl3 при температуре 140-190°С в течение 5-20 мин. Рекомендуется катализатор 5% Pd/BaSO4 и RhCl3 использовать в соотношении 10:(0,5-2,5). Анализ и очистку меченого диазепама проводили тонкослойной (ТСХ) и высокоэффективной жидкостной (ВЭЖХ) хроматографией. TCX(Sorbfil)-гексан-изо-пропанол (4:1), Rf=0,74; гексан-изо-пропанол (22:3), Rf=0,66. ВЭЖХ диазепама проводили на колонке Kromasil 100 C18, 5 мкм, 8х150 мм, в системе метанол – 0,05% трифторуксусная кислота (65:35), скорость элюента – 2,0 мл/мин, время удерживания – 7,41 мин; на колонке Kromasil 100 C18, 5 мкм, 4×150 мм, в системе метанол – 50 мМ фосфатный буфер (рН 2,8) (65:35), скорость элюента – 1,0 мл/мин, время удерживания – 8,81 мин; на колонке Diasorb C8T, 7 мкм, 4×150 мм, в системе метанол – 50 мМ фосфатный буфер (рН 2,8) (1:3), скорость элюента – 1.0 мл/мин, время удерживания – 10,93 мин, в системе метанол – 50 мМ фосфатный буфер (рН 2,8) (11:19), скорость элюента – 1,0 мл/мин, время удерживания – 10,07 мин. Для приема и обработки хроматографических данных использован программно-аппаратный комплекс “МультиХром” (ЗАО “Амперсенд”, Россия) на базе IBM PC/AT. Радиоактивность измеряли на сцинтилляционном счетчике с эффективностью регистрации трития 30% в диоксановом сцинтилляторе. Ниже приведены примеры, иллюстрирующие изобретение. Пример 1. В реакционную ампулу помещали 5 мг немеченого диазепама, нанесенного на 50 мг волокнистого углерода, 50 мг катализатора 5% PdO/BaSO4, 0,5 мл гексана. Растворитель упаривали на роторе и осадок лиофилизировали. Затем ампулу вакуумировали до давления 0,1 Па, заполняли ее газообразным тритием до давления 333 гПа, нагревали до 160°С и выдерживали при этой температуре 15 мин. Избыточный тритий удаляли вакуумированием. После охлаждения продукты реакции растворяли в метаноле (6×1 мл), катализатор отфильтровывали, а фильтраты упаривали несколько раз в виде раствора в метаноле (3×3 мл) для удаления лабильного трития. Остаток очищали методом ВЭЖХ с выделением целевого продукта. В реакционной смеси содержалось 26% метки в диазепаме, радиохимическая чистота – около 28%. Выход меченого диазепама – 4%, молярная радиоактивность – 0,63 ПБк/моль, радиохимическая чистота – 98-99%. Пример 2. По методике примера 1 получили высокомеченный тритием диазепам. Нагревание исходного немеченого аналога в атмосфере газообразного трития осуществляли при температуре 140°С 25 мин. Выход меченого диазепама – 10%, молярная радиоактивность – 0,34 ПБк/моль, радиохимическая чистота – 98-99%. Пример 3. Приготовили смесь – 100 мг 5% Pd/BaSO4 и 0,1 мл водного раствора RhCl3 (100 мг/мл). К смеси добавили метанол до образования сметаноподобной массы, упарили на роторном испарителе и лиофилизировали. Сухой остаток тщательно растирали шпателем и обрабатывали 0,1 мл хлороформенного раствора диазепама (50 мг/мл). К смеси добавили хлороформ до образования сметаноподобной массы, упарили на роторном испарителе и лиофилизировали. В реакционную ампулу поместили 60 мг приготовленной смеси катализатора и немеченого диазепама. Затем ампулу вакуумировали до давления 0,1 Па, заполнили газообразным тритием до давления 333 гПа и выдержали при температуре 190°С 5 мин. Избыточный тритий удалили вакуумированием. После охлаждения продукты реакции растворили в метаноле (6×1 мл), катализатор отфильтровали, а фильтраты упарили несколько раз в виде раствора в метаноле (3×3 мл) для удаления лабильного трития. Остаток очистили методом ВЭЖХ. В реакционной смеси содержалось 6% метки в диазепаме, радиохимическая чистота – около 43%. Выход меченого диазепама – 4-5%, молярная радиоактивность – 1,56 ПБк/моль, радиохимическая чистота – 98-99%. Пример 4. По методике примера 3 получили высокомеченный тритием диазепам. Использовали смесь катализатора 5% Pd/BaSO4 и RhCl3, взятых в соотношении 10:0,5. Нагревание немеченого диазепама в атмосфере газообразного трития выполняли при температуре 140°С в течение 20 мин. Выход меченого диазепама – 40%, молярная радиоактивность – 0,33 ПБк/моль, радиохимическая чистота – 98-99%. Пример 5. По методике примера 3 получили высокомеченный тритием диазепам. Использовали смесь катализатора 5% Pd/BaSO4 и RhCl3, взятых в соотношении 10:2,5, Нагревание немеченого аналога диазепама в атмосфере газообразного трития выполняли при температуре 160°С в течение 15 мин. Выход меченого диазепама – 38%, молярная радиоактивность – 0,97 ПБк/моль, радиохимическая чистота – 98-99%. Таким образом, вариантами способа согласно изобретению получен высокомеченный тритием диазепам.
Формула изобретения
1. Высокомеченный тритием [3Н]-7-хлоро-1,3-дигидро-1-метил-5-фенил-2Н-1,4-бенздиазепин-2-он формулы I 2. Способ получения высокомеченного тритием [3H]-7-хлоро-1,3-дигидро-1-метил-5-фенил-2Н-1,4-бенздиазепин-2-она, заключающийся в нанесении его немеченого аналога на волокнистый углерод с последующим нагреванием в атмосфере газообразного трития в присутствии катализатора 5% PdO/BaSO4 при 140-160°С в течение 15-25 мин. 3. Способ по п.2, отличающийся тем, что волокнистый углерод и катализатор 5% PdO/BaSO4 используют в отношении 1:1. 4. Способ получения высокомеченного тритием [3Н]-7-хлоро-1,3-дигидро-1-метил-5-фенил-2Н-1,4-бенздиазепин-2-она, заключающийся в нагревании его немеченого аналога в атмосфере газообразного трития в присутствии смеси катализатора 5% Pd/BaSO4 и RhCl3 при температуре 140-190°С в течение 5-20 мин. 5. Способ по п.4, отличающийся тем, что катализатор 5% Pd/BaSO4 и RhCl3 используют в отношении 10:(0,5-2,5).
|
||||||||||||||||||||||||||