Патент на изобретение №2244716
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ НАТРИЕВОЙ СОЛИ 7-(1-Н-ТЕТРАЗОЛ-1-ИЛ)-АЦЕТАМИДО-3-(2-МЕТИЛ-1,3,4-ТИАДИАЗОЛ-5-ИЛ)ТИОМЕТИЛ)- 3-ЦЕФЕМ-4-КАРБОНОВОЙ КИСЛОТЫ(ЦЕФАЗОЛИНА)
(57) Реферат:
Изобретение относится к способу получения высокоэффективного антибиотика цефалоспоринового ряда – натриевой соли 7-(1-Н-тетразол-1-ил)-ацетамидо-3-(2-метил-1,3,4-тиадиазол-5-ил)тиометил)-3-цефем-4-карбоновой кислоты (цефазолина), пригодного для приготовления инъекционных растворов. Способ осуществляется путем кристаллизации цефазолина из водных или водно-органических растворов при введении в раствор хлорида или ацетата натрия в количестве 10-25% от веса воды в растворе, фильтрации выделившейся в осадок натриевой соли цефазолина, промывки осадка и сушки. Заявленный способ обеспечивает получение продукта, удовлетворяющего требованиям соответствующей фармакопейной статьи РФ с выходом 85,1-93,0%. 1 табл.
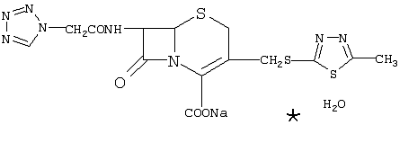
Предлагаемое изобретение относится к получению высокоэффективного антибиотика цефалоспоринового ряда – натриевой соли 7-(1-Н-тетразол-1-ил)-ацетамидо-3-(2-метил-1,3,4-тиадиазол-5-ил)тиометил)-3-цефем-4-карбоновой кислоты (цефазолина), соответствующей формуле Имеющие практическое применение способы получения цефазолина включают синтез 7-(1-Н-тетразол-1-ил)-ацетамидо-3-(2-метил-1,3,4-тиадиазол-5-ил)тиометил)-3-цефем-4-карбоновой кислоты взаимодействием 7-амино-3-(2-метил-1,3,4-тиадиазол-5-ил)тиометил)-3-цефем-4-карбоновой кислоты с 1-Н-тетразол-1-ацетилхлоридом в неводной среде с последующим выделением полученного соединения из реакционной массы в форме кислоты, из которой различными методами получают целевой продукт [US-PS 3954745; US-PS 3516997; US-PS 3502655]. Известны способы получения натриевой соли цефазолина растворением цефазолина в форме кислоты в водном щелочном растворе, стерилизующей фильтрацией полученного раствора, его охлаждением до температуры от минус 10 до минус 55°С и сублимацией растворителя при глубоком вакууме (остаточное давление в системе не должно превышать 1 мм рт. ст.) [DE 2614668; GB 1565267; ЕР 636623; US 4002748]. Перечисленные способы обеспечивают получение стерильной кристаллической натриевой соли цефазолина, пригодной для приготовления инъекционных растворов. Однако промышленное использование способов получения цефазолина методом лиофилизации требует значительных затрат на его реализацию и связано с необходимостью решения ряда существенных трудностей, главными из которых являются: – необходимость создания глубокого вакуума в процессе сублимации растворителя из раствора натриевой соли цефазолина, – необходимость поддержания специального температурно-временного режима, обеспечивающего удовлетворительную скорость сублимации растворителя, исключающего процесс плавления реакционной массы и обеспечивающего получение желательной кристаллической структуры продукта. Наиболее близким заявляемому способу по технической сущности и достигаемому результату является способ получения натриевой соли цефазолина из цефазолина в форме кислоты растворением последней в воде при добавлении к реакционной массе эквимолекулярного количества едкого натра, добавлением в полученный раствор органического растворителя (этилового или бутилового спирта), отгонкой части растворителя под вакуумом и кристаллизацией целевого продукта из кубового остатка [DE 3911321, C 07 D 501/36, опубл. 11.10.90]. Способ по патенту DE 3911321 обеспечивает получение натриевой соли цефазолина с выходом от 80 до 95% от теории. Существенными недостатками способа по патенту DE 3911321 являются необходимость применения больших объемов органического растворителя (водный раствор натриевой соли цефазолина разводится этанолом в соотношении 1:1 или бутанолом в соотношении 1:2), возможность разрушения целевого продукта в процессе отгонки растворителя, в особенности, при недостаточно глубоком вакууме, возможность загрязнения цефазолина продуктами, образовавшимися при гидролизе цефазолина в процессе отгонки растворителя. Заявляемый способ направлен на снижение затрат органических растворителей и упрощение технологического процесса в производстве натриевой соли 7-(1-Н-тетразол-1-ил)-ацетамидо-3-(2-метил-1,3,4-тиадиазол-5-ил)тиометил)-3-цефем-4-карбоновой кислоты (цефазолина). Поставленная задача достигается проведением процесса получения натриевой соли 7-(1-Н-тетразол-1-ил)-ацетамидо-3-(2-метил-1,3,4-тиадиазол-5-ил)тиометил)-3-цефем-4-карбоновой кислоты путем ее кристаллизации из водных или водно-органических растворов при введении в раствор хлорида или ацетата натрия в количестве 10-25% от веса воды в растворе, фильтрации выделившейся в осадок натриевой соли цефазолина, промывки осадка и сушки. Отличительными признаками заявляемого способа являются: – проведение процесса кристаллизации в водной или водно-органической среде в присутствии хлорида или ацетата натрия, – количество введенного в раствор хлорида или ацетата натрия, равное 10-25% от веса воды в растворе. Совокупность перечисленных выше отличительных признаков обеспечивают достижение положительного результата в заявленном способе: процесс кристаллизации натриевой соли цефазолина осуществляется без применения отгонки растворителя из реакционной массы при атмосферном давлении. Положительный результат в заявленном способе достигается за счет следующих выявленных в процессе разработки особенностей кристаллизации натриевой соли цефазолина: – Равновесная растворимость натриевой соли цефазолина в водных растворах вспомогательного электролита резко снижается при превышении концентрации хлорида натрия 9,0% (10% от веса воды в растворе) и при превышении концентрации ацетата натрия 15%. – Кристаллизация натриевой соли цефазолина из водных растворов хлорида или ацетата натрия происходит при комнатной температуре в форме моногидрата. Скорость и размеры кристаллов зависят от степени пересыщения раствора (соотношения концентраций натриевой соли цефазолина в растворе к равновесной концентрации). Проведение процесса кристаллизации во временном режиме согласно приведенным ниже примерам обеспечивает получение кристаллической структуры осадка натриевой соли цефазолина. – Верхний предел концентрации хлорида или ацетата натрия, вводимого в раствор натриевой соли цефазолина (25% от веса воды в растворе) обеспечивает возможность полного удаления электролита из выделившегося в осадок продукта в процессе его фильтрации и промывки. Использование других электролитов для высаливания натриевой соли цефазолина, например, сульфата натрия не обеспечивает получение свободного от постороннего электролита продукта, а применение органических электролитов, например, 2-этилгексаноата натрия существенно увеличивает стоимость сырьевых затрат на проведение процесса. При превышении концентрации вводимого в раствор электролита величины 25% от веса воды возможно загрязнение продукта хлоридом или ацетатом натрия. Пример 1. В круглодонную колбу вместимостью 250 мл загружают 150 мл пригодной для приготовления инъекционных растворов воды и 50,0 г цефазолина в форме кислоты, отвечающего требованиям USP 24-NF, содержащего 96,4% основного вещества (0,106 моль). При включенной мешалке и температуре 10-15°С из капельной воронки в суспензию загружают 17,5 мл 20% раствора NaOH до полного растворения осадка. Полученный раствор фильтруют через фильтр для стерилизующей фильтрации с размером пор 0,22 мкм и принимают в стерильную колбу вместимостью 500 мл. В условиях, обеспечивающих сохранение стерильности реакционной массы, при включенной мешалке при температуре около 20°С через капельную воронку вводят 86,0 мл (98,3 г, 25 г в пересчете на 100% вещество) 26% стерильного раствора хлорида натрия. Количество вводимого в раствор хлорида натрия составляет 14,8% от веса воды в растворе натриевой соли цефазолина. Скорость введения раствора хлорида натрия должна находиться в пределах 20-30 мл/час. После появления осадка в реакционной массе, что наблюдается после загрузки 40-50% расчетного количества раствора хлорида натрия, подачу раствора NaСl прекращают и дают выдержку при перемешивании в течение 20-30 минут. В течение этого времени происходит формирование кристаллов натриевой соли цефазолина. Затем в образовавшуюся суспензию продолжают подачу раствора хлорида натрия со скоростью 30-40 мл/час. После введения всего расчетного объема раствора хлорида натрия реакционную массу перемешивают 30-40 минут и, соблюдая требования к поддержанию стерильности реакционной массы, осадок фильтруют, промывают на фильтре 30-50 мл бутилового спирта и сушат под вакуумом при температуре не выше 50°С. Получают 48,4 г стерильной кристаллической натриевой соли цефазолина с содержанием основного вещества 94,2% (в пересчете на безводный продукт). Содержание воды в продукте составляет 5,4%. Выход продукта составляет 90,3% от теории в пересчете на загруженный цефазолин в форме кислоты. Пример 2 Получают раствор натриевой соли из 50,0 г цефазолина в условиях примера 1. В условиях, обеспечивающих сохранение стерильности реакционной массы, при включенной мешалке при температуре около 20°С через капельную воронку вводят 98,0 мл (112,6 г, 33,78 г в пересчете на 100% вещество) 30% стерильного раствора ацетата натрия. Количество вводимого в раствор ацетата натрия составляет 20,0% от веса воды в растворе натриевой соли цефазолина. Скорость введения раствора хлорида натрия должна находиться в пределах 20-30 мл/час. После появления осадка в реакционной массе, что наблюдается после загрузки 30-40% расчетного количества раствора ацетата натрия, подачу раствора NaCH3COO прекращают и дают выдержку при перемешивании в течение 20-30 минут. В течение этого времени происходит формирование кристаллов натриевой соли цефазолина. Затем в образовавшуюся суспензию продолжают подачу раствора ацетата натрия со скоростью 40-50 мл/час. Дальнейшую операцию получения натриевой соли цефазолина осуществляют в соответствии с описанием примера 1. Получают 49,17 г стерильной кристаллической натриевой соли цефазолина с содержанием основного вещества 94,5% (в пересчете на безводный продукт). Содержание воды в продукте составляет 5,1%. Выход продукта составляет 92,0% от теории в пересчете на загруженный цефазолин в форме кислоты. Пример 3. Процесс ведут в соответствии с описанием примера 1. В раствор натриевой соли цефазолина вводят 58,4 мл (65,4 г, 17,0 г в пересчете на 100% вещество) 26% стерильного раствора хлорида натрия. Количество вводимого в раствор хлорида натрия составляет 10,0% от веса воды в растворе натриевой соли цефазолина. Получают 46,58 г стерильной кристаллической натриевой соли цефазолина с содержанием основного вещества 94,0% (в пересчете на безводный продукт). Содержание воды в продукте составляет 5,7%. Выход продукта составляет 86,70% от теории в пересчете на загруженный цефазолин в форме кислоты. Пример 4 Процесс ведут в соответствии с описанием примера 2. В раствор натриевой соли цефазолина вводят 122,5 мл (140,8 г, 42,25 г в пересчете на 100% вещество) 30% стерильного раствора ацетата натрия. Количество вводимого в раствор ацетата натрия составляет 25,0% от веса воды в растворе натриевой соли цефазолина. Получают 49,5 г стерильной кристаллической натриевой соли цефазолина с содержанием основного вещества 91,2% (в пересчете на безводный продукт). Содержание воды в продукте составляет 5,4%. Выход продукта составляет 89,3% от теории в пересчете на загруженный цефазолин в форме кислоты. Пример 5 В круглодонную колбу вместимостью 250 мл загружают 150 мл пригодной для приготовления инъекционных растворов воды, 30 мл ацетона и 50,0 г цефазолина в форме кислоты с содержанием основного вещества 87,5% (0,0962 моль). При включенной мешалке и температуре 10-15°С из капельной воронки в суспензию загружают 15,9 мл 20% раствора NaOH до полного растворения осадка. Полученный раствор обрабатывают 0,5 г активированного угля и фильтруют последовательно через бумажный фильтр и фильтр для стерилизующей фильтрации с размером пор 0,22 мк. Раствор принимают в стерильную колбу вместимостью 500 мл. В дальнейшем процесс ведут в соответствии с описанием примера 1. Получают 42,3 г стерильной кристаллической натриевой соли цефазолина с содержанием основного вещества 92,2% (в пересчете на безводный продукт). Содержание воды в продукте составляет 5,8%. Выход продукта составляет 85,1% от теории в пересчете на загруженный цефазолин в форме кислоты. Пример 6 В круглодонную колбу вместимостью 250 мл загружают 150 мл пригодной для приготовления инъекционных растворов воды, 25 мл изопропилового спирта и 50,0 г цефазолина в форме кислоты с содержанием основного вещества 87,5% (0,0962 моль). В дальнейшем процесс ведут в соответствии с описанием примера 5. Получают 43,4 г стерильной кристаллической натриевой соли цефазолина с содержанием основного вещества 93,0% (в пересчете на безводный продукт). Содержание воды в продукте составляет 5,1%. Выход продукта составляет 88,05% от теории в пересчете на загруженный цефазолин в форме кислоты. Примеры с запредельными параметрами Процесс получения натриевой соли цефазолина в примерах 7-9 ведут в соответствии с описанием, приведенным в примере 1, но с количеством вводимого в реакционную массу хлорида или ацетата натрия, выходящим за пределы, приведенные в формуле предлагаемого изобретения. Результаты приведены в таблице.
Формула изобретения
Способ получения натриевой соли 7-(1-Н-тетразол-1-ил)-ацетамидо-3-(2-метил-1,3,4-тиадиазол-5-ил)тиометил-3-цефем-4-карбоновой кислоты (цефазолина) кристаллизацией ее из водных или водно-органических растворов, фильтрацией, промывкой и сушкой осадка, отличающийся тем, что кристаллизацию целевого продукта осуществляют путем введения в раствор хлорида или ацетата натрия в количестве 10-25% от веса воды в растворе.
PC4A – Регистрация договора об уступке патента Российской Федерации на изобретение
(73) Патентообладатель(и):
(73) Патентообладатель:
Дата и номер государственной регистрации перехода исключительного права: 22.09.2006 № РД0012392
Извещение опубликовано: 10.11.2006 БИ: 31/2006
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 28.06.2007
Извещение опубликовано: 20.02.2009 БИ: 05/2009
TK4A Исправление очевидных и технических ошибок в публикациях сведений об изобретениях в
Номер и год публикации бюллетеня: 5-2009
Код раздела бюллетеня: MM4A
Опубликовано: Дата прекращения действия патента: 28.06.2007
Следует читать: Дата прекращения действия патента: 28.06.2008
Дата публикации: 10.01.2011
|
||||||||||||||||||||||||||