Патент на изобретение №2242479
|
||||||||||||||||||||||||||
(54) СОЕДИНЕНИЯ, НАБОР, АНДРОГЕННАЯ КОМПОЗИЦИЯ
(57) Реферат:
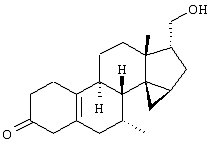
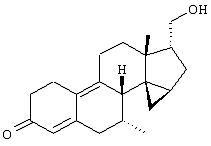
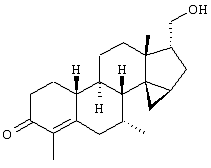
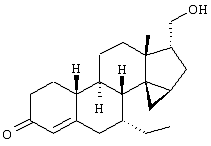
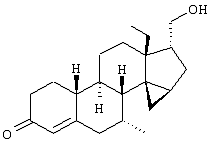
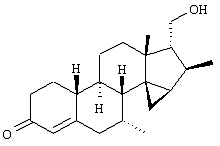
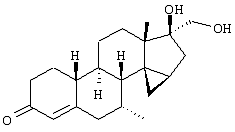
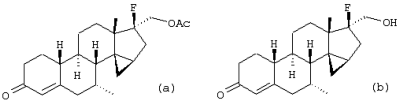
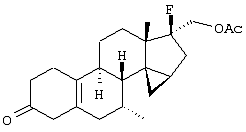
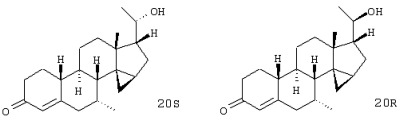
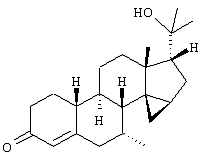
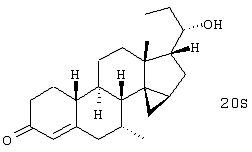
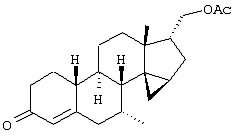
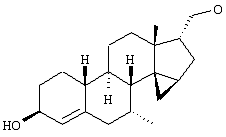
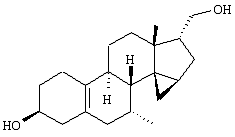
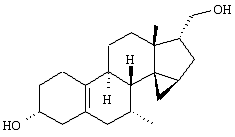
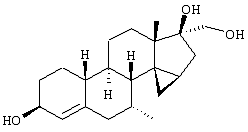
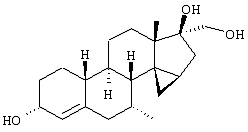
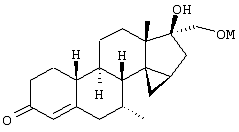
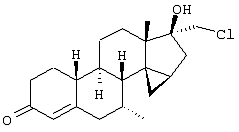
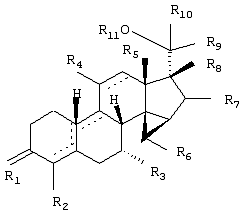
Изобретение относится к стероидам общей формулы I где R1 – О, (Н,Н), (H,OR), NOR, где R – H, С1-6алкил, С1-6ацил; R2 – H или С1-6алкил, R3 – H, или R3 – С1-6алкил, С2-6алкенил, С2-6алкинил, возможно замещенный галогеном, R4 – H, C1-6алкил или С2-6алкенил; R5 – C1-6 алкил, R5 – H, R7 – H, C1-6алкил, R8 – H, OH, галоген; R9 и R10, независимо H или R9 и R10 независимо C1-6алкил, возможно замещенный C1-4алкокси или галогеном; R11 – H, SO3H, С1-15ацил, пунктир означает возможную связь из
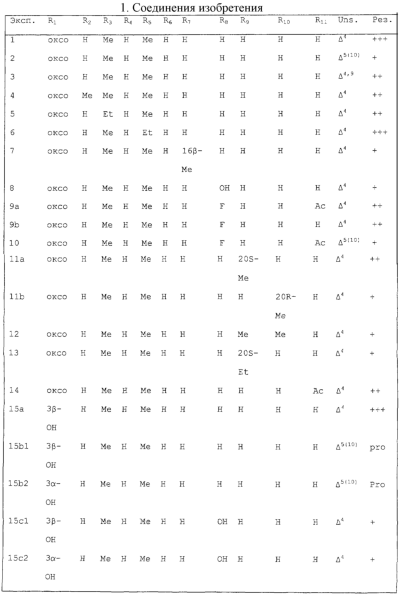
Настоящее изобретение относится к области стероидных соединений, имеющих кольцо циклопропана, которое включает атомы углерода 14 и 15 стероидного скелета. Более конкретно, изобретение относится к таким стероидным соединениям, которые обладают андрогенной активностью. Стероиды, имеющие вышеуказанное кольцо циклопропана, были описаны в Европейском патенте 768316, который относится к области женской контрацепции и гормональной терапии против эндометриоза или климактерических жалоб. Стероиды описываются, как обладающие прогестагенной активностью, примерами являются 14 В заявке на патент PCT/DE99/01795 (опубликована 29 декабря 1999 как WO 99/67276) была описана группа 14,15-циклопропилстероидов, среди которых имеются 17 Другой заявкой на патент является WO 00/53619, в которой описана группа андрогенных стероидов, которые имеют 14 Настоящее изобретение охватывает новую группу стероидов общего типа, как указано выше, которые обладают неожиданной андрогенной активностью. В отличие от прогестагенов, описанных в известной области техники, андрогены настоящего изобретения, включая очень сильнодействующие андрогены, между прочим, удовлетворяют требованиям, чтобы кольцо циклопропана было Стероиды согласно изобретению соответствуют структурной формуле I: где R1 представляет О, (Н,Н), (H,OR), NOR, причем R представляет водород, (С1-6)алкил, (С1-6)ацил; R2 представляет водород или (С1-6)алкил; R3 представляет водород или R3 представляет (С1-6)алкил, (С2-6)алкенил или (С2-6)алкинил, каждый из которых, необязательно, замещен галогеном; R4 представляет водород, (С1-6)алкил или (С2-6)алкенил; R5 представляет (С1-6)алкил; R6 представляет водород, галоген или (C1-4)алкил; R7 представляет водород или (С1-6)алкил; R8 представляет водород, гидрокси, (C1-6)алкокси, галоген или (C1-6)алкил; R9 и R10, независимо, представляют водород или R9 и R10, независимо, представляют (C1-6)алкил, (С2-6)алкенил, (С3-6)циклоалкил, (С5-6)циклоалкенил или (С2-6)алкинил, каждый из которых, необязательно, замещен (C1-4)алкокси или галогеном; R11 представляет водород, SО3Н, (C1-15)aцил и пунктирные линии обозначают необязательные связи, выбранные из Изобретение относится не только к стероидам, которые соответствуют структурной формуле I, но также к их фармацевтически приемлемым солям или эфирам, пролекарствам и предшественникам. Термин (C1-6)алкил, используемый в определении формулы I, означает разветвленную или неразветвленную алкильную группу, имеющую 1-6 атомов углерода, подобную метилу, этилу, пропилу, изопропилу, бутилу, изобутилу, третичному бутилу, пентилу и гексилу. Таким же образом термин (C1-4)алкил означает алкильную группу, имеющую 1-4 атомов углерода. Предпочтительные алкильные группы имеют 1-4 атома углерода, и очень предпочтительными алкильными группами являются метил и этил. Термин (С2-6)алкенил означает разветвленную или неразветвленную алкенильную группу, имеющую, по меньшей мере, одну двойную связь и 2-6 атомов углерода. Предпочтительные алкенильные группы имеют 2-4 атома углерода, такие как винил и пропенил. Термин (С2-6)алкинил означает разветвленную или неразветвленную алкинильную группу, имеющую, по меньшей мере, одну тройную связь и 2-6 атомов углерода. Предпочтительные алкинильные группы имеют 2-4 атома углерода, такие как этинил и пропинил. Термин (С3-6)циклоалкил означает кольцо циклоалкана, имеющее 3-6 атомов углерода, подобное циклопропану, циклобутану, циклопентану и циклогексану. Термин (С5-6)циклоалкенил означает кольцо циклоалкена, имеющее, по меньшей мере, одну двойную связь и 5 или 6 атомов углерода. Термин (C1-6)алкокси означает разветвленную или неразветвленную алкилоксигруппу, имеющую 1-6 атомов углерода, подобную метилокси, этилокси, пропилокси, изопропилокси, бутилокси, изобутилокси, третичный бутилокси, пентилокси и гексилокси. Подобным же образом термин (C1-4)алкокси означает разветвленную или неразветвленную алкилоксигруппу, имеющую 1-4 атома углерода. Предпочтительные алкилоксигруппы имеют 1-4 атома углерода, и очень предпочтительной является метилокси. Термин (С1-6)ацил означает ацильную группу, образованную из карбоновой кислоты, имеющей 1-6 атомов углерода, подобную формилу, ацетилу, пропаноилу, бутирилу, 2-метилпропаноилу, пентаноилу, пивалоилу и гексаноилу. Подобным же образом термин (С1-15)ацил означает ацильную группу, образованную из карбоновой кислоты, имеющей 1-15 атомов углерода. В определение (С1-6)ацила или (С1-15)ацила включены также ацильные группы, образованные из дикарбоновых кислот, подобные гемималоилу, гемисукциноилу, гемиглутароилу и т.д. Термин галоген означает фтор, хлор, бром или иод. Когда галоген представляет собой заместитель у алкильной группы, как в определении R3, R6, R8, R9 И R10, предпочтительными галогенами являются С1 и F, причем очень предпочтительным является F. Производные 14 Для терапевтического использования соли соединений формулы I являются солями, в которых противоион является фармацевтически приемлемым. Однако соли кислот в соответствии с формулой I могут также найти использование, например, при получении или очистке фармацевтически приемлемого соединения. Все соли, независимо от того, являются ли они фармацевтически приемлемыми или нет, включены в пределы настоящего изобретения. Примеры солей кислот в соответствии с изобретением являются минеральными солями, такими как соль натрия, соль калия и соли, образованные органическими основаниями, подобными аммиаку, имидазолу, этилендиамину, триэтиламину и тому подобное. Соединения в соответствии с изобретением, как описано здесь выше, обладают неожиданной андрогенной активностью. Андрогенную активность можно измерить различными путями. Так, эффективность андрогенов можно определить in vitro с использованием цитоплазмического рецептора андрогенов из клеток опухоли грудной железы человека (клеточная линия MCF-7); см. Bergink, E.W. et al., “Сравнение связывающих рецепторы свойств нандролона и тестостерона в условиях in vitro и in vivo”, J. Steroid Biochem. 22, 831-836 (1985). Можно также использовать клетки яичника китайского хомячка (СНО), трансфекцированные рецептором андрогенов человека (время инкубации 16 ч, температура 4° С) и сравненные со сродством 5 Предпочтение отдается тем соединениям в соответствии с изобретением, которые проявляют относительно высокую андрогенную активность. Таким образом, предпочтительными соединениями изобретения являются соединения, которые соответствуют вышеуказанной формуле I, в которой R1 представляет оксо и пунктирные линии указывают В качестве андрогенных гормонов стероиды настоящего изобретения можно использовать, inter alia, в мужской контрацепции и мужской HRT (гормональная заместительная терапия). Так, например, мужская контрацепция может включать схему введения гормонов, в которой прогестаген служит для достижения контрацептивного действия и андроген служит для пополнения тестостерона, пониженный уровень которого наблюдается. Другой вариант состоит в том, что мужскую контрацепцию проводят только с андрогенным гормоном. Андрогены можно также использовать для пополнения андрогена у стареющей особи мужского пола с частичным дефицитом андрогена. Следующим за использованием андрогенов для особей мужского пола андрогены изобретения можно также использовать для особей женского пола, например, как андрогенную заместительную терапию у постклимактерических женщин или у детей с андрогенным дефицитом. Настоящее изобретение относится также к фармацевтической композиции, включающей стероидное соединение в соответствии с изобретением, смешанное с фармацевтически приемлемым вспомогательным средством, так, как описано в стандартной ссылке, Gennaro et al., Remmington Подходящие носители, с которыми можно вводить композиции, включают лактозу, крахмал, производные целлюлозы и тому подобное или их смеси, используемые в подходящих количествах. Кроме того, изобретение относится к использованию стероидного соединения в соответствии с изобретением для изготовления лекарственного средства, применяемого при лечении андрогенного дефицита, таком как мужская или женская HRT (гормональная заместительная терапия). В соответствии с этим изобретение включает также способ лечения в области мужской или женской HRT, включающий введение пациенту особи мужского или женского пола, страдающему андрогенным дефицитом, соединения, как описано здесь ранее (в подходящей фармацевтической дозированной форме). Кроме того, изобретение относится к использованию стероидного соединения в соответствии с изобретением для изготовления лекарственного средства, имеющего контрацептивную активность (для которого в данной области используют также термин “контрацептивный агент”). Таким образом, изобретение относится к медицинскому показанию контрацепции, т.е. способу контрацепции, включающему введение субъекту, являющемуся особью мужского пола, предпочтительно мужской особи человека, соединения, как описано здесь ранее (в подходящей фармацевтической дозированной форме) в комбинационной терапии с прогестагеном или без него. Андрогены в соответствии с изобретением можно также использовать в наборе для мужской контрацепции. Хотя данный набор может включать только один или несколько андрогенов, предпочтительно, чтобы он включал средство для введения прогестагена и средство для введения андрогена. Последним средством является фармацевтическая готовая препаративная форма, включающая соединение в соответствии с изобретением, как описано здесь выше, и фармацевтически приемлемый носитель. Изобретение относится также к способу лечения, включающему введение особи мужского или женского пола (особенно человеку), нуждающейся в андрогенном пополнении, терапевтически эффективного количества производного 14 Кроме того, изобретение относится к способу контрацепции, включающему введение фертильной особи мужского пола, особенно мужской особи человека, производного 14 Соединения изобретения можно получить различными способами, известными в области органической химии в общем и, особенно, в области химии стероидов (см., например: Fried, J. et al., “Organic Reactions in Steroid Chemistry”, Volumes I and II, Van Nostrand Reinhold Company, New York, 1972). Существенным является введение 14 Подходящим исходным веществом для получения соединений формулы I, где R1 представляет оксо; R2, R7, R8 и R11 представляют водород; R3 и R4 представляют водород или (С1-6)алкил; R5 представляет метил; R6, R9 и R10 имеют ранее приведенные значения, и пунктирные линии означают двойную связь Возможный путь синтеза соединений в соответствии с изобретением начинается с превращения соединений формулы II в Превращение 17-оксо в 17-(CH2OH) можно выполнить несколькими путями: (a) 1: Реакцией Виттига или Петерсона для производного 17-метиленэстра-1,3,5(10)-триена [Maercker, А., в “Оrg. Reactions” 14, р. 270, Wiley, New York, 1965; Аgеr, D.J., в “Оrg. Reactions”, 38, р. 1, Wiley, New York, 1990]; 2: гидроборированием, например, посредством использования 9-BBN, диизамилборана или гексилборана [см., например, Zweifel, G. et al., в “Оrg. Reactions” 13, р. 1, Wiley, New York, 1963], приводящим к образованию производного (17 (b) 1: Превращением 17-кетона в (17 (с ) 1: Превращением 17-кетона в 17-метиленсоединение; 2: эпоксидированием, например, пероксикислотой, такой как м-хлорпербензойная кислота, в (17 (d) Превращением 17-кетона в 17 (e) 1: Превращением 17-кетона в 17-цианостероид взаимодействием с тозилметилизоцианидом [TosMIC, см. Bull, J.R. et al., Tetrahedron 31, 2151 (1975)]; 2: восстановлением цианогруппы в формил диизобутилалюминийгидридом; 3: восстановлением 17-формильной группы в 17-(СН2OН). (f) 1: Конденсацией Виттига с участием (Ph)3Р=CНОМе; 2: гидролизом образовавшегося простого эфира енола; 3: восстановлением 17-формила в 17-(CH2OH). (g) 1: Превращением 17-кетона в 17 (h) 1: Превращением 17-кетона в соответствующий трифторметансульфонат енола [см., например, Cacchi, S. et al, Tetrahedron Lett. 25, 4821 (1984)]; 2: катализируемым палладием алкоксикарбонилированием последнего в алкилэстра-1,3,5(10),16-тетраен-17-карбоксилат [Cacchi, S. et al, Tetrahedron Lett. 26, 1109 (1985)]; 3: восстановлением последнего в соответствующее производное 17-метанола; 4: гидрированием двойной связи (i) 1: Превращением 17-кетона в алкилэстра-1,3,5(10),16-тетраен-17-карбоксилат, как описано в (h); 2: 1,4-восстановлением, например, гидрированием или восстановлением литием или натрием в жидком аммиаке, в производное алкилэстра-1,3,5(10)-триен-17-карбоксилата; 3: восстановлением эфира в 17-(СН2OН). Некоторые из указанных способов (например, b, с) приводят к стереоселективному образованию 17 Полученные таким образом производные (14 (14 (14 20-Кетон можно, необязательно, восстановить взаимодействием с LiAlH4, NaBH4 или другими восстанавливающими агентами. В данном случае получают 17-(CHR9OH)-производные с инвертированной стереохимией у С-20. Эпимеризацию у С-20 можно выполнить при помощи реакции Мицунобу (Mitsunobu) [Dodge, J.A. et al., Bioorg. and Med. Chem. Lett. 6, 1 (1996)] или обработкой метансульфонилхлоридом или п-толуолсульфонилхлоридом с последующим взаимодействием с кислородным нуклеофилом [например, супероксидом калия, см. Corey, E.J. et al., Tetrahedron Lett. 3183 (1975)]. Производное (14 Соединения формулы I с заместителями у С-3, С-4, С-7, С-11, С-13, С-1’, С-16 и С-17, другими, чем заместители, описываемые при определении формулы II, или соединения с R11, другим, чем водород, или соединения без двойных связей в стероидном кольце или с ненасыщенностями, другими, чем двойная связь Соединения изобретения, у которых R1 представляет (Н,Н), (H,OR), NOR и R представляет Н, (С1-6)алкил или (С1-6)ацил, можно получить из соединений формулы I, в которой R1 представляет оксо. Соединения, у которых R2 представляет (С1-6)алкил, получают из соединений формулы I, в которой R2 представляет водород. Соединения с заместителем R3, отличным от водорода, можно получить, например, из (7 Соединения с заместителями R4, отличными от водорода или (С1-6)алкил, можно получить, например, из циклического 1,2-этандиилацеталя (11 Соединения, у которых R5 представляет, например, этил, можно получить, например, из 13-этилгон-4-ен-3,17-диона [Brito, M. et al., Synth. Соmm. 26, 623 (1996)]. 16-Замещенные соединения можно получить посредством алкилирования у С16 производного (14 (17 Соединения изобретения, у которых R11 представляет SО3Н или (С1-15)ацил, получают из соединений формулы I, в которой R11 представляет водород. Соединения в соответствии с изобретением, не содержащие ненасыщенных связей в стероидном кольце, получают из Соединения изобретения, имеющие двойную связь Соединения, имеющие двойную связь Изобретение будет дополнительно объясняться в дальнейшем со ссылкой на следующие примеры. Пример 1 (7 i) Раствор (7 ii) Раствор продукта, полученного на предыдущей стадии (6,50 г), в ацетоне (325 мл) охлаждают до 5° С, обрабатывают реагентом Джонса (8 М, 11,9 мл). После 15 мин перемешивания при 5-10° С добавляют 2-пропанол и смесь фильтруют. Фильтрат концентрируют; добавляют воду и продукт экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, получая при этом (7 iii) трет-Бутоксид калия (6,1 г) порциями добавляют к раствору продукта, полученного на предыдущей стадии (3,81 г), в смеси безводного тетрагидрофурана (26 мл) и безводного диметилсульфоксида (65 мл), содержащего иодид триметилсульфония (8,4 г). Реакционную смесь перемешивают при комнатной температуре в течение 3 ч и затем выливают в водный раствор хлорида аммония. Продукт экстрагируют этилацетатом; объединенные органические фазы промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, получая при этом (7 iv) Раствор продукта, полученного в предыдущей стадии (3,76 г), в 1,4-диоксане (113 мл) обрабатывают водным раствором перхлорной кислоты (70%, 1,80 мл). Реакционную смесь перемешивают при комнатной температуре в течение 2 ч и затем обрабатывают другой порцией перхлорной кислоты (0,36 мл). Смесь перемешивают в течение еще 2 ч и затем выливают в насыщенный водный раствор гидрокарбоната натрия. Продукт экстрагируют этилацетатом; объединенные органические фазы промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, получая при этом (7 v) Раствор продукта, полученного на предыдущей стадии (3,7 г), в безводном тетрагидрофуране (24 мл) добавляют по каплям к охлажденной льдом суспензии литийалюминийгидрида (1,90 г) в тетрагидрофуране (24 мл). После перемешивания 1 ч реакционную смесь гасят добавлением насыщенного водного раствора сульфата натрия. Добавляют этилацетат и смесь фильтруют через дикалит. Органическую фазу отделяют от водной фазы и промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Колоночная хроматография дает (7 vi) Продукт, полученный на предыдущей стадии (1,30 г), в безводном тетрагидрофуране (27 мл) добавляют к кипящему с обратным холодильником раствору лития (0,82 г) в жидком аммиаке (54 мл). Реакционную смесь перемешивают при температуре кипения флегмы в течение 45 мин. Добавляют трет-бутанол (2,7 мл) и смесь перемешивают в течение 30 мин. Добавляют этанол и дают испариться аммиаку. Добавляют воду и продукт экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным водным раствором хлорида аммония и насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, при этом получая (7 vii) Раствор продукта, полученного на предыдущей стадии (1,17 г), в ацетоне (23 мл) обрабатывают хлористоводородной кислотой (6 М, 2 мл). После перемешивания в течение 1 ч при комнатной температуре добавляют насыщенный водный раствор гидрокарбоната натрия и продукт экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Колоночная хроматография дает (7 Пример 2 (7 Раствор (7 Пример 3 (7 Бромид фенилтриметиламмония (1,01 г) добавляют к раствору (7 Пример 4 (7 i) Раствор (7 ii) Раствор продукта, полученного на предыдущей стадии (0,13 г), в ацетоне (4,8 мл) обрабатывают никелем Ренея (суспензия в этаноле, 0,5 мл) и смесь нагревают при температуре кипения флегмы в течение 45 мин. Смесь фильтруют и фильтрат концентрируют при пониженном давлении. Колоночная хроматография дает (7 Пример 5 (7 i) Хлортриметилсилан (19 мл) добавляют в течение 5 мин к суспензии (17 ii) Смесь лития (5,0 г) и безводного диэтилового эфира (200 мл) охлаждают до -30° С. По каплям добавляют бромэтан (26,9 мл), после чего образовавшийся раствор этиллития переносят в суспензию иодида меди(1) (30,6 г) в безводном тетрагидрофуране (140 мл), охлажденную до -30° С. Образовавшийся раствор купрата перемешивают в течение 45 мин при указанной температуре и по каплям добавляют раствор продукта, полученного на предыдущей стадии (20,0 г), в безводном тетрагидрофуране (160 мл). После 45 мин перемешивания при -25° С добавляют хлортриметилсилан (20 мл) и перемешивание продолжают в течение еще 30 мин. Реакционную смесь выливают в насыщенный водный раствор хлорида аммония и продукт экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным водным раствором хлорида аммония и насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, получая при этом (7 iii) Раствор продукта, полученного на предыдущей стадии (29,5 г), в ацетоне (400 мл) обрабатывают хлористоводородной кислотой (2,3 М, 20 мл). После перемешивания 1,5 ч при комнатной температуре реакционную смесь нейтрализуют насыщенным водным раствором гидрокарбоната натрия. Ацетон удаляют при пониженном давлении и продукт экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, получая при этом (7 iv) Хлористоводородную кислоту (6 М, 240 мл) добавляют по каплям к суспензии дикалита (240 г) в метаноле (1200 мл). После перемешивания 20 мин при комнатной температуре дикалит отфильтровывают и промывают водой до достижения нейтральности. Затем его суспендируют в воде (960 мл). При энергичном перемешивании добавляют тригидрат нитрата меди (II) (145 г) с последующим осторожным добавлением раствора карбоната натрия (72,2 г) в воде (360 мл). После перемешивания 30 мин продукт отфильтровывают и промывают водой до достижения нейтральности. Продукт сушат при 80° С при пониженном давлении, получая при этом карбонат меди(II) на дикалите (310 г). Смесь продукта, полученного в стадии iii (19,5 г), и карбоната меди (II) на дикалите (70 г) в толуоле (330 мл) нагревают при температуре кипения флегмы в течение 9 ч при удалении воды с использованием ловушки Дина-Старка. Реакционную смесь фильтруют, остаток тщательно промывают этилацетатом и фильтрат концентрируют при пониженном давлении. Колоночная хроматография дает (7 v) Раствор продукта, полученного на предыдущей стадии (9,14 г), бромида меди (II) (13,6 г) и бромид лития (2,64 г) в ацетонитриле (285 мл) перемешивают при комнатной температуре в течение 4 ч. Реакционную смесь выливают в воду и продукт экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным водным раствором хлорида аммония и насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Колоночная хроматография дает (7 vi) Смесь продукта, полученного в предыдущей стадии (6,54 г), безводного карбоната калия (18,6 г), иодметана (5,6 мл) и безводного диметилформамида (22 мл) перемешивают при комнатной температуре в течение 3,5 ч. Реакционную смесь выливают в воду и продукт экстрагируют этилацетатом. Объединенные органические фазы промывают водой, насыщенным водным раствором хлорида аммония и насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, получая при этом (7 vii) Раствор диизопропиламина (6,15 мл) в безводном тетрагидрофуране (70 мл) охлаждают до -30° С. По каплям добавляют н-BuLi (1,6 М раствор в гексанах, 27,5 мл) и перемешивание продолжают в течение 30 мин. Реакционную смесь охлаждают до -50° С и по каплям добавляют раствор продукта, полученного на предыдущей стадии (6,95 г), в безводном тетрагидрофуране (100 мл). Перемешивание продолжают в течение 1 ч. После охлаждения до -60° С добавляют хлортриметилсилан (11,1 мл). Смесь перемешивают в течение 20 мин и затем обрабатывают раствором трибромида фенилтриметиламмония (10,0 г) в безводном пиридине (31 мл). После перемешивания 1 ч при -60° С смесь выливают в воду и продукт экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным водным раствором гидрокарбоната натрия и насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Колоночная хроматография дает (7 viii) Смесь продукта, полученного на предыдущей стадии (8,75 г), бромида лития (12,7 г) и карбоната лития (10,9 г) в безводном диметилформамиде (77 мл) нагревают при кипении с обратным холодильником в течение 3,25 ч. После охлаждения реакционную смесь выливают в воду и продукт экстрагируют этилацетатом. Объединенные органические фазы промывают водой и насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Колоночная хроматография дает (7 ix) Раствор боргидрида натрия (0,21 г) и гидроксида натрия (0,44 г) в метаноле (50 мл) добавляют по каплям к раствору (7 х) Следуя процедуре, аналогичной процедуре, описываемой на стадии i примера 1, продукт, полученный на предыдущей стадии (24,27 г), превращают в (7 xi) Следуя процедуре, аналогичной процедуре, описываемой на стадии ii примера 1, продукт, полученный на предыдущей стадии (14,03 г), превращают в (7 xii) Следуя процедуре, аналогичной процедуре, описываемой на стадии iii примера 1, продукт, полученный на предыдущей стадии (6,80 г), превращают в (7 xiii) Следуя процедуре, аналогичной процедуре, описываемой на стадии iv примера 1, продукт, полученный на предыдущей стадии (7,24 г), превращают в (7 xiv) Следуя процедуре, аналогичной процедуре, описываемой на стадии v примера 1, продукт, полученный на предыдущей стадии (8,48 г), превращают в (7 xv) Следуя процедуре, аналогичной процедуре, описываемой на стадии vi примера 1, продукт, полученный на предыдущей стадии (1,23 г), превращают в (7 xvi) Следуя процедуре, аналогичной процедуре, описываемой на стадии vii примера 1, продукт, полученный на предыдущей стадии (1,19 г), превращают в (7 Пример 6 (7 i) Перрутенат тетрапропиламмония (1,3 г) добавляют к раствору (7 ii) К раствору продукта, полученного на предыдущей стадии (9,9 г), в смеси этиленгликоля (13,3 мл) и триэтилортоформиата (23,9 мл) добавляют п-толуолсульфоновую кислоту (0,41 г). Реакционную смесь перемешивают при комнатной температуре в течение 3 ч. Добавляют дополнительную порцию п-толуолсульфоновой кислоты (0,41 г) и перемешивание продолжают в течение 2 ч. Добавляют воду и перемешивание продолжают в течение еще 1 ч. Продукт экстрагируют этилацетатом; объединенные органические фазы промывают насыщенным водным раствором гидрокарбоната натрия и насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, получая при этом циклический 1,2-этандиилацеталь (7 iii) Трибромид фенилтриметиламмония (8,25 г) добавляют к раствору продукта, полученного на предыдущей стадии (9,80 г), в безводном тетрагидрофуране (55 мл). После перемешивания 1 ч добавляют дополнительную порцию трибромида фенилтриметиламмония (4,12 г) и перемешивание продолжают в течение дополнительного 1 ч. Реакционную смесь выливают в насыщенный водный раствор тиосульфата натрия. Продукт экстрагируют этилацетатом; объединенные органические фазы промывают водой и насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, получая при этом циклический 1,2-этандиилацеталь (7 iv) Раствор продукта, полученного на предыдущей стадии (14,5 г), в безводном диметилсульфоксиде (55 мл) обрабатывают трет-бутоксидом калия (12,4 г) и реакционную смесь перемешивают при комнатной температуре в течение 1,5 ч. Добавляют дополнительную порцию трет-бутоксида калия (12,4 г) и реакционную смесь перемешивают в течение еще 3 ч при 40° С. Смесь выливают в насыщенный водный раствор хлорида аммония и продукт экстрагируют этилацетатом. Объединенные органические фазы промывают водой и насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Колоночная хроматография дает циклический 1,2-этандиилацеталь (7 v) Раствор продукта, полученного на предыдущей стадии (6,3 г), в безводном толуоле (162 мл) обрабатывают п-толуолсульфонатом пиридиния (4,21 г) и нагревают при кипении с обратным холодильником в течение 1 ч. После охлаждения реакционную смесь выливают в насыщенный водный раствор гидрокарбоната натрия и продукт экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, получая при этом циклический 1,2-этандиилацеталь (7 vi) Раствор продукта, полученного на предыдущей стадии (6,5 г), в безводном толуоле (251 мл) обрабатывают п-толуолсульфоновой кислотой (3,5 г) и нагревают при кипении с обратным холодильником в течение 45 мин. После охлаждения реакционную смесь выливают в насыщенный водный раствор гидрокарбоната натрия и продукт экстрагируют этилацетатом. Объединенные органические фазы промывают водой и насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, получая при этом (7 vii) Следуя процедуре, аналогичной процедуре, описываемой на стадии v примера 1, продукт, полученный на предыдущей стадии (5,9 г), превращают в (7 viii) Следуя процедуре, аналогичной процедуре, описываемой на стадии i примера 1, продукт, полученный на предыдущей стадии (5,9 г), превращают в (7 ix) Следуя процедуре, аналогичной процедуре, описываемой на стадии ii примера 1, продукт, полученный на предыдущей стадии (1,4 г), превращают в (7 х) Следуя процедуре, аналогичной процедуре, описываемой на стадии iii примера 1, продукт, полученный на предыдущей стадии (1,3 г), превращают в (7 xi) Следуя процедуре, аналогичной процедуре, описываемой на стадии iv примера 1, продукт, полученный на предыдущей стадии (1,36 г), превращают в (7 xii) Следуя процедуре, аналогичной процедуре, описываемой на стадии v примера 1, продукт, полученный на предыдущей стадии (1,35 г), превращают в (7 xiii) Следуя процедуре, аналогичной процедуре, описываемой на стадии vi примера 1, продукт, полученный на предыдущей стадии (0,60 г), превращают в (7 xiv) Следуя процедуре, аналогичной процедуре, описываемой на стадии vii примера 1, продукт, полученный на предыдущей стадии (0,60 г), превращают в (7 Пример 7 (7 i) Раствор бис(триметилсилил)амида лития (20,2 ммоль) в тетрагидрофуране (35 мл) охлаждают до -40° С. По каплям добавляют раствор (7 ii) Смесь бромида метилтрифенилфосфония (17 г), трет-бутоксида калия (4,4 г) и безводного толуола (173 мл) нагревают при кипении с обратным холодильником в течение 1 ч. По каплям добавляют раствор кетона, полученного на предыдущей стадии (5,04 г), в безводном толуоле (40 мл) и нагревание продолжают в течение 3 ч. После охлаждения реакционную смесь выливают в насыщенный водный раствор хлорида аммония. Продукт экстрагируют этилацетатом; объединенные органические фазы промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Колоночная хроматография дает (7 iii) м-Хлорпербензойную кислоту (70-75%, 2,3 г) добавляют к раствору продукта, полученного на предыдущей стадии (3,0 г), в безводном дихлорметане (51 мл), содержащем твердый гидрокарбонат натрия (3 г). Реакционную смесь перемешивают при комнатной температуре в течение 3 ч; через 1 ч и 2 ч соответственно добавляют дополнительные порции м-хлорпербензойной кислоты (70-75%, 0,77 г). Реакционную смесь выливают в насыщенный водный раствор сульфита натрия и продукт экстрагируют дихлорметаном. Объединенные органические фазы промывают водным раствором гидроксида натрия (10%) и насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, получая при этом (7 iv) Следуя процедуре, аналогичной процедуре, описываемой на стадии iv примера 1, продукт, полученный на предыдущей стадии (2,85 г), превращают в (7 v) Следуя процедуре, аналогичной процедуре, описываемой на стадии v примера 1, продукт, полученный на предыдущей стадии (2,99 г), превращают в (7 vi) Следуя процедуре, аналогичной процедуре, описываемой на стадии vi примера 1, продукт, полученный на предыдущей стадии (0,30 г), превращают в (7 vii) Следуя процедуре, аналогичной процедуре, описываемой на стадии vii примера 1, продукт, полученный на предыдущей стадии (0,31 г), превращают в (7 Пример 8 (7 i) Гидроксид калия (3,28 г) добавляют к раствору (7 ii) Следуя процедуре, аналогичной процедуре, описываемой на стадии vi примера 1, продукт, полученный на предыдущей стадии (1,02 г), превращают в (7 iii) Следуя процедуре, аналогичной процедуре, описываемой на стадии vii примера 1, продукт, полученный на предыдущей стадии (1,05 г), превращают в (7 Пример 9 (7 i) Раствор (7 (ii) Следуя процедуре, аналогичной процедуре vi примера 1, продукт, полученный на предыдущей стадии (0,36 г), превращают в смесь (7 (iii) Следуя процедуре, аналогичной процедуре vii примера 1, продукт, полученный на предыдущей стадии (0,36 г), превращают в (7 iv) Раствор смеси, полученной на предыдущей стадии (0,32 г) в смеси безводного пиридина (1,50 мл) и безводного тетрагидрофурана (5 мл), содержащий 4-(диметиламино)пиридин (0,005 г), обрабатывают уксусным ангидридом (0,90 мл). Смесь перемешивают при комнатной температуре в течение 1,5 ч и затем гасят смесью лед-вода с последующим добавлением насыщенного водного раствора гидрокарбоната натрия. Продукт экстрагируют этилацетатом; объединенные органические фазы промывают водой, водной серной кислотой (2 М) и насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Колоночная хроматография дает (7 v) Раствор продукта, полученного на стадии iv (0,030 г), в метаноле (1 мл) обрабатывают раствором гидроксида натрия (0,009 г) в смеси метанола (0,3 мл) и воды (0,03 мл). Реакционную смесь перемешивают при комнатной температуре в течение 30 мин и выливают в смесь лед-вода. Продукт экстрагируют этилацетатом; объединенные органические фазы промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении, получая при этом (7 Пример 10 (7 i) Следуя процедуре, аналогичной процедуре, описываемой в примере 2, смесь (7 ii) Следуя процедуре, аналогичной процедуре, описываемой на стадии iv примера 9, смесь продуктов, полученных на i (0,060 г), ацетилируют и разделяют колоночной хроматографией, получая при этом (7 Пример 11 (7 i) Раствор (7 iia) Следуя процедуре, аналогичной процедуре, описываемой на стадии vi примера 1, (7 iib) Следуя процедуре, аналогичной процедуре, описываемой на стадии vi примера 1, (7 iiia) Следуя процедуре, аналогичной процедуре, описываемой на стадии vii примера 1, (7 iiib) Следуя процедуре, аналогичной процедуре, описываемой на стадии vii примера 1, (7 Пример 12 (7 i) Следуя процедуре, аналогичной процедуре, описываемой на стадии ii примера 1, смесь (7 ii) Следуя процедуре, аналогичной процедуре, описываемой на стадии i примера 11, продукт, полученный на предыдущей стадии (0,55 г), превращают в (7 iii) Следуя процедуре, аналогичной процедуре, описываемой на стадии vi примера 1, продукт, полученный на предыдущей стадии (0,14 г), превращают в (7 iv) Следуя процедуре, аналогичной процедуре, описываемой на стадии vii примера 1, продукт, полученный на предыдущей стадии (0,14 г), превращают в (7 Пример 13 (7 Указанное в заголовке соединение получают из (7 Пример 14 (7 Раствор (7 Пример 15 Следуя процедуре, аналогичной процедуре, описываемой на стадии v примера 1, и с использованием соединений примера 1, 2 и 8 соответственно в качестве исходного материала, были получены следующие продукты: а) (3 1H ЯМР (CDCl3) b1) (3 1H ЯМР (CDCl3) b2) (3 1H ЯМР (CDCl3) с1) (3 1H ЯМР (CDCl3) с2) (3 1H ЯМР (CDCl3) Пример 16 (7 i) Раствор (7 ii) Следуя процедуре, аналогичной процедуре, описываемой на стадии vi примера 1, продукт, полученный на предыдущей стадии (0,50 г), превращают в (7 iii) Следуя процедуре, аналогичной процедуре, описываемой на стадии vii примера 1, продукт, полученный на предыдущей стадии (0,69 г), превращают в (7 Пример 17 (7 i) Следуя процедуре, аналогичной процедуре, описываемой на стадии vi примера 1, (7 ii) Следуя процедуре, аналогичной процедуре, описываемой на стадии vii примера 1, продукт, полученный на предыдущей стадии (3,0 г), превращают в (7 iii) Следуя процедуре, аналогичной процедуре, описываемой на стадии ii примера 1, продукт, полученный на предыдущей стадии (2,51 г), превращают в (7 iv) Диэтилэфират трифторида бора (0,27 мл) добавляют к смеси продукта, полученного на предыдущей стадии (2,23 г), 1,2-этандитиола (0,67 мл), безводного тетрагидрофурана (10 мл) и безводного метанола (20 мл), охлажденной до 0° С. После перемешивания 2 ч при комнатной температуре реакционную смесь выливают в воду. Продукт экстрагируют этилацетатом; объединенные органические фазы промывают водным гидроксидом натрия (10%) и насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Колоночная хроматография дает циклический 3-(1,2-этандиилдитиоацеталь) (7 v) Следуя процедуре, аналогичной процедуре, описываемой на стадии iii примера 1, продукт, полученный на предыдущей стадии (2,68 г), превращают в (7 vi) Раствор продукта, полученного на предыдущей стадии (0,50 г), в диметилформамиде (7,3 мл) обрабатывают концентрированной хлористоводородной кислотой (0,73 мл). После перемешивания 1 ч при комнатной температуре реакционную смесь выливают в насыщенный водный раствор гидрокарбоната натрия и продукт экстрагируют этилацетатом. Объединенные органические фазы промывают насыщенным раствором соли, сушат над сульфатом натрия и концентрируют при пониженном давлении. Колоночная хроматография дает (7 Пример 18 Биологические результаты Соединения в соответствии с изобретением и четыре сравнительных соединения испытывали на андрогенную активность (процедуры для испытания которых были описаны выше) и оценивали в соответствии со следующей схемой: (-) не найдена андрогенная активность; (+) найдена андрогенная активность; (++) высокая андрогенная активность; (+++) превосходная андрогенная активность; (n.d.) нет данных; (pro) пролекарство. I. Соединения изобретения
Формула изобретения
1. Соединение, соответствующее структурной формуле где R1 представляет О, (Н,Н), (H,OR), NOR, причем R представляет водород, (С1-6)алкил, (С1-6)ацил; R2 представляет водород или (С1-6)алкил; R3 представляет водород или R3 представляет (С1-6)алкил, (С2-6)алкенил или (С2-6)алкинил, каждый из которых, необязательно, замещен галогеном; R4 представляет водород, (C1-6) алкил или (С2-6) алкенил; R5 представляет (C1-6) алкил; R6 представляет водород; R7 представляет водород или (C1-6) алкил; R8 представляет водород, гидрокси, галоген; R9 и R10, независимо, представляют водород или R9 и R10, независимо, представляют (C1-6)алкил, необязательно замещенный (C1-4)алкокси или галогеном; R11 представляет водород, SО3Н, (С1-15)ацил, пунктирные линии обозначают необязательные связи, выбранные из 2. Соединение по п.1, отличающееся тем, что заместитель R1 представляет О. 3. Соединение по п.1 или 2, отличающееся тем, что пунктирные линии означают двойную связь 4. Соединение по любому из предыдущих пунктов, отличающееся тем, что R4 представляет 7 5. Соединение (7 6. Соединение по любому из предыдущих пунктов для использования в терапии. 7. Соединение по любому из пп.1-5 для изготовления лекарственного средства, имеющего андрогенную активность. 8. Набор, обеспечивающий гормональную контрацепцию у особи мужского пола и включающий стерилизующее средство и андроген, отличающийся тем, что андроген представляет собой соединение по любому из пп.1-5. 9. Андрогенная композиция, включающая стероидное соединение по любому из пп.1-5, смешанное с фармацевтически приемлемым вспомогательным средством.
PC4A – Регистрация договора об уступке патента Российской Федерации на изобретение
(73) Патентообладатель(и):
(73) Патентообладатель:
Дата и номер государственной регистрации перехода исключительного права: 17.04.2007 № РД0020956
Извещение опубликовано: 27.05.2007 БИ: 15/2007
|
||||||||||||||||||||||||||

 -hydroxy-7
-hydroxy-7 -methyl-D-homoestra-4,16-dien-3-one: a highly potent orally active androgen” STEROIDS, N.Y., v.55, №2, 1990, p. 59-64.
-methyl-D-homoestra-4,16-dien-3-one: a highly potent orally active androgen” STEROIDS, N.Y., v.55, №2, 1990, p. 59-64.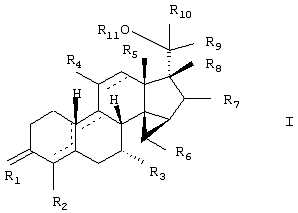
 4,
4, 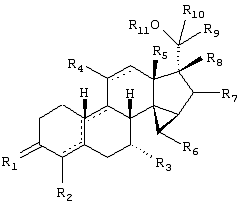
 s Pharmaceutical Sciences (18th ed., Mack Publishing Company, 1990, особенно см. часть 8: “Фармацевтические препараты и их изготовление”). Смесь стероидных соединений в соответствии с изобретением и фармацевтически приемлемого вспомогательного средства можно прессовать в твердые дозированные лекарственные формы, такие как пилюли, таблетки, или вводить в капсулы или суппозитории. При помощи фармацевтически приемлемых жидкостей соединения можно также применять в качестве препарата для инъекции в форме раствора, суспензии, эмульсии или спрея, например назального спрея. Для изготовления дозированных лекарственных форм, например таблеток, рассматривается использование общепринятых добавок, таких как наполнители, красители, полимерные связующие и тому подобное. В общем, можно использовать любую фармацевтически приемлемую добавку, которая не препятствует действию активного соединения. Стероидные соединения изобретения можно также включать в имплантат, вагинальное кольцо, пластырь, гель и любой другой препарат для длительного высвобождения (активного соединения).
s Pharmaceutical Sciences (18th ed., Mack Publishing Company, 1990, особенно см. часть 8: “Фармацевтические препараты и их изготовление”). Смесь стероидных соединений в соответствии с изобретением и фармацевтически приемлемого вспомогательного средства можно прессовать в твердые дозированные лекарственные формы, такие как пилюли, таблетки, или вводить в капсулы или суппозитории. При помощи фармацевтически приемлемых жидкостей соединения можно также применять в качестве препарата для инъекции в форме раствора, суспензии, эмульсии или спрея, например назального спрея. Для изготовления дозированных лекарственных форм, например таблеток, рассматривается использование общепринятых добавок, таких как наполнители, красители, полимерные связующие и тому подобное. В общем, можно использовать любую фармацевтически приемлемую добавку, которая не препятствует действию активного соединения. Стероидные соединения изобретения можно также включать в имплантат, вагинальное кольцо, пластырь, гель и любой другой препарат для длительного высвобождения (активного соединения).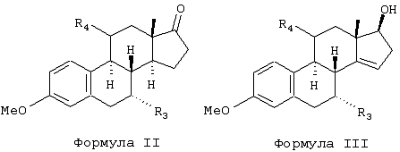
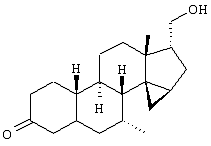
 5,80 (шир.с, 1H), 3,69 (м, 1H), 3,50 (м, 1Н), 1,09 (с, 3Н), 0,62 (д, 3Н, J=7,1 Гц), 0,47 (дд, 1H, J=8,3 и 5,1 Гц), 0,28 (дд, 1H, J=5,1 и 3,5 Гц).
5,80 (шир.с, 1H), 3,69 (м, 1H), 3,50 (м, 1Н), 1,09 (с, 3Н), 0,62 (д, 3Н, J=7,1 Гц), 0,47 (дд, 1H, J=8,3 и 5,1 Гц), 0,28 (дд, 1H, J=5,1 и 3,5 Гц).